|
|
Tratamiento farmacológico de personas viviendo con
VIH-SIDA
Impacto de
la Licencia Obligatoria de DOLUTEGRAVIR y Combinaciones
en Colombia
CONTEXTO:
Después de la declaratoria de existencia de razones de
interés público para someter la patente del principio
activo Dolutegravir a licencia obligatoria en la
modalidad de uso gubernamental (mediante la
Resolución N° 01579 de 2023
armi) el 23 de abril de 2024 la
Superintendencia de Industria y Comercio SIC expidió la
Resolución No. 20049 de 2024
armi, que concedió la
Licencia Obligatoria para Uso Gubernamental (LOUG) de
DOLUTEGRAVIR, (TIVICAY®).
Esta
medida que -por primera vez se expidió en
Colombia- ya entró en vigencia, pese a las
acciones legales
interpuestas por AFIDRO
armi. y otros actores que le respaldaron.
La adquisición del primer lote y las dificultades que se
presentaron para su introducción, plantean la necesidad
de reunir los hechos objetivos que respaldan la
pertinencia de la medida del gobierno para promover este tratamiento,
por su
✔mayor eficacia,
✔menores efectos secundarios y
✔mejor
relación costo-beneficio, en su propósito de defender
los intereses
de la salud pública, al margen de las acciones legales que se
interpongan en su contra.
En esa línea, el 20 de agosto de 2024 el
Ministerio de Salud
publicó el Proyecto
de Resolución armi y
su respectiva Memoria
Justificativa armi,
estableciendo un período de consulta pública de la norma hasta
el Miércoles 28 de agosto de 2024. Ver la evolución
completa en los enlaces del TEMARIO
COYUNTURA ACTUALIZADA 2025
La implementación de la primera Licencia Obligatoria
en Colombia y tres demandas de
oposición están en marcha. Tanto las experiencias
concretas de la implementación como la resolución de las
demandas tendrán un gran impacto en la salud pública y
las finanzas del sistema de salud. Por lo tanto es necesario revisar
y generar
evidencia científica, para contar con elementos fácticos que sirvan
para la defensa del interés público en
cualquiera de dichos escenarios, incluido el próximo
vencimiento de la patente reclamada por GSK.
En la coyuntura actual, es importante definir por
ejemplo:
✔Si
la combinación triple elegida por la OPS sigue siendo la
mejor alternativa,
✔Si
conviene impulsar la doble (Dolutegravir+Lamivudina)
como lo está haciendo GSK,
✔Cuál
sería la mejor respuesta en términos científicos y
económicos en caso de fallos contrarios de las demandas
en curso,
✔Cuál
la situación de patente de Bictegravir y las
posibilidades de reemplazo de DTG
✔Cuáles
las consecuencias de suspender el suministro y
tratamientos con Dolutegravir y
✔Cuáles
serían las alternativas para enfrentar consecuencias del
desabastecimiento DTG.
Ver ejemplo:
Estudio Piloto Indetectabilidad Con Dolutegravir En
Migrantes_27oct25 |
TEMARIO:
1.
Introducción: Información económica y terapéutica de
fármacos en el sistema de salud
2.
Antivirales VIH-SIDA en Colombia según reportes a SISMED
de los años 2015 a 2024
2.1.
Validación y análisis de Transacciones Primarias,
Secundarias y Finales en SISMED
2.2.
Validación y análisis de reportes de Antivirales VIH
Colombia en Sismed de 1T2021 a 4T2024
2.3.
Ventas de principales 5 Antivirales VIH SIDA, según
SISMED del Trimestre 4° de 2024
2.4.
Evolución de ventas de Dolutegravir y sus Combinaciones
de años 2014 a 2023 y 2024
2.5.
Validación y análisis de datos de Dolutegravir (Tivicay®)
en SISMED del 4T2023 y 2024
2.6.
Validación y análisis de ventas de Dolutegravir (Tivicay®)
a SISMED de 2022, 2023 y 2024
2.6.1.
Validación y análisis de datos de Tivicay® CUM
20071938-01 en Trimestres 1°2022 a 4°2024
2.6.2.
Validación y análisis de datos de Tivicay® CUM
20071938-02 en Trimestres 1°2022 a 4°2024
2.6.3.
Validación y análisis de Dolutegravir+Abacavir+Lamivudina
(Triumeq®) de Trimestres 1°2022 a 4°2024
2.6.4.
Validación y análisis de Dolutegravir+Lamivudina (Dovato®)
de Trimestres 1°2022 a 4°2024
2.6.5.
La Combinación Lamivudina+Dolutegravir está
evolucionando más dinámicamente en la actualidad
2.7.
Validación y análisis Ventas Trimestrales Dolutegravir y
Combinaciones de Trimestres 1°2020 a 4°2024
2.7.1.
Validación y análisis Ventas Trimestrales Dolutegravir y
Combinaciones de Trimestres 1°2020 a 4°2023
2.7.2.
Validación y análisis Ventas Trimestrales Dolutegravir y
Combinaciones de Trimestres 1°2021 a 4°2024
2.7.3.
Prescripciones de DOLUTEGRAVIR y Combinaciones por
Región y por EPS en años 2021 a 2025
2.7.4.
Evolución de ventas anuales de GlaxoSmithKline
reportadas a SISMED 2014 a 2024
2.7.5.
Importancia de DOLUTEGRAVIR y Combinaciones para
GlaxoSmithKline Trimestres 4°2023 y 4°2024
3.
VIH-SIDA en Colombia según Informes de la CAC, GPC,
IETS, SIVIGILA y el INS de años 2022 a 2024
3.1.
VIH-SIDA en Colombia según Informes Cuenta de Alto Costo
CAC de los años 2022 a 2024
3.2.
Situación del VIH-SIDA en Colombia según Guías de
Práctica Clínica de 2021 y 2024
3.3.
Situación del VIH-SIDA en Colombia según el IETS y
SIVIGILA del INS de 2022 a 2024
3.4.
Litigio en curso y alternativas posibles en caso de
Derogatoria de la Licencia Obligatoria
4.
Lamivudina+Tenofovir Disoproxil + Dolutegravir la opción
STR seleccionada y disponible en OPS
4.1.
Combinación Biktarvy que es monopólica y sin precio
regulado pero posiblemente no patentable
4.2.
Lamivudina+Tenofovir Disoproxil+Dolutegravir: Opciones
similares a opción OPS con DTG
4.3.
Combinaciones disponibles con Emtricitabina y Tenofovir
Disoproxil o Tenofovir Alafenamida
4.4.
Emtricitabinas disponibles en Colombia (sin Bictegravir
que podría resultar no patentable)
4.5.
Combinación Emtricitabina y Tenofovir Alafenamida ahora
con
protección de patente negada
4.6.
Total ventas Tenofovir Disoproxil sin protección de patente para
diversas combinaciones
4.7.
Ventas de Lamivudina sin Dolutegravir reportadas a
SISMED de 2014 a 2023 y 2015 a 2024
5.
Proyección de acciones coyunturales de Litigio y
organizacionales desde gremios de la salud
6.
Proyección de cambios estructurales en el sistema de
salud Ley 2386/24 de Soberanía Farmacéutica
7.
Construcción del Sistema Integrado Transaccional y Distribuido de
Información en Salud SITDIS |
1.
1. Introducción:
Información económica y terapéutica de fármacos
en el sistema de salud
La fragmentación del sistema de información de la salud en
Colombia
constituye su mayor deficiencia estructural y esta característica
es particularmente crítica en relación con la
información
económica y terapéutica de medicamentos. En la actualidad, esa información se encuentra
fragmentada en múltiples subsistemas con inconsistencia propias
y problemas serios de falta Validación, Analítica e integración de datos.
Este estudio, intentará obtener
conclusiones a partir de un proceso de Validación, Analítica e Integración
(VAI) de datos tomados de los siguientes Subsistemas de
Información:
✔ Sistema de Información de Precios de Medicamentos SISMED
dependiente del
Ministerio de Salud y Protección Social y su Oficina de
Tecnologías de Información y Comunicaciones (OTIC) que
funcionan como Secretaría Técnica de la Comisión Nacional de
Precios de Medicamentos y Dispositivos Médicos CNPMyDM,
✔ Instituto Nacional de
Vigilancia de Medicamentos y Alimentos INVIMA, responsable
de la base de datos de registros sanitarios de medicamentos
disponibles en Colombia y los aspectos regulatorios
correspondientes,
✔ Cuenta de
Alto Costo CAC, responsable de la información focalizada y
específica del manejo de las patologías de mayor impacto
económico y epidemiológico en el sistema de salud colombiano
✔ Instituto Nacional de Salud
INS,
Instituto de Evaluación Tecnologica en Salud IETS y demás Subsistemas que tengan alguna
relación importante con el tratamiento de VIH y SIDA en el país.
Para contextualizar este proceso de Validación, Analítica e Integración
(VAI) de datos deben tomarse en cuenta las siguientes
aclaraciones:
✔ SISMED,
el
Sistema de Información de Precios de Medicamentos que con su
respectivo Cubo de acceso al
microdato, fue la base de datos más robusta de reportes
trimestrales de ventas y precios de todos los actores de la
cadena de medicamentos (producción, importación,
comercialización, cobros y recobros al sistema de salud) en la
actualidad tiene utilidad disminuida por sus múltiples inconsistencias.
La regulación de precios,
que otrora fue ejemplo de política pública exitosa, hoy presenta
casos con inconsistencias. Pese a sus problemas de cobertura
(incluye datos del régimen contributivo pero no incluye datos
del régimen subsidiado ni de regímenes especiales como Fuerzas
Armadas. FECODE, Banco de la República, etc.) y que OTIC
la
Oficina de Tecnologías de Información y Comunicación de MinSalud,
no valida ni analiza los datos reportados, SISMED sigue siendo
la mejor fuente de datos económicos. Obviamente, el análisis de
estos datos deberá complementarse con información del
✔ Cubo
MI-PRES, especialmente cuando se implemente la
Resolución 2164 de 2024 del Ministerio de Salud y Protección
Social. que permite la prescripción de Dolutegravir a través de
esta plataforma (aplicativo diseñado para obtener información de
prescripciones de tecnologías de alto costo, por indicación,
región, EPS, etc. que actualmente está inactivo por la implementación del pago anticipado
de los "presupuestos máximos" que acabaron con esa trazabilidad)
✔ ADRES,
el "Banco de la salud" que en la actualidad
tiene buenos niveles de transparencia en relación con los
destinatarios de los pagos que realiza, pero es un "pagador ciego
de destinaciones específicas" porque no publica el microdato de los pagos
correspondientes a
medicamentos y tecnologías en salud. Es decir, permite conocer
los beneficiarios de los pagos que r4ealiza (a quién), pero no
identifica el producto específico (por CUM o CUPS) objeto del
pago, además según facturación electrónica de la
DIAN,
✔ INVIMA,
el Instituto Nacional de
Vigilancia de Medicamentos y Alimentos que reúne información
farmacológica y regulatoria de medicamentos autorizados para su
comercialización en Colombia. Tomaremos los datos necesarios de
los principios activos y registros sanitarios vigentes. No
tomaremos el Código de Clasificación ATC de esta base de datos
porque tiene inconsistencias, tomaremos los Códigos ATC del
Instituto de Salud Pública de Noruega NIPH (Centro de
Coordinación de Metodología de las Estadísticas de Drogas de la
OMS) porque son universales y libres de error. Tampoco tomaremos
los datos del Identificador Único del Medicamento IUM porque
está incompleto y trabajaremos con el Código Único del
Medicamento CUM, que es simple, corresponde al número del
expediente sanitario y dos dígitos de verificación de cada
presentación y puede ser construido con los datos publicados.
✔
CAC, la
Cuenta de
Alto Costo creada para el seguimiento de
Artritis Reumatoide,
Hemofilia,
ERC,
VIH,
Cáncer y
Cáncer, publica in
formes periódicos sobre el manejo de VIH y SIDA en el sistema de
salud colombiano. Será la fuente de los aspectos clínicos y
epidemiológicos de este estudio al igual que
IETS, el
Instituto de Evaluación Tecnologica en Salud (que elabora
guías, manuales y evaluaciones sobre
Enfermedades
Cardiovasculares y
Respiratorias,
Cáncer,
así como
Enfermedades Infecciosas,
Neurológicas,
Ginecológicas,
Musculares Osteomusculares y
Dermatológicas) pese a su falta de actualización.
El presente estudio no incluye datos de
✔ MedColSTAT,
que como puede verse en
https://pospopuli.minsalud.gov.co/MEDCOL-STAT/POSEstadisticasMedicamentos.aspx
tiene información reportada por las EPS de los años 2014 a 2021.
Su utilidad es
discutible por su falta de actualización y seguimiento, tanto
que el propio Ministerio de Salud
debe
solicitar informes específicos para el cálculo dke
suficiencia de la Unidad de Pago por Capitación UPC.
•
En Síntesis,
todos los subsistemas de información
del sistema de salud colombiano presentan inconsistencias y el
nivel de integración es casi nulo. Esta investigación intentará
obtener conclusiones a partir de un proceso de Validación,
Análísis e Integración (VAI) de datos de los subsistemas
vigentes.
•
Proyectamos iniciar el
proceso DP+AT+AD+AP (Derecho de Petición + Acción de
Tutela + Acción de Desacato + Acción Penal 'por Fraude a
Resolución Judicial) para exigir que el Ministerio de Salud
instituya las Rutinas VAI que correspondan en los Subsistemas de
información en orden de prioridad por mayor impacto. |
2.
2. Antivirales VIH-SIDA en Colombia según reportes a SISMED de
los años 2015 a 2024
De acuerdo con reportes de Laboratorios a SISMED, las ventas de
medicamentos antivirales para VIH SIDA en Colombia se
mantuvieron entre 4.200.152 unidades (1) por casi
132.533 millones de COP corrientes en 2015 y casi casi 6
millones de unidades por casi 180.000 millones de COP
corrientes en 2020. En 2021, posiblemente en relación con la
pandemia de COVID-19, las ventas de este grupo de medicamentos
se redujeron a 1.979.437 unidades por casi 178.100 millones
(COP corrientes). A partir del año 2021 los reportes de
Transacciones Primarias Institucionales y Comerciales de Actores
que fabrican o importan estos medicamentos evolucionaron
dinámicamente hasta 6.134.189 unidades por COP
396.432.386.862 el año 2024 (4). El acumulado de la década
2025 a 2024 -con ambos sistemas de reporte- llegó a
45.747.840 unidades diversas por 1.986.304.226.577 COP
en valores corrientes.
|
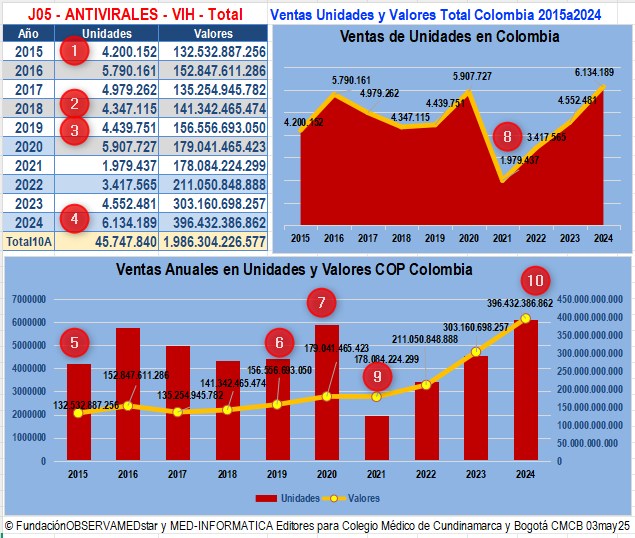
Gráfico N°1: Mercado Total de
Antivirales VIH-SIDA Colombia según reportes de Laboratorios
Farmacéuticos a SISMED de años 2015 a 2024 |
|
 |
Ventas Farma VIH_SIDA Colombia 2021-2024
Según reportes a SISMED de Transacciones
Primarias (de Farmacéuticas) 1T2021 a 4T2024
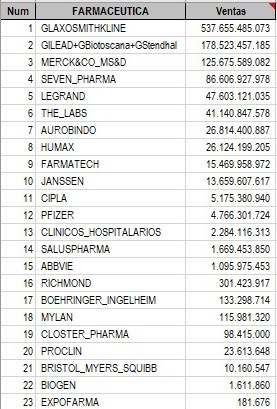
Unificamos los reportes de GILEAD con Antivirales
VIH_SIDA de GILEAD reportados por BIOTOSCANA
y por STENDHAL. Las Transacciones Primarias
corresponden a Ventas Institucionales y Comerciales
de actores que fabrican o importan medicamentos |
|
El gráfico N°1
muestra los valores mencionados en el párrafo anterior y
en el recuadro pueden verse los valores acumulados de
reportes de Transacciones Primarias Institucionales y
Comerciales de los trimestres 1° de 2021 a 4° de 2024
ordenados por firma farmacéutica. Nótese el alto
grado de concentración de este mercado con un 64 % de
participación correspondiente a solo 2 Laboratorios:
El 48% a
GLAXOSMITHKLINE y el 16% a GILEAD (en comarketing con BIOTOSCANA
Y STENDHAL), |
Definidas las principales
características de las ventas de Antivirales para VIH SIDA en
Colombia en la década 2015-2024. resulta importante conocer con
mayor detalle la evolución trimestral de ventas en unidades y
valores en los años 2021 a 2024, así como la situación
actualizada en el cuarto trimestre de 2024
2.1.
2.1. Validación y análisis de Transacciones Primarias,
Secundarias y Finales en SISMED
Antes de analizar la información de las Transacciones Primarias,
Secundarias y Finales que se publican en SISMED resulta
indispensable mostrar el tipo de validación simple a que
fue sometida dicha información para este estudio. En el gráfico
N°2 se muestra la existencia de datos absurdos en los
reportes de estas transacciones en SISMED, tanto en las ventas
de unidades y valores (siendo los reportes del 2° trimestre de
2022 y del 2° trimestre de 2023 los más absurdos). Se resaltan
en campos rojos los datos absurdos de Transacciones Primarias,
en color azul los de Transacciones Secundarias y en naranja los
de Transacciones Finales
Gráfico N°2: Inconsistencias más
frecuentes en la información de Transacciones Primarias,
Secundarias y Finales que se publican en SISMED
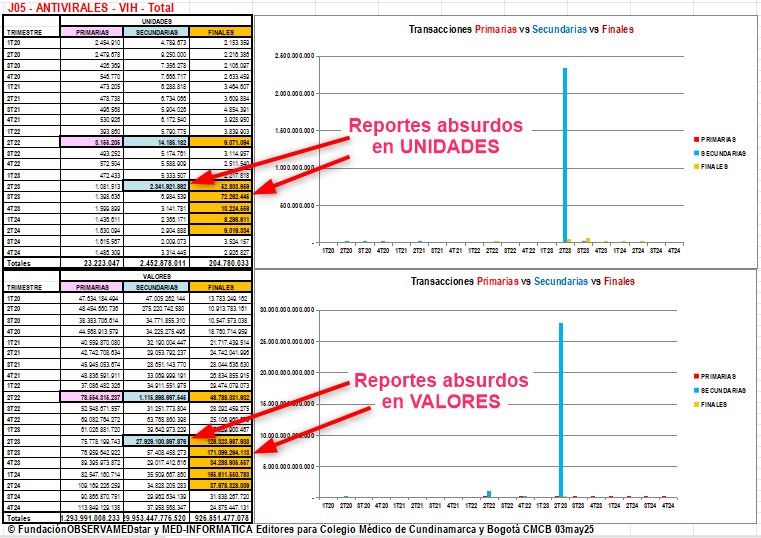
Al corregir los datos absurdos
encontrados en el proceso de validación simple y
reemplazar los valores absurdos con datos del reporte del
período anterior, puede verse que el gráfico cambia
radicalmente. Así, en el gráfico N°3 ya puede verse la mayor
importancia de las ventas de unidades en las Transacciones
secundarias y su evolución decreciente (columnas azules) frente
a la mayor importancia y evolución dinámicamente creciente de
las ventas en valores de Transacciones Primarias (columnas
rojas), algo que sugiere la importancia del impacto creciente de
los precios.
Gráfico N°3: Aspecto de los gráficos luego de validar y
corregir datos absurdos de Transacciones Primarias, Secundarias
y Finales en SISMED
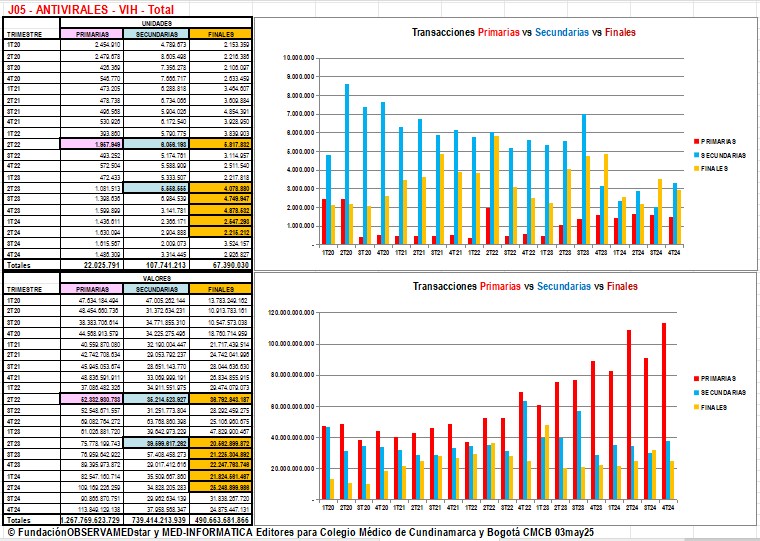
Este gráfico muestra la tendencia claramente decreciente de
las ventas de unidades en las Transacciones Secundarias (entre
diferentes actores del sistema) y la tendencia claramente
creciente de las ventas en valores de las Transacciones
Primarias (reportadas por actores que importan estos
medicamentos).
- Problemas de
Consistencia de Datos: Antes de proceder con el
análisis de la información de Transacciones Primarias,
Secundarias y Finales publicada en SISMED, se llevó a cabo
una "validación simple". Esta validación reveló la
existencia de "datos absurdos" en los reportes de
ventas en unidades y valores. Los reportes de los
segundos trimestres de 2022 y 2023 fueron identificados como
los más problemáticos en cuanto a estos datos
inconsistentes. Los datos absurdos se resaltaron en color
rojo para las Transacciones Primarias, en azul para las
Secundarias y en naranja para las Finales.
- Impacto de las
Correcciones: Al corregir estos datos absurdos,
sustituyéndolos con información del período anterior, se
observó un cambio radical en los gráficos. Las ventas en
unidades de las Transacciones Secundarias mostraron una
tendencia decreciente, mientras que las ventas en valores de
las Transacciones Primarias (reportadas por los actores que
importan medicamentos) evidenciaron una importancia mayor y
un crecimiento dinámico, lo que sugiere un creciente
impacto de los precios.
- Deficiencia en la
Calidad de la Información y Acción Tomada: La
presencia de valores absurdos en los datos reportados
deteriora gravemente la calidad de la información.
La corrección simple mediante el reemplazo de datos con los
del período anterior se considera demasiado básica y
potencialmente inexacta. Por esta razón, el Colegio Médico
de Cundinamarca y Bogotá (CMCB) interpuso un Derecho de
Petición ante las entidades responsables y de vigilancia
para que realicen la validación y corrección adecuadas de la
información.
2.2.
2.2. Validación y
análisis de reportes
Antivirales VIH Colombia en Sismed 1T2021a4T2024
De acuerdo con reportes trimestrales de Transacciones
Primarias Institucionales y Comerciales de actores que fabrican
y/o importan medicamentos Antivirales para VIH SIDA de los
trimestres 1° de 2021 a 4° de 2024, la opción más vendida en
unidades fue Tenofovir Disoproxil + Emtricitabina de Seven Pharma,
seguida de Dolutegravir solo (Tivicay de
Glaxosmithkline) y sus
combinaciones con Lamivudina (Dovato) y con Lamivudina
+ Abacavir (Triumeq) todos 3 de Glaxosmithkline,
así como Raltegravir (Isentress de Merck&Co-MSD). Ver gráfico
N°3, en la parte superior.
Gráfico N°3: Ventas de
Antivirales VIH SIDA en Colombia, según reportes de
Transacciones Primarias en SISMED de los años 2021 a 2024
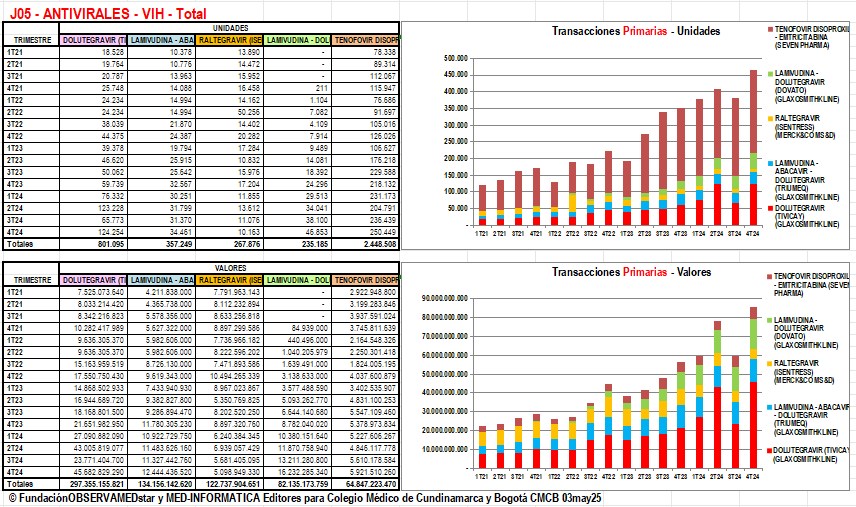
En valores, la opción más
vendida fue Dolutegravir (Tivicay) junto con sus
combinaciones con Lamivudina (Dovato) y con Lamivudina
+ Abacavir (Triumeq) todos 3 de Glaxosmithkline.
Les siguieron Raltegravir (Isentress de Merck&Co-MSD) y
Tenofovir Disoproxil + Emtricitabina de SevenPharma. Ver gráfico N°3, en la parte inferior.
El gráfico N°3 muestra la mayor
importancia y tendencia creciente de las ventas de unidades
de Tenofovir Disoproxil + Emtricitabina de Seven Pharma y
en valores la sustancialmente mayor importancia y
evolución dinámica de Dolutegravir solo (Tivicay de
Glaxosmithkline) y sus
combinaciones con Lamivudina (Dovato) y con Lamivudina
+ Abacavir (Triumeq) todos 3 de Glaxosmithkline,
que prácticamente monopoliza este mercado, claramente con
precios más elevados.
2.3.
2.3.
Ventas de principales 5 Antivirales VIH SIDA, según SISMED del
Trimestre 4° de 2024
Para estimar la situación actual de las ventas de los
principales Antivirales VIH SIDA en Colombia, es necesario
revisar los reportes de Transacciones Primarias
Institucionales y Comerciales de actores que fabrican y/o
importan estos medicamentos en el trimestre
4° de 2024. El gráfico N°4 en su parte superior muestra que la opción más vendida en
unidades siguió siendo Tenofovir Disoproxil
+ Emtricitabina de Seven Pharma, seguida de Dolutegravir
solo (Tivicay) con sus
combinaciones con Lamivudina (Dovato) y con Lamivudina
+ Abacavir (Triumeq) todos 3 de Glaxosmithkline
y Darunavir + Ritonavir de TheLabs)
Gráfico N°4:
Ventas de
Antivirales VIH SIDA en Colombia, según reportes de
Transacciones Primarias en SISMED del 4° trimestre de 2024
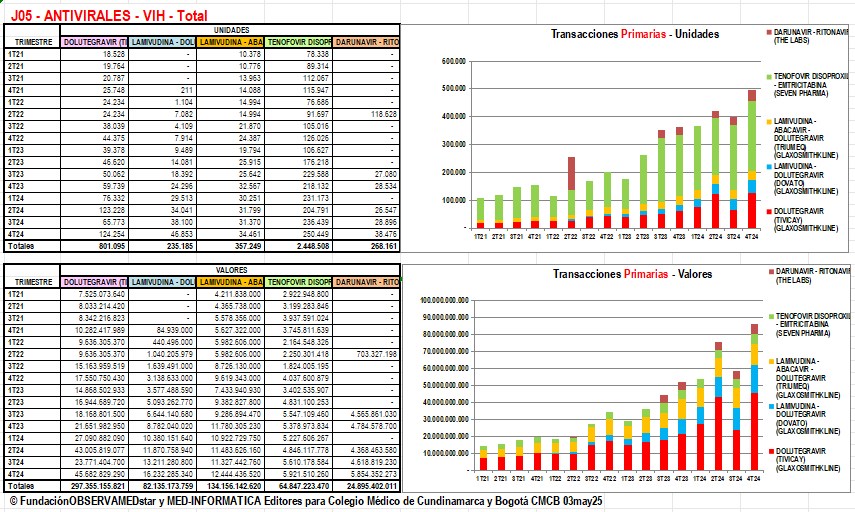
En valores (parte baja del Gráfico N°4) las opción más
vendida también continuó siendo Dolutegravir (Tivicay)
seguida de sus combinaciones con Lamivudina (Dovato)
y con Lamivudina + Abacavir (Triumeq) de Glaxosmithkline
que prácticamente sigue monopolizando este mercado,
claramente con precios más elevados.
De acuerdo con reportes
trimestrales del 1° de 2021 hasta el 4° de 2024 puede decirse
que Dolutegravir (Tivicay) y sus combinaciones con
Lamivudina (Dovato) y con Lamivudina + Abacavir
(Triumeq) de Glaxosmithkline dominan amplia y
crecientemente el mercado de Antivirales para VIH SIDA en
Colombia. algo que se hace cada vez más evidente desde la
introducción de Triumeq (2015) y Dovato (2021) hasta los últimos
reportes del 4° trimestre de 2024 (Gráfico N°4),
2.4.
2.4. Evolución de
ventas de DOLUTEGRAVIR y sus Combinaciones de 2014 a 2023 y 2024
DOLUTEGRAVIR (TIVICAY® de GLAXOSMITHKLINE) obtuvo su Registro
Sanitario en 2014 (INVIMA 2014M-001555) y la renovó en 2019 (INVIMA
2019M-0015552-R1), Inició sus reportes a SISMED el año 2015. La
combinación LAMIVUDINA + ABACAVIR + DOLUTEGRAVIR (TRIUMEQ®) se registró en 2015 (INVIMA 2015M-0016583) y sus ventas
se reflejaron significativamente en SISMED desde 2019. La
combinación LAMIVUDINA + DOLUTEGRAVIR (DOVATO®) se
registró en 2021 (INVIMA 2021M-0020330). En 9 años, de 2015 a
2023 el acumulado de ventas de unidades diversas reportadas a
SISMED por el laboratorio superaron el millón y las ventas
en valores llegaron a $400.000 millones. La estrategia de
desarrollar mercados con combinaciones de moléculas y el
argumento de mayor adherencia, mejores resultados terapéuticos y
menores efectos secundarios resultó muy beneficioso para
GlaxoSmithKline en Colombia. No es de extrañar que esta
tendencia se haya extendido a nivel mundial con el nombre de "Single Treatment Regimen STR".
|
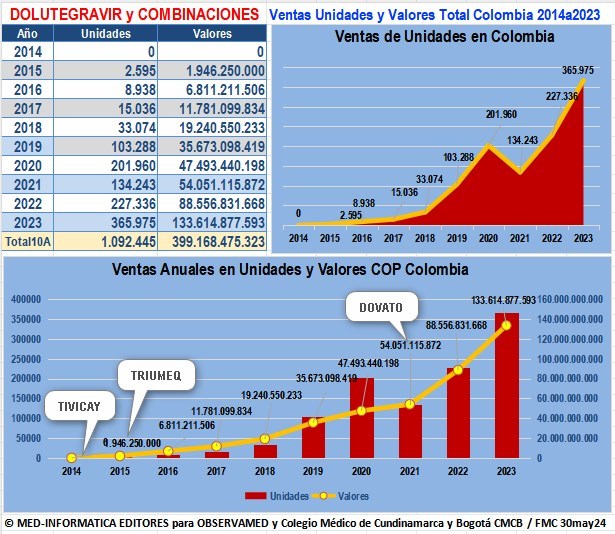
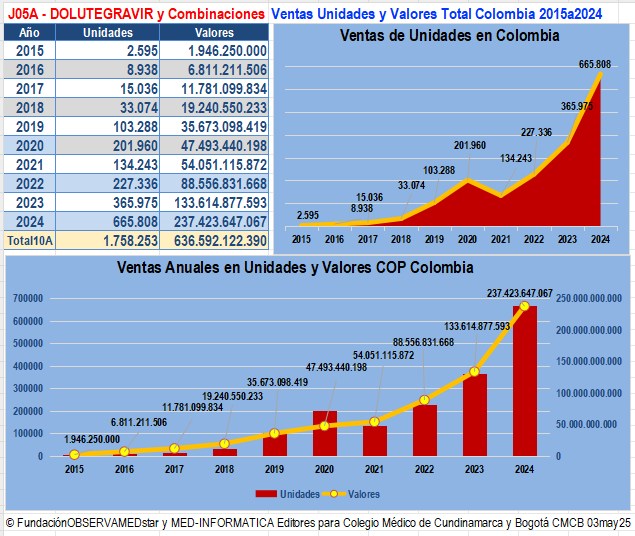
Gráfico N°5: DOLUTEGRAVIR y
sus Combinaciones: Evolución de ventas anuales en unidades y valores
reportados a SISMED de 2014
a 2023 y hasta 2024 |
|
 |
 |
|
.
Según datos reportados por GlaxoSmithKline a SISMED, en
2015 Dolutegravir
(Tivicay®)
vendió 2.595 unidades
por algo más de COP 1.946 millones y con la
introducción de sus combinaciones con Lamivudina y Abacavir (Triumeq
en 2015)
y con Lamivudina (Dovato en 2021) el año 2023 pasó a vender
365.975 unidades por más de COP $133,000
millones. En 2024 esos valores ascendieron a 665.808
unidades por casi COP 237.424 millones. Estos
gráficos permiten visualizar la evidente maximización de
beneficios que está implícita en la introducción de
combinaciones "fijas" con el discurso de "mejoría de
adherencia, aumento de eficacia y disminución de efectos
secundarios" impulsada por las farmacéuticas. La
protección de la propiedad intelectual que se otorga con
las patentes para una exclusividad de beneficios durante
20 años, siendo legal y suficiente, no debería
acelerarse ni extenderse con mecanismos que limitan la
investigación y la competencia como la "protección de
datos" del Decreto 2085 vigente en Colombia y las
técnicas llamadas de "evergreening" perennización o
sobreexplotación que se emplean a nivel mundial con la
adición de componentes, solo excipientes y hasta solo
nuevas formas farmacéuticas. |
2.5.
2.5.
Validación y análisis de datos Dolutegravir (Tivicay®)
en SISMED
del 4T2023 y 2024
En
la pantalla de seguimiento por Principio Activo del
Sistema VMI-CFN
puede verse que Dolutegravir (Tivicay® 50 mg de GLAXOSMITHKLINE
COLOMBIA S.A.) fue incluido en Normas Farmacológicas con Código
4.1.3.0.N10. El Código ATC J05AX12 asignado en la
base de datos del INVIMA está desactualizado. El ATC actualizado
por la OMS es J05AJ03. Dolutegravir obtuvo Protección del
Decreto 2085 (Patente Express) con vigencia del 5 de enero de
2015 al 5 de enero de 2020 (Acta 45 de 2013 numeral
3.1.1.2). Sus precios aparecen regulados en las últimas
Circulares de la Comisión Nacional de Precios de Medicamentos
CNPM y el Plan de Beneficios PBS incluye todas las
concentraciones y formas farmacéuticas.
. Gráfico N°6: Pantalla
de seguimiento del Principio Activo DOLUTEGRAVIR en el
Sistema VMI-CFN
con información
económica del
4° trimestre de 2023
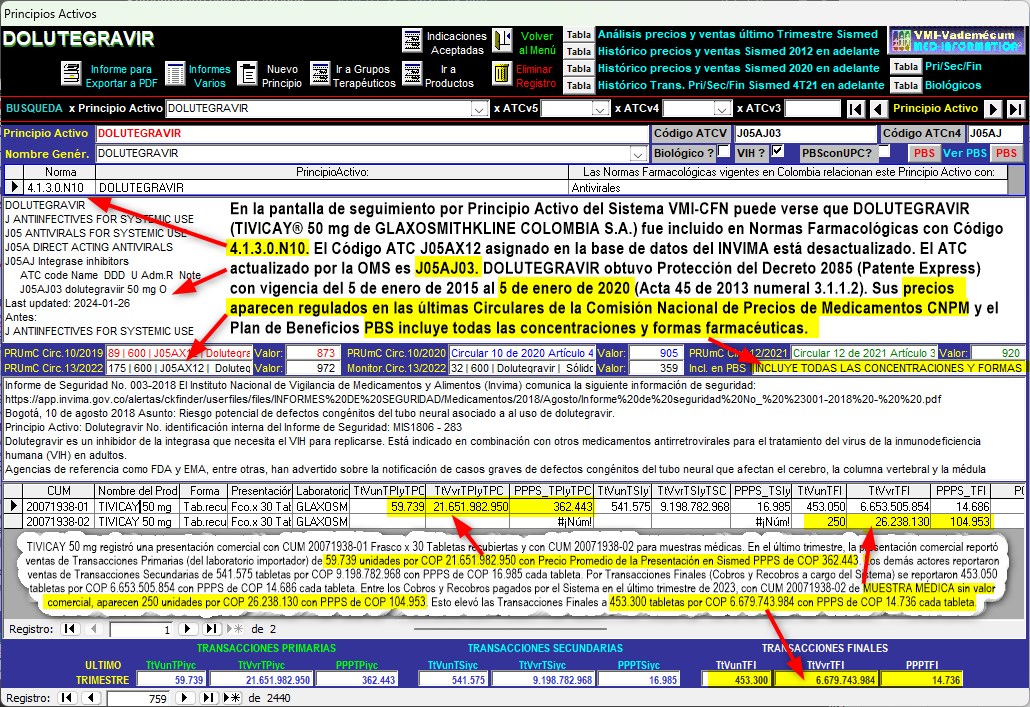
TIVICAY 50 mg registró una presentación comercial con CUM
20071938-01 Frasco x 30 Tabletas recubiertas y con CUM
20071938-02 para muestras médicas "sin valor comercial".. En el
4° trimestre de
2023, la presentación comercial reportó ventas de
Transacciones Primarias (datos monofuente del laboratorio importador) de
59.739 unidades por COP 21.651.982.950 con Precio
Promedio de la Presentación en Sismed PPPS de COP 362.443.
Los demás actores del sistema reportaron Transacciones
Secundarias de 541.575 tabletas por COP
9.198.782.968 con PPPS de COP 16.985 cada tableta
(datos multifuente con muchas inconsistencias).
Como Transacciones Finales (Cobros y Recobros a cargo del
Sistema) se reportaron 453.050 tabletas por COP
6.653.505.854 con PPPS de COP 14.686 la tableta.
Nótese que como Cobros pagados por el Sistema en 4°
trimestre de 2023, con CUM 20071938-02 de MUESTRA MÉDICA
sin valor comercial, aparecen 250 unidades por COP
26.238.130 con PPPS de COP 104.953, algo ilegal que elevó
los pagos del sistema de salud (Transacciones Finales) a 453.300 tabletas por COP
6.679.743.984 con PPPS de COP 14.736 la tableta.
Gráfico N°7: Enfasis en cambios de datos
económicos en Pantalla de
seguimiento del Principio Activo DOLUTEGRAVIR correspondiente al
4° trimestre de 2024


Según el seguimiento del
Sistema VMI-CFN,
en el 4° trimestre de
2024, TIVICAY 50 mg CUM
20071938-01 Frasco x 30 Tabletas recubiertas de
GlaxoSmithKline pasó a reportar ventas de
Transacciones Primarias (del Laboratorio) de
124.254 unidades por COP 45.682.829.290 con Precio
Promedio de la Presentación en Sismed PPPS de COP 367.657.
Los demás actores del sistema reportaron Transacciones
Secundarias de 576.114 unidades por COP
10.816.289.361 con PPPS de COP 18.775 cada tableta.
Como Transacciones Finales (Cobros y Recobros a cargo del
Sistema) se reportaron 464.987 tabletas por COP
6.140.780.082 con PPPS de COP 13.206.
Y con CUM
20071938-02 de MUESTRAS MÉDICAS "sin valor comercial" aparecen
transacciones secundarias de 30 unidades por COP
431.820 con PPPS de COP 14.394 y como cobros y
recobros se reportaron 420 unidades por COP 18.409.320 con PPPS de COP
43.832, algo ilegal no detectado ni corregido. En
Transacciones Primarias el total del 4° trimestre de 2024 se
mantuvo en
124.254 unidades por COP 45.682.829.290 con Precio
Promedio de la Presentación en Sismed PPPS de COP 367.657,
el total de Transacciones
Secundarias pasó a 576.144 unidades por COP
10.816.721.181 con PPPS de COP 18.774 y el total de
Transacciones Finales (Cobros y Recobros a cargo del
Sistema) pasó a 465.407 tabletas por COP
6.159.189.402 con PPPS de COP 13.234 cada tableta.
Importante: No aparecen en esta pantalla CUM
20143772-01 SANTIGRASE Dolutegravir Base 50mg/1U Sólido Oral x
30 de CIPLA porque desistió del registro sanitario ni CUM
20166850-01 TIVICAY Dolutegravir Base 10mg/1U Sólido Oral x 30,
o CUM 20166851-01 TIVICAY Dolutegravir Base 25mg/1U Sólido Oral
x 30 de GLAXOSMITHKLINE porque no reportaron ventas ni precios a
SISMED, al igual que CUM 20208612-01 TIVICAY Dolutegravir Base
5mg/1U Sólido Oral x 60 y CUM 20208612-02 TIVICAY
Dolutegravir Base 5mg/1U Sólido Oral x 60 muestra médica
también de VIIV HEALTHCARE.
2.6.
2.6. Validación y análisis de ventas Dolutegravir (Tivicay®)
a SISMED de 2022, 2023 y 2024
Las pantallas del
Sistema VMI-CFN
de
seguimiento a los reportes de TIVICAY 50 mg con CUM
20071938-01 (presentación comercial) y CUM
20071938-02 (muestras médicas) desde el trimestre 1° de 2022
hasta el 4° de 2023, permiten ver el detalle de
Transacciones Primarias, reportadas por el laboratorio importador,
Transacciones
Secundarias reportadas por otros actores de la cadena de
distribución y Transacciones Finales reportadas como
Cobros y Recobros al Sistema de Salud. Llaman la atención
especialmente las cantidades en unidades y los valores absurdos
de los datos "multifuente" de transacciones secundarias de los
trimestres 2° de 2023 y 2° de 2022 de la presentación comercial,
así como el precio regulado y las transacciones secundarias y
finales de las muestras médicas "sin valor comercial".
2.6.1.
2.6.1. Validación y análisis datos de Tivicay® CUM 20071938-01 en
Trimestres 1°22 a 4°24
En la ventana superior de la pantalla de validación y
seguimiento de Productos Registrados del
Sistema VMI-CFN
(Gráfico N°7)
pueden verse los datos básicos de cada presentación o CUM (1).
En ese fragmento pueden verse los datos
básicos de cada presentación, Régimen de regulación de
precios que le corresponde, Registro sanitario, Nombre comercial semiparametrizado,
Principio activo parametrizado, Principio activo reportado por
el laboratorio, Forma farmacéutica, Concentración del principio
activo, Presentación comercial, etc.
Gráfico N°7: Pantalla de
seguimiento de reportes de DOLUTEGRAVIR (TIVICAY 50 mg GSK)
CUM 20071938-01 de Trimestres 1° de 2022 a 4° de 2023
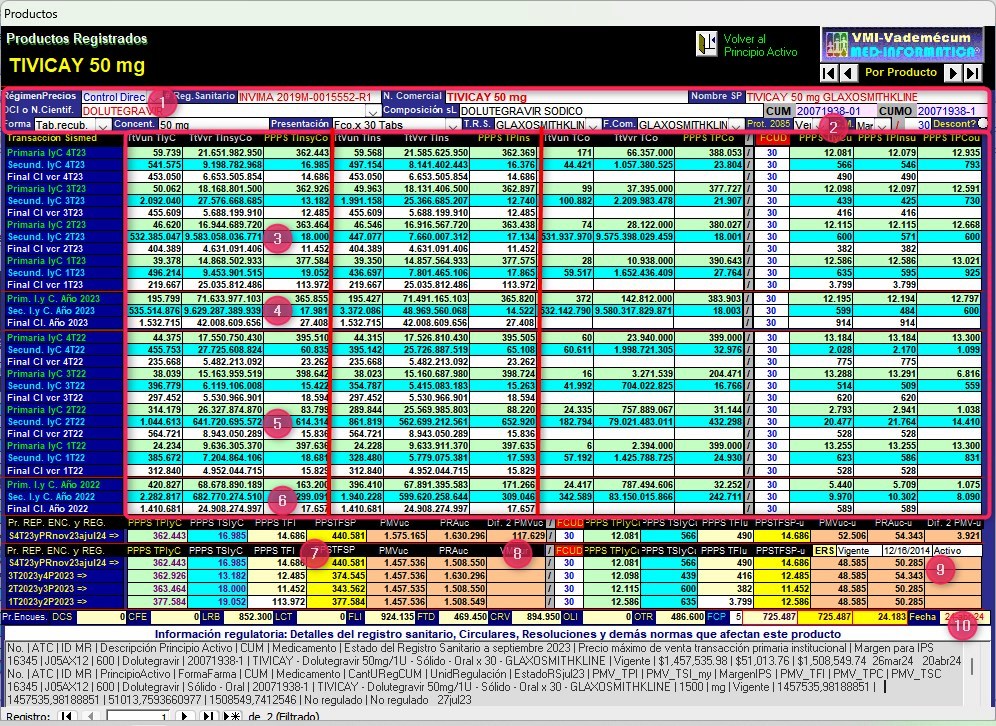
La información económica se muestra en bloques de columnas (ver
marcos de líneas rojas) que en el extremo izquierdo corresponden
a ventas de unidades y sus valores con Precio Promedio de la
Presentación en Sismed (PPPS) de Transacciones Primarias
sumatoria de ventas Institucionales y Comerciales de TIVICAY 50 mg CUM
20071938-01 del trimestre 1° de 2022 al 4° de 2023, reportadas
por GlaxoSmithKline. En las tres columnas siguientes, dichas
ventas pero solo del canal institucional y en las tres
siguientes solo del canal comercial. La
siguiente columna muestra el Factor de Cálculo de Unidosis con los
respectivos Precios Promedio de la Presentación en Sismed
unitario (PPPSu).
En las líneas horizontales de fondo verde
aparecen los datos de Transacciones Primarias, en las de fondo azul
los datos de
Transacciones Secundarias y en las de fondo blanco los datos de Transacciones
finales. Cada grupo de líneas de fondo verde, azul y blanco
corresponde a un trimestre y al final de los cuatro trimestres
se totaliza cada año, en orden cronológico inverso (arriba los
más recientes y abajo los anteriores). En total se muestran ocho
trimestres con sumatoria de dos anuales, en este caso 2022 y
2023.
A continuación aparece la ventana comparativa de
Precios Promedio de la Presentación en Sismed (PPPS) de Transacciones
Primarias (campos de fondo verde), Secundarias (campos de fondo
azul) y Finales (campos con fondo blanco). En la siguiente
columna, con fondo amarillo intenso, aparecen los Precios
Promedio Encuestado en Farmacias de Internet (PPEFI) que
son exclusivos del
Sistema VMI-CFN
y corresponden al promedio de dos o más farmacias de Internet
que publican sus precios, tal como puede verse al final de la
línea con su valor unitario y fecha de actualización.
Seguidamente aparecen dos columna con fondo rojo que
corresponden a Precios Regulados (cuando existen) con el valor
que aparece en la última Circular de la
Comisión Nacional de Precios de Medicamentos (PRCNPM) que
lo fija y el Precio
Regulado Ajustado para Prestadores (PRAP), que incrementa el
precio en un 7 % cuando es inferior a COP un millón o un 3,5 %
cuando es superior a dicho valor. Nota: La tercera columna de
fondo rojo correspondía al Valor Máximo de Recobro (VMR) que en
la actualidad fue abandonado. La siguiente columna muestra
el Factor de Cálculo de Unidosis con los respectivos precios unitarios
de Transacciones Primarias, Secundarias, Finales, PPEFIu,
PRCNPMu, PRAPu,y VMRu con los colores de
fondo correspondientes. Finalmente, el "campo memo" de la parte
inferior muestra anotaciones regulatorias, detalles del Registro sanitario
tomado de la base de datos del INVIMA y notas aclaratorias de
los datos registrados.
|
Este diseño de la pantalla de seguimiento de Productos
Registrados permite ver claramente las siguientes
evidencias analíticas:
✔ TIVICAY 50 mg
CUM 20071938-01 ya tiene una renovación del registro
sanitario como INVIMA 2019M-0015552-R1. Permanece sometido a régimen de Control Directo
 de la regulación de precios vigente , algo de entrada ya
sorprendente,
porque en la parte final se verá que el precio regulado
resulta ser tres veces superior al precio de venta
reportado por el laboratorio).
de la regulación de precios vigente , algo de entrada ya
sorprendente,
porque en la parte final se verá que el precio regulado
resulta ser tres veces superior al precio de venta
reportado por el laboratorio).
✔ La
Protección
de datos de prueba del Decreto 2085 para DOLUTEGRAVIR
estuvo vigente hasta el 5 de enero de 2020 y
actualmente se encuentra VENCIDA  . Nótese que el
vencimiento de la protección de la llamada "patente
extra y express" del Decreto 2085 que facilitó y
adelantó la protección de propiedad intelectual de esta
molécula en Colombia, NO MODIFICÓ la protección de patente internacional que
GlaxoSmithKline sigue reclamando como vigente . Nótese que el
vencimiento de la protección de la llamada "patente
extra y express" del Decreto 2085 que facilitó y
adelantó la protección de propiedad intelectual de esta
molécula en Colombia, NO MODIFICÓ la protección de patente internacional que
GlaxoSmithKline sigue reclamando como vigente
✔ Actualmente
el sistema de reportes a SISMED no cuenta con mecanismos
de validación y analítica de datos  .
Por esta razón, pueden presentarse reportes con valores
absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 532.385.047 unidades por un valor
de COP 9.583.058.036.771. En este caso los datos
absurdos dañan los datos de Transacciones
secundarias comerciales de los trimestres 2° de 2023 y
2022 afectando los totales de los trimestres y sus
acumulados anuales. .
Por esta razón, pueden presentarse reportes con valores
absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 532.385.047 unidades por un valor
de COP 9.583.058.036.771. En este caso los datos
absurdos dañan los datos de Transacciones
secundarias comerciales de los trimestres 2° de 2023 y
2022 afectando los totales de los trimestres y sus
acumulados anuales.
✔
Estos errores afectan más a los reportes "multifuente"    de innumerables reportes de Transacciones Secundarias y
Finales que son de
múltiples actores del sistema que negocian, cobran o
recobran medicamentos. Por esta razón el análisis de las ventas reportadas a SISMED
de este estudio se basan en datos de Transacciones
primarias del Laboratorio productor o importador que
son "monofuente" (de un solo reportante) que
pueden tener hasta mayor valor legal en casos de litigio.
de innumerables reportes de Transacciones Secundarias y
Finales que son de
múltiples actores del sistema que negocian, cobran o
recobran medicamentos. Por esta razón el análisis de las ventas reportadas a SISMED
de este estudio se basan en datos de Transacciones
primarias del Laboratorio productor o importador que
son "monofuente" (de un solo reportante) que
pueden tener hasta mayor valor legal en casos de litigio.
✔ Al comparar
los Precios PPPS de Transacciones Primarias, Secundarias
y Finales puede verse que los precios del Laboratorio
son de cajas por 30 tabletas
 mientras los de
Transacciones Secundarias y Finales son precios por tableta.
Los precios por tableta de Transacciones Secundarias
tienen muchas inconsistencias y poca utilidad, pero las
Finales (cobros y recobros pagados por el sistema)
ameritan la conversión de precios Unidosis a precios de
la presentación o CUM que aquí aparecen en amarillo. mientras los de
Transacciones Secundarias y Finales son precios por tableta.
Los precios por tableta de Transacciones Secundarias
tienen muchas inconsistencias y poca utilidad, pero las
Finales (cobros y recobros pagados por el sistema)
ameritan la conversión de precios Unidosis a precios de
la presentación o CUM que aquí aparecen en amarillo.
✔
Como ya se dijo, los Valores Máximos de Recobro (VMR) y sus unitarios (VMRu)
y sus unitarios (VMRu) fueron abandonados. Pero, esta zona de Comparación de
Precios
fueron abandonados. Pero, esta zona de Comparación de
Precios Reportados, Encuestados y Regulados, con su fecha
de actualización, es de mucha utilidad: Como
puede verse, el Precio Promedio de la Presentación en
Sismed de Transacciones Primarias del canal
Institucional más el canal Comercial (PPPS_TPIyC)
del 4° trimestre de 2023 fue COP 362.443 con
precio unitario (PPPS_TPIyCu) de COP 12.081.
Este precio unitario en el caso de Transacciones
Secundarias (PPPS_TSIyCu) fue de COP 16.985
y el de Transacciones Finales (PPPS_TFIu) -lo
pagado por el sistema de salud- fue de COP 14.686. El Precio
Público Promedio Encuestado en Internet (PPPEI)
fue de COP 440.581 con un precio unitario de COP
14.686. El Precio Máximo de Venta de la
Presentación (PMV) fijado por la última Circular
de 2023 de la CNPM fue de COP 1.457.536 con un
unitario (PMVu) de COP 48.585 y el Precio
Ajustado para Prestadores (PAP) fue de COP
1.508.550 con un precio unitario (PAPu) de
COP 50.285. Por
lo tanto, los precios regulados de TIVICAY 50 mg de
GlaxoSmithKline más que triplican los precios reportados
por el laboratorio y más que duplican los precios
encuestados en Farmacias de Internet.
Reportados, Encuestados y Regulados, con su fecha
de actualización, es de mucha utilidad: Como
puede verse, el Precio Promedio de la Presentación en
Sismed de Transacciones Primarias del canal
Institucional más el canal Comercial (PPPS_TPIyC)
del 4° trimestre de 2023 fue COP 362.443 con
precio unitario (PPPS_TPIyCu) de COP 12.081.
Este precio unitario en el caso de Transacciones
Secundarias (PPPS_TSIyCu) fue de COP 16.985
y el de Transacciones Finales (PPPS_TFIu) -lo
pagado por el sistema de salud- fue de COP 14.686. El Precio
Público Promedio Encuestado en Internet (PPPEI)
fue de COP 440.581 con un precio unitario de COP
14.686. El Precio Máximo de Venta de la
Presentación (PMV) fijado por la última Circular
de 2023 de la CNPM fue de COP 1.457.536 con un
unitario (PMVu) de COP 48.585 y el Precio
Ajustado para Prestadores (PAP) fue de COP
1.508.550 con un precio unitario (PAPu) de
COP 50.285. Por
lo tanto, los precios regulados de TIVICAY 50 mg de
GlaxoSmithKline más que triplican los precios reportados
por el laboratorio y más que duplican los precios
encuestados en Farmacias de Internet.
|
Gráfico N°8: Pantalla de
seguimiento de reportes de DOLUTEGRAVIR (TIVICAY 50 mg GSK)
CUM 20071938-01 de Trimestres 1° de 2023 a 4° de 2024
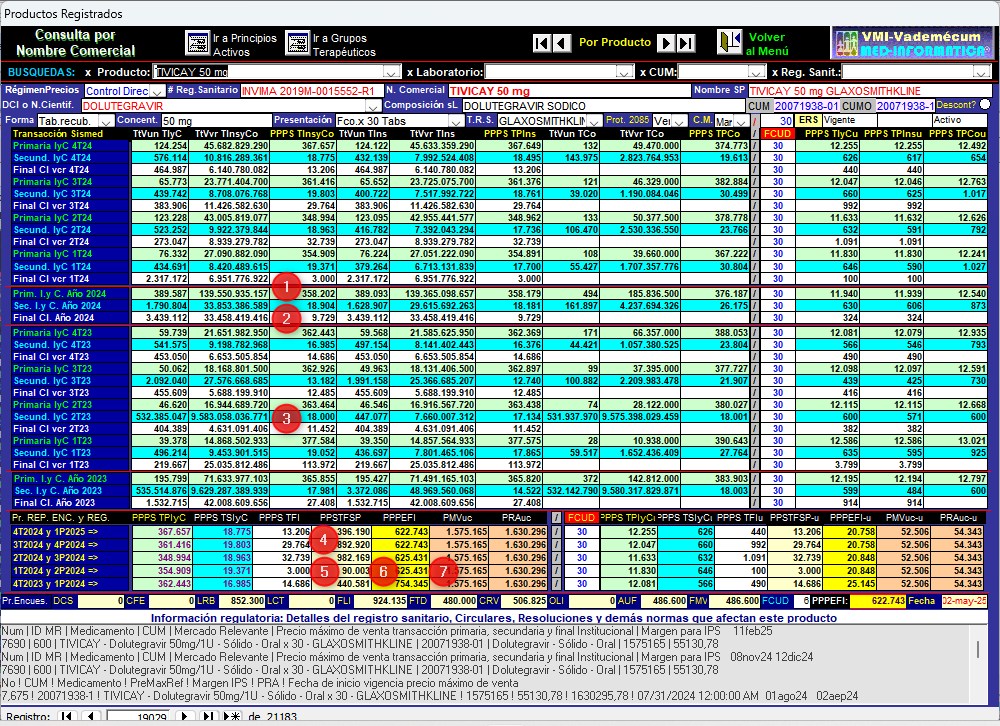
✔ El
año 2024 GlaxoSmithKline reportó Transacciones Primarias
Institucionales y Comerciales de venta de TIVICAY 50 mg
CUM 20071938-01  por 389.587 unidades y COP 139.550.935.157 con un
Precio Promedio de la Presentación en Sismed (PPPS_TPIyC)
de COP 358.202. Es decir, prácticamente duplicó las
ventas de 2023 tanto en unidades como en valores.
por 389.587 unidades y COP 139.550.935.157 con un
Precio Promedio de la Presentación en Sismed (PPPS_TPIyC)
de COP 358.202. Es decir, prácticamente duplicó las
ventas de 2023 tanto en unidades como en valores.
✔ Las
diferencias extraordinarias en el número de unidades vendidas
entre las Transacciones Primarias y las Transacciones
Secundarias o las Finales  se deben a que el Laboratorio siguió reportando las
presentaciones vendidas, mientras los demás actores persistieron
en el error de reportar UniDosis o tabletas. Y la gran
diferencia entre el valor reportado por el Laboratorio
corresponde a todas sus ventas en el período, mientras las
Transacciones Secundarias y Finales reflejan solo datos del
régimen contributivo mientras los datos del régimen subsidiado y
los regímenes especiales prácticamente permanecen desconocidos.
se deben a que el Laboratorio siguió reportando las
presentaciones vendidas, mientras los demás actores persistieron
en el error de reportar UniDosis o tabletas. Y la gran
diferencia entre el valor reportado por el Laboratorio
corresponde a todas sus ventas en el período, mientras las
Transacciones Secundarias y Finales reflejan solo datos del
régimen contributivo mientras los datos del régimen subsidiado y
los regímenes especiales prácticamente permanecen desconocidos.
✔
El sistema de reportes a SISMED sigue sin contar con mecanismos
de validación y analítica de datos  .
Por esta razón, persisten los valores absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 532.385.047 unidades por un valor
de COP 9.583.058.036.771. Los datos absurdos
de Transacciones
secundarias del 2° trimestre de 2023 dañaron los datos
de
acumulados anuales. .
Por esta razón, persisten los valores absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 532.385.047 unidades por un valor
de COP 9.583.058.036.771. Los datos absurdos
de Transacciones
secundarias del 2° trimestre de 2023 dañaron los datos
de
acumulados anuales.
✔
Estos errores siguen afectando básicamente a los reportes "multifuente"   de las Transacciones Secundarias y Finales donde
múltiples actores del sistema siguen reportando valores
errados y absurdos. Por esta razón los análisis de datos de este
estudio deben basarse en datos de Transacciones
primarias y en casos especiales como los precios de
Transacciones Finales convertirse de UniDosis a valor por
Presentación o CUM (campos de color amarillo tenue). Solo así
pueden compararse los precios de venta del Laboratorio con los
precios pagados por el sistema.
de las Transacciones Secundarias y Finales donde
múltiples actores del sistema siguen reportando valores
errados y absurdos. Por esta razón los análisis de datos de este
estudio deben basarse en datos de Transacciones
primarias y en casos especiales como los precios de
Transacciones Finales convertirse de UniDosis a valor por
Presentación o CUM (campos de color amarillo tenue). Solo así
pueden compararse los precios de venta del Laboratorio con los
precios pagados por el sistema.
✔
Como ya se dijo, los Valores Máximos de Recobro (VMR)
y sus unitarios (VMRu) se abandonaron. Pero, la Comparación de
Precios  Reportados, Encuestados y Regulados son de mucha
utilidad: Nótese que el Precio Promedio de la Presentación
en Sismed de Transacciones Primarias del canal Institucional más
el canal Comercial (PPPS_TPIyC) del 4° trimestre de 2023
fue COP 362.443 y en 2024 pasó a COP 367.657, con
precio unitario (PPPS_TPIyCu) de COP 12.081. que
pasó a COP 12.255. Este precio unitario en el caso de
Transacciones Secundarias (PPPS_TSIyCu) que en 2023 fue
COP 16.985 en 2024 pasó a COP 18.775 y el de Transacciones
Finales (PPPS_TFIu) que en 2023 fue de COP 14.686,
en 2024 pasó a 13.206, aunque en trimestres
inmediatamente anteriores fue 29.764 y 32.739. El Precio
Público Promedio Encuestado en Internet (PPPEI)
que en 2023 fue de COP 440.581 con un precio unitario de
COP 14.686, en 2024 fue COP 622.743 con precio
unitario de COP 20.758. El Precio Máximo de Venta de la
Presentación (PMV) fijado por la última Circular de 2023
de la CNPM en 2023 fue de COP 1.457.536 con un unitario (PMVu)
de COP 48.585, en 2024 pasó a COP 1.575.165 con
precio unitario de COP 52.506. Y el Precio Ajustado para
Prestadores (PAP) que en 2023 fue de COP 1.508.550
con un precio unitario (PAPu) de COP 50.285, en
2024 pasó a COP 1.630.296 con un precio unitario de COP
54.343. Por
lo tanto, en 2024 los precios regulados de TIVICAY 50 mg de
GlaxoSmithKline no se rectificaron, antes aumentaron y siguen más que triplicando los precios
reportados por el laboratorio y más que duplican los precios
encuestados en Farmacias de Internet.
Reportados, Encuestados y Regulados son de mucha
utilidad: Nótese que el Precio Promedio de la Presentación
en Sismed de Transacciones Primarias del canal Institucional más
el canal Comercial (PPPS_TPIyC) del 4° trimestre de 2023
fue COP 362.443 y en 2024 pasó a COP 367.657, con
precio unitario (PPPS_TPIyCu) de COP 12.081. que
pasó a COP 12.255. Este precio unitario en el caso de
Transacciones Secundarias (PPPS_TSIyCu) que en 2023 fue
COP 16.985 en 2024 pasó a COP 18.775 y el de Transacciones
Finales (PPPS_TFIu) que en 2023 fue de COP 14.686,
en 2024 pasó a 13.206, aunque en trimestres
inmediatamente anteriores fue 29.764 y 32.739. El Precio
Público Promedio Encuestado en Internet (PPPEI)
que en 2023 fue de COP 440.581 con un precio unitario de
COP 14.686, en 2024 fue COP 622.743 con precio
unitario de COP 20.758. El Precio Máximo de Venta de la
Presentación (PMV) fijado por la última Circular de 2023
de la CNPM en 2023 fue de COP 1.457.536 con un unitario (PMVu)
de COP 48.585, en 2024 pasó a COP 1.575.165 con
precio unitario de COP 52.506. Y el Precio Ajustado para
Prestadores (PAP) que en 2023 fue de COP 1.508.550
con un precio unitario (PAPu) de COP 50.285, en
2024 pasó a COP 1.630.296 con un precio unitario de COP
54.343. Por
lo tanto, en 2024 los precios regulados de TIVICAY 50 mg de
GlaxoSmithKline no se rectificaron, antes aumentaron y siguen más que triplicando los precios
reportados por el laboratorio y más que duplican los precios
encuestados en Farmacias de Internet.
2.6.2.
2.6.2. Validación y análisis datos de Tivicay® CUM 20071938-02 en
Trimestres 1°22 a 4°24
Las ventas reportadas por TIVICAY 50 mg CUM
20071938-02 de "muestra médica sin valor comercial" entre el trimestre
1° de 2022
y trimestre 4° de 2023 son ilegales pero muestran Transacciones
Secundarias (de
múltiples actores de la cadena de distribución) por $343.784.997
el año 2023, junto con otras inconsistencias que pueden verse en
el siguiente gráfico:
Gráfico N°9: Pantalla de
seguimiento de reportes de DOLUTEGRAVIR (TIVICAY 50 mg GSK)
CUM 20071938-02 de Trimestres 1° de 2022 a 4° de 2023
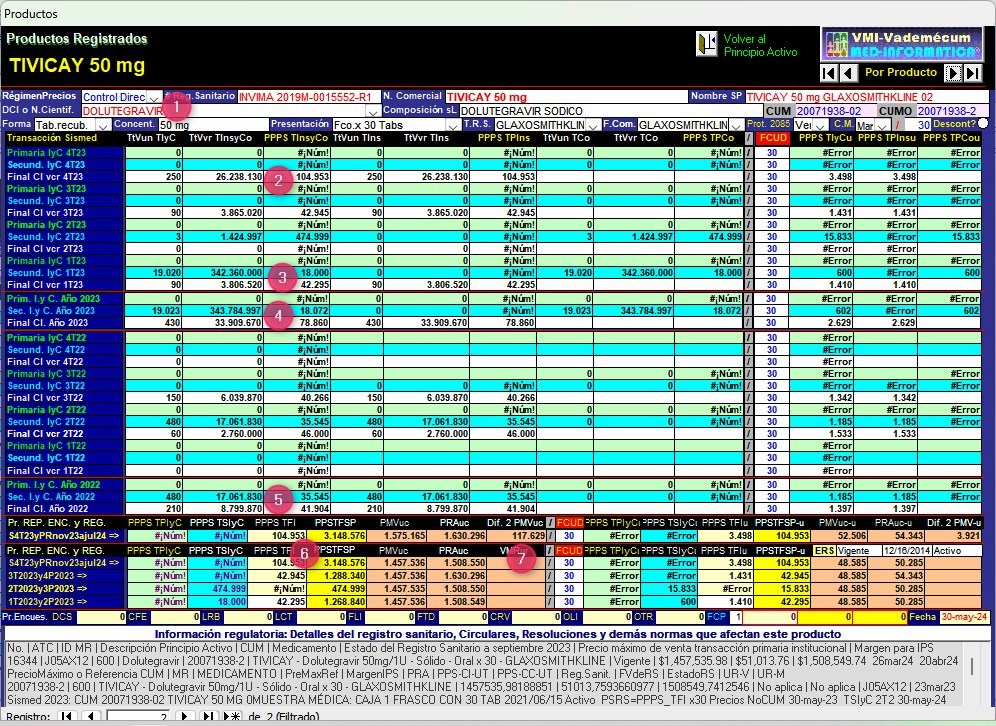
Siete
inconsistencias en los reportes de TIVICAY 50 mg CUM
20071938-02 MUESTRA MEDICA de trimestres 1° de 2022 a 4°
de 2023
 TIVICAY
de 50 mg, con
CUM 20071938-02 y registro "Muestra Médica sin valor comercial"
aparece sometido a régimen de Control
Directo. Algo absurdo porque fija precio regulado
para algo no vendible. Constituye una "inducción
perversa" a error en los reportes, que deteriora el sistema de regulación de precios
vigente en el país. TIVICAY
de 50 mg, con
CUM 20071938-02 y registro "Muestra Médica sin valor comercial"
aparece sometido a régimen de Control
Directo. Algo absurdo porque fija precio regulado
para algo no vendible. Constituye una "inducción
perversa" a error en los reportes, que deteriora el sistema de regulación de precios
vigente en el país.
 En el 4° trimestre de 2023 aparecen reportes de Transacciones
finales de
230 unidades por las cuales el sistema habría pagado COP 26.238.130.
Y en el 1°
En el 4° trimestre de 2023 aparecen reportes de Transacciones
finales de
230 unidades por las cuales el sistema habría pagado COP 26.238.130.
Y en el 1° y también se reportaron 19.020
unidades de muestras médicas sin valor comercial por COP
342.360.000, algo que el Ministerio de Salud y su
OTIC debieron validar, analizar y
corregir,
y también se reportaron 19.020
unidades de muestras médicas sin valor comercial por COP
342.360.000, algo que el Ministerio de Salud y su
OTIC debieron validar, analizar y
corregir,
 Estas
inconsistencias reproducen lo que ya sucedía con los reportes de
2022. Según datos
acumulados de Transacciones Finales, en 2022 Estas
inconsistencias reproducen lo que ya sucedía con los reportes de
2022. Según datos
acumulados de Transacciones Finales, en 2022 se
cobraron al sistema 210 tabletas
por COP 8.799.870 a 41.904 c/u. Y como Transacciones
secundarias
se vendieron 480 tabletas
por COP 17.061.830 s COP 35.545 c/u. se
cobraron al sistema 210 tabletas
por COP 8.799.870 a 41.904 c/u. Y como Transacciones
secundarias
se vendieron 480 tabletas
por COP 17.061.830 s COP 35.545 c/u.
 El precio de COP 104.953 como aparece como precio cobrado
al sistema de salud en el último trimestre de 2022
El precio de COP 104.953 como aparece como precio cobrado
al sistema de salud en el último trimestre de 2022 resulta absurdo porque el precio reportado por el CUM 20071938-01 TIVICAY 50 mg
x 30 Tabs, fue COP 358.202 y -si el valor fuese por tableta- el
precio de la presentación sería 3.148.590.
resulta absurdo porque el precio reportado por el CUM 20071938-01 TIVICAY 50 mg
x 30 Tabs, fue COP 358.202 y -si el valor fuese por tableta- el
precio de la presentación sería 3.148.590.
 El Valor máximo de Recobro VMR ya abandonado, también era
absurdo por las mismas razones: Porque el precio reportado por
el CUM 20071938-01 TIVICAY 50 mg x 30 Tabs, fue COP 358.202 y
-si el valor fuese por tableta- el precio de la presentación
sería 3.148.590.
El Valor máximo de Recobro VMR ya abandonado, también era
absurdo por las mismas razones: Porque el precio reportado por
el CUM 20071938-01 TIVICAY 50 mg x 30 Tabs, fue COP 358.202 y
-si el valor fuese por tableta- el precio de la presentación
sería 3.148.590.
El año 2024 TIVICAY
de 50 mg, con
CUM 20071938-02 y registro "Muestra Médica sin valor comercial"
siguió reportando ventas y se mantuvo con precio
regulado pese a su condición de producto "sin valor comercial". Como
Transacciones Secundarias por canal institucional se reportaron
180 unidades por COP 2.590.920 y como Transacciones Finales
(cobros o recobros) se reportaron 870 unidades por COP
36.406.560. La falta
de validación y analítica de los datos reportados s SISMED,
sigue sin corregirse y deteriora cada vez más el sistema de información.
La implementación de la Licencia
Obligatoria obligaría a la revisión de todos estos
valores, algo que -insistimos- constituye un paso en la dirección correcta para
resolver estructuralmente estas inconsistencias del sistema de
Información.
2.6.3.
2.6.3. Validación y
análisis Dolutegravir+Abacavir+Lamivudina(Triumeq®)
de
T1°22 aT4°24
Los reportes de ventas a SISMED de la
combinación Lamivudina 300 mg + Abacavir 600 mg y
Dolutegravir 50 mg (TRIUMEQ®
de GlaxoSmithKline
CUM 20081132-01) de los trimestres 1° de 2022 al 4° de 2023
puede verse en el siguiente gráfico:
Gráfico N°10: Pantalla de
seguimiento de reportes a SISMED de TRIUMEQ de
GlaxoSmithKline CUM 20081132-01 de Trimestres 1° de
2022 a 4° de 2023
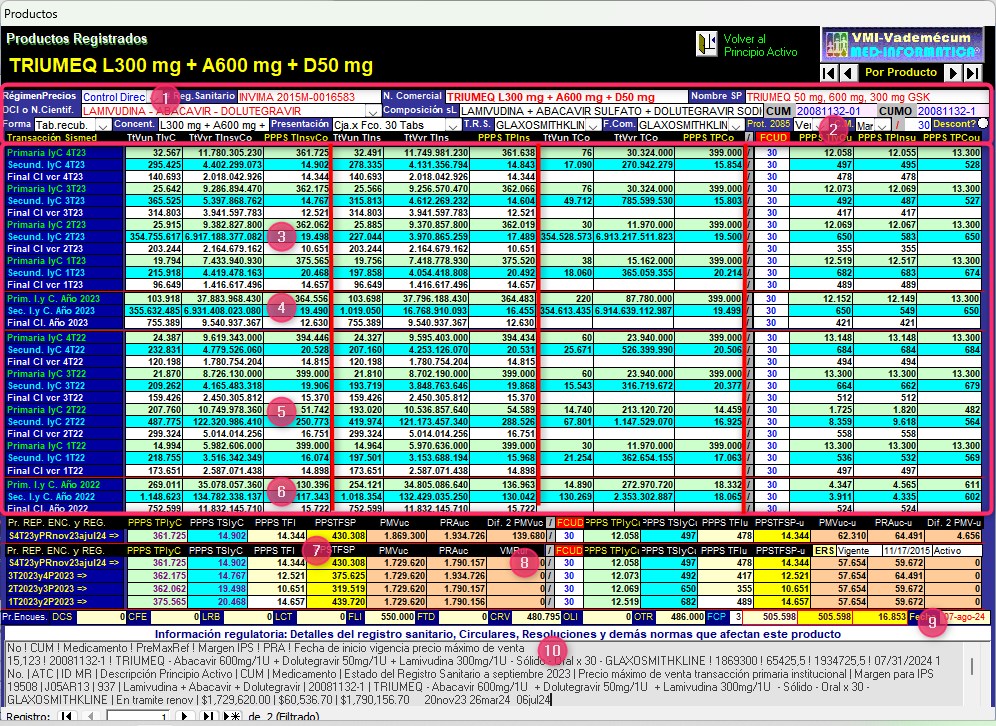
Esta pantalla de seguimiento de Productos
Registrados permite ver las siguientes evidencias
analíticas:
✔ En
2023
TRIUMEQ de
GlaxoSmithKline CUM
20081132-01 permanece sometido a régimen de Control Directo
 de la regulación de precios vigente, algo
sorprendente,
porque en la parte final de esta pantalla se verá que el precio regulado
resulta ser casi cuatro veces superior al precio de venta
reportado por el laboratorio).
de la regulación de precios vigente, algo
sorprendente,
porque en la parte final de esta pantalla se verá que el precio regulado
resulta ser casi cuatro veces superior al precio de venta
reportado por el laboratorio).
✔ La
Protección
de datos de prueba del Decreto 2085 para DOLUTEGRAVIR
estuvo vigente hasta el 5 de enero de 2020 y
actualmente se encuentra VENCIDA  . Nótese la protección de la llamada "patente
extra y express" del Decreto 2085 que facilita y
adelanta la protección de propiedad intelectual de
medicamentos en Colombia, En la práctica NO altera la protección de patente internacional que GlaxoSmithKline
se sigue reclamando como vigente . Nótese la protección de la llamada "patente
extra y express" del Decreto 2085 que facilita y
adelanta la protección de propiedad intelectual de
medicamentos en Colombia, En la práctica NO altera la protección de patente internacional que GlaxoSmithKline
se sigue reclamando como vigente
✔ Actualmente
el sistema de reportes a SISMED no cuenta con mecanismos
de validación y analítica de datos  .
Por esta razón, pueden presentarse reportes con valores
absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 354.755.617 unidades por un valor
de COP 6.917.188.377.082. En este caso los datos
absurdos dañan los datos de Transacciones
secundarias comerciales de los trimestres 2° de 2023 y
3° de 2022, afectando los
acumulados anuales de ambos períodos. .
Por esta razón, pueden presentarse reportes con valores
absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 354.755.617 unidades por un valor
de COP 6.917.188.377.082. En este caso los datos
absurdos dañan los datos de Transacciones
secundarias comerciales de los trimestres 2° de 2023 y
3° de 2022, afectando los
acumulados anuales de ambos períodos.
✔
Estos errores afectan más a los reportes "multifuente"    de innumerables reportes de Transacciones Secundarias y
Finales que son de
múltiples actores del sistema que negocian, cobran o
recobran medicamentos. Por esta razón el análisis de las ventas reportadas a SISMED
de este estudio se basan en datos de Transacciones
primarias del Laboratorio productor o importador que
son "monofuente" (de un solo reportante) que
pueden tener hasta mayor valor legal en casos de litigio.
de innumerables reportes de Transacciones Secundarias y
Finales que son de
múltiples actores del sistema que negocian, cobran o
recobran medicamentos. Por esta razón el análisis de las ventas reportadas a SISMED
de este estudio se basan en datos de Transacciones
primarias del Laboratorio productor o importador que
son "monofuente" (de un solo reportante) que
pueden tener hasta mayor valor legal en casos de litigio.
✔ Al comparar
los Precios PPPS de Transacciones Primarias, Secundarias
y Finales puede verse que los precios del Laboratorio
son de cajas por 30 tabletas
 mientras los de
Transacciones Secundarias y Finales son precios por tableta.
Los precios por tableta de Transacciones Secundarias
tienen muchas inconsistencias y poca utilidad, pero las
Finales (cobros y recobros pagados por el sistema)
ameritan la conversión de precios Unidosis a precios de
la presentación o CUM que aquí aparecen en amarillo. mientras los de
Transacciones Secundarias y Finales son precios por tableta.
Los precios por tableta de Transacciones Secundarias
tienen muchas inconsistencias y poca utilidad, pero las
Finales (cobros y recobros pagados por el sistema)
ameritan la conversión de precios Unidosis a precios de
la presentación o CUM que aquí aparecen en amarillo.
✔
Como ya se dijo, los Valores Máximos de Recobro (VMR) y sus unitarios (VMRu)
y sus unitarios (VMRu) fueron abandonados. Pero, esta zona de Comparación de
Precios
fueron abandonados. Pero, esta zona de Comparación de
Precios Reportados, Encuestados y Regulados, con su fecha
de actualización, es de mucha utilidad: Como
puede verse, el Precio Promedio de la Presentación en
Sismed de Transacciones Primarias del canal
Institucional más el canal Comercial (PPPS_TPIyC)
del 4° trimestre de 2023 fue COP 361.725 con
precio unitario (PPPS_TPIyCu) de COP 12.058.
Este precio unitario en el caso de Transacciones
Secundarias (PPPS_TSIyCu) fue de COP 14.902
y el de Transacciones Finales (PPPS_TFIu) -lo
pagado por el sistema de salud- fue de COP 14.344. El Precio
Público Promedio Encuestado en Internet (PPPEI)
fue de COP 505.598 con un precio unitario de COP
16.853. El Precio Máximo de Venta de la
Presentación (PMV) fijado por la última Circular
de 2023 de la CNPM fue de COP 1.869.300 con un
unitario (PMVu) de COP 62.310 y el Precio
Ajustado para Prestadores (PAP) fue de COP
1.934.726 con un precio unitario (PAPu) de
COP 64.491. Por
lo tanto, los precios regulados de
TRIUMEQ de
GlaxoSmithKline más que
cuadruplican los precios reportados
por el laboratorio y más que triplican los precios
encuestados en Farmacias de Internet. La
implementación de la Licencia
Obligatoria obligará a la revisión de todos estos
valores, razón por la cual constituye un paso en la dirección correcta para
resolver estructuralmente estas inconsistencias.
Reportados, Encuestados y Regulados, con su fecha
de actualización, es de mucha utilidad: Como
puede verse, el Precio Promedio de la Presentación en
Sismed de Transacciones Primarias del canal
Institucional más el canal Comercial (PPPS_TPIyC)
del 4° trimestre de 2023 fue COP 361.725 con
precio unitario (PPPS_TPIyCu) de COP 12.058.
Este precio unitario en el caso de Transacciones
Secundarias (PPPS_TSIyCu) fue de COP 14.902
y el de Transacciones Finales (PPPS_TFIu) -lo
pagado por el sistema de salud- fue de COP 14.344. El Precio
Público Promedio Encuestado en Internet (PPPEI)
fue de COP 505.598 con un precio unitario de COP
16.853. El Precio Máximo de Venta de la
Presentación (PMV) fijado por la última Circular
de 2023 de la CNPM fue de COP 1.869.300 con un
unitario (PMVu) de COP 62.310 y el Precio
Ajustado para Prestadores (PAP) fue de COP
1.934.726 con un precio unitario (PAPu) de
COP 64.491. Por
lo tanto, los precios regulados de
TRIUMEQ de
GlaxoSmithKline más que
cuadruplican los precios reportados
por el laboratorio y más que triplican los precios
encuestados en Farmacias de Internet. La
implementación de la Licencia
Obligatoria obligará a la revisión de todos estos
valores, razón por la cual constituye un paso en la dirección correcta para
resolver estructuralmente estas inconsistencias.
Gráfico N°11: Pantalla de
seguimiento de TRIUMEQ de
GlaxoSmithKline CUM 20081132-01 de Trimestres 1° de
2023 a 4° de 2024
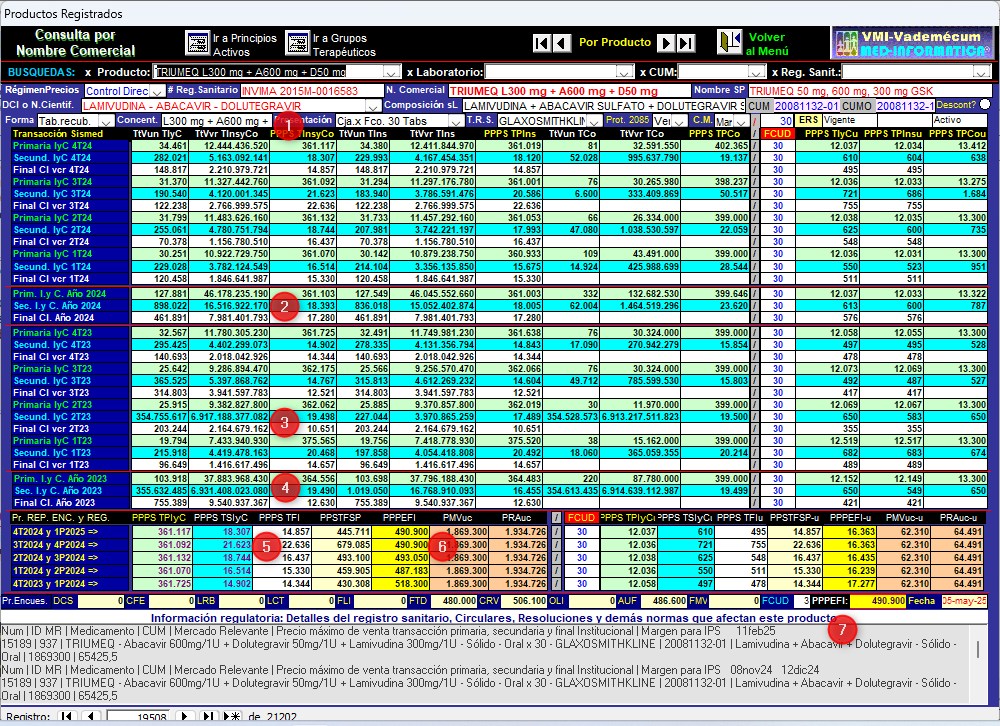
Esta pantalla de seguimiento de Productos
Registrados del Sistema VMI-CFN permite ver las
siguientes evidencias analíticas:
✔ En
2024
TRIUMEQ de
GlaxoSmithKline CUM
20081132-01 reportó
prácticamente los mismos datos básicos de 2023 .
Permanece sometido a régimen de Control Directo
de la regulación de precios vigente, algo sorprendente,
porque en la parte inferior de esta pantalla puede verse que el precio regulado
es casi cuatro veces superior al precio de venta
reportado por el laboratorio). .
Permanece sometido a régimen de Control Directo
de la regulación de precios vigente, algo sorprendente,
porque en la parte inferior de esta pantalla puede verse que el precio regulado
es casi cuatro veces superior al precio de venta
reportado por el laboratorio).
✔ En 2024 GlaxoSmithKline reportó Transacciones Primarias
Institucionales y Comerciales de venta de Triumeq CUM
20081132-01 por 127.881 unidades y COP 46.178.235.190 con un
Precio Promedio de la Presentación en Sismed (PPPS_TPIyC)
de COP 361.103. Es decir, prácticamente todo por canal
institucional.
por 127.881 unidades y COP 46.178.235.190 con un
Precio Promedio de la Presentación en Sismed (PPPS_TPIyC)
de COP 361.103. Es decir, prácticamente todo por canal
institucional.
✔ Las
diferencias extraordinarias en el número de unidades vendidas
entre las Transacciones Primarias y las Transacciones
Secundarias o las Finales
se deben a que el Laboratorio siguió reportando las
presentaciones vendidas, mientras los demás actores persistieron
en el error de reportar UniDosis o tabletas. Y la gran
diferencia entre el valor reportado por el Laboratorio
corresponde a todas sus ventas en el período, mientras las
Transacciones Secundarias y Finales reflejan solo datos del
régimen contributivo mientras los datos del régimen subsidiado y
los regímenes especiales prácticamente permanecen desconocidos.
✔
El sistema de reportes a SISMED sigue sin contar con mecanismos
de validación y analítica de datos .
Por esta razón, persisten los valores absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 354.755.617 unidades por un valor
de COP 6.917.188.377.082. Los datos absurdos
dañaron los datos de Transacciones
secundarias del 2° trimestre de 2023 y
afectaron los
acumulados anuales. .
Por esta razón, persisten los valores absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 354.755.617 unidades por un valor
de COP 6.917.188.377.082. Los datos absurdos
dañaron los datos de Transacciones
secundarias del 2° trimestre de 2023 y
afectaron los
acumulados anuales.
✔
Estos errores siguen afectando básicamente a los reportes "multifuente" de las Transacciones Secundarias y Finales donde
múltiples actores del sistema siguen reportando valores
errados y absurdos. Por esta razón los análisis de datos de este
estudio deben basarse en datos de Transacciones
primarias y en casos especiales como los precios de
Transacciones Finales convertirse de UniDosis a valor por
Presentación o CUM (campos de color amarillo tenue). Solo así
pueden compararse los precios de venta del Laboratorio con los
precios pagados por el sistema.
de las Transacciones Secundarias y Finales donde
múltiples actores del sistema siguen reportando valores
errados y absurdos. Por esta razón los análisis de datos de este
estudio deben basarse en datos de Transacciones
primarias y en casos especiales como los precios de
Transacciones Finales convertirse de UniDosis a valor por
Presentación o CUM (campos de color amarillo tenue). Solo así
pueden compararse los precios de venta del Laboratorio con los
precios pagados por el sistema.
✔
La Comparación de
Precios  Reportados, Encuestados y Regulados es de mucha
utilidad: Nótese que el Precio Promedio de la Presentación
en Sismed de Transacciones Primarias del canal Institucional más
el canal Comercial (PPPS_TPIyC) en 2024 pasó a COP
361.117, con
precio unitario (PPPS_TPIyCu) de COP 12.037. Este precio unitario en el caso de
Transacciones Secundarias (PPPS_TSIyCu) en 2024 pasó a COP
18.307 y el de Transacciones
Finales (PPPS_TFIu),
en 2024 pasó a COP 14.857, aunque el trimestre
inmediatamente anterior fue COP0 22.636. El Precio
Público Promedio Encuestado en Internet (PPPEI)
en 2024 fue COP 490.900 con precio
unitario de COP 16.363. El Precio Máximo de Venta de la
Presentación (PMV) fijado por la última Circular de 2024
de la CNPM pasó a COP 1.869.300 con
precio unitario de COP 62.310. Y el Precio Ajustado para
Prestadores (PAP) pasó a COP 1.934.726 con un precio unitario de COP
64.491. Por
lo tanto, en 2024 los precios regulados de Triumeq CUM
20081132-01 de
GlaxoSmithKline en lugar de corregirse siguieron
aumentando, más que triplicando los precios
reportados por el laboratorio y más que duplicando los precios
encuestados en Farmacias de Internet.
Reportados, Encuestados y Regulados es de mucha
utilidad: Nótese que el Precio Promedio de la Presentación
en Sismed de Transacciones Primarias del canal Institucional más
el canal Comercial (PPPS_TPIyC) en 2024 pasó a COP
361.117, con
precio unitario (PPPS_TPIyCu) de COP 12.037. Este precio unitario en el caso de
Transacciones Secundarias (PPPS_TSIyCu) en 2024 pasó a COP
18.307 y el de Transacciones
Finales (PPPS_TFIu),
en 2024 pasó a COP 14.857, aunque el trimestre
inmediatamente anterior fue COP0 22.636. El Precio
Público Promedio Encuestado en Internet (PPPEI)
en 2024 fue COP 490.900 con precio
unitario de COP 16.363. El Precio Máximo de Venta de la
Presentación (PMV) fijado por la última Circular de 2024
de la CNPM pasó a COP 1.869.300 con
precio unitario de COP 62.310. Y el Precio Ajustado para
Prestadores (PAP) pasó a COP 1.934.726 con un precio unitario de COP
64.491. Por
lo tanto, en 2024 los precios regulados de Triumeq CUM
20081132-01 de
GlaxoSmithKline en lugar de corregirse siguieron
aumentando, más que triplicando los precios
reportados por el laboratorio y más que duplicando los precios
encuestados en Farmacias de Internet.
✔
La anterior inconsistencia puede confirmarse con la
transcripción de las respectivas líneas de la tabla de precios regulados, en
el campo memo de información regulatoria.
de las respectivas líneas de la tabla de precios regulados, en
el campo memo de información regulatoria.
2.6.4.
2.6.4. Validación y
análisis de Dolutegravir+Lamivudina (Dovato®)
de 1T2022
a 4T2024
El Impacto de la
combinación Lamivudina + DOLUTEGRAVIR (DOVATO GSK CUM
20171830-01) en los reportes a SISMED del trimestre 1° de 2022 al 4° de 2023
puede verse en el siguiente gráfico:
Gráfico N°12: Pantalla de
seguimiento de DOVATO de
GlaxoSmithKline CUM 20171830-01 de Trimestres 1° de 2022 a 4°
de 2023
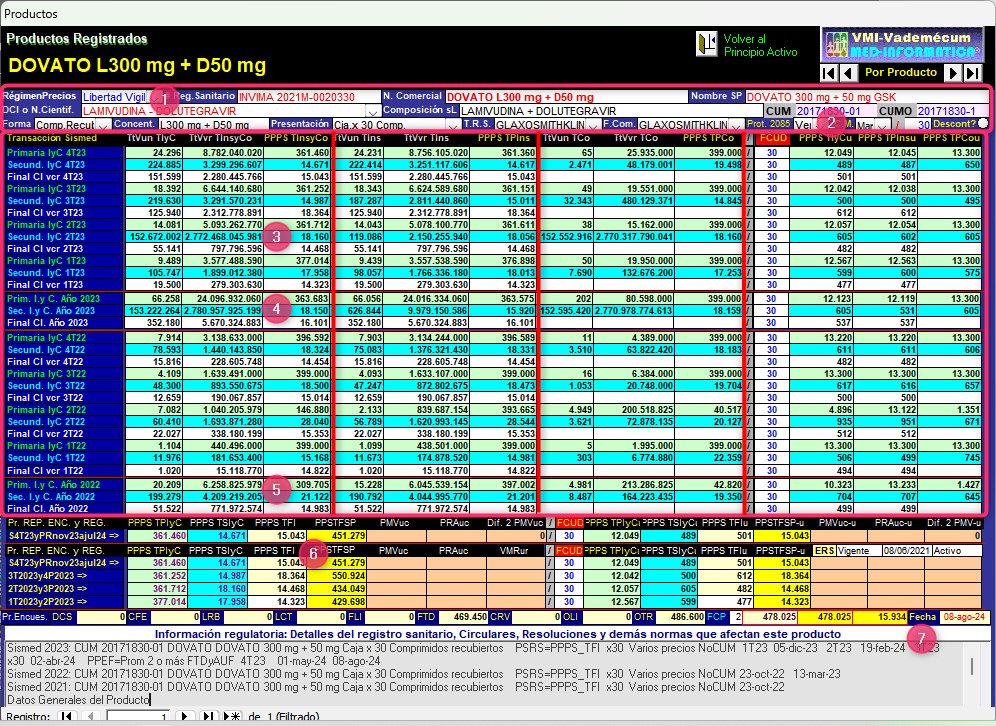
✔ En
2023
DOVATO de
GlaxoSmithKline CUM
20171830-01
no se encuentra sometido a régimen de Control Directo
 de la regulación de precios vigente, algo que se
confirma en la parte final de esta pantalla donde los campos de
precios regulados aparecen sin datos.
de la regulación de precios vigente, algo que se
confirma en la parte final de esta pantalla donde los campos de
precios regulados aparecen sin datos.
✔ Actualmente
el sistema de reportes a SISMED no cuenta con mecanismos
de validación y analítica de datos   .
Por esta razón, pueden presentarse reportes con valores
absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 152.672.002 unidades por un valor
de COP 2.772.468.045.981. En este caso los datos
absurdos dañan los datos de Transacciones
secundarias comerciales del trimestres 2° de 2023, afectando
el
acumulado anual de ese año. .
Por esta razón, pueden presentarse reportes con valores
absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 152.672.002 unidades por un valor
de COP 2.772.468.045.981. En este caso los datos
absurdos dañan los datos de Transacciones
secundarias comerciales del trimestres 2° de 2023, afectando
el
acumulado anual de ese año.
✔
No existe
proporcionalidad entre reportes de
Precios Reportados, Encuestados y Regulados  .
Nótese que los datos de Transacciones
primarias institucionales y comerciales son "monofuente"
corresponden a la presentación comercial o CUM, mientras los de Transacciones secundarias
institucionales o comerciales y finales son de UniDosis
(comprimidos recubiertos que obligan a calcular precios por CUM)
que son "multifuente" y calculados para permitir las
comparaciones. .
Nótese que los datos de Transacciones
primarias institucionales y comerciales son "monofuente"
corresponden a la presentación comercial o CUM, mientras los de Transacciones secundarias
institucionales o comerciales y finales son de UniDosis
(comprimidos recubiertos que obligan a calcular precios por CUM)
que son "multifuente" y calculados para permitir las
comparaciones.
✔
Como puede verse en la parte inferior  DOVATO
CUM 20171830-01 no se encuentra sometido al régimen de
Control Directo, por lo tanto, no tiene precio regulado,
ni máximo de venta, ni ajustado para prestadores (fondo rojo)
pese a su precio y falta de competidores. DOVATO
CUM 20171830-01 no se encuentra sometido al régimen de
Control Directo, por lo tanto, no tiene precio regulado,
ni máximo de venta, ni ajustado para prestadores (fondo rojo)
pese a su precio y falta de competidores.
Gráfico N°13: Pantalla de
seguimiento de DOVATO GSK CUM 20171830-01 de Trimestres 1° de 2023
a 4° de 2024
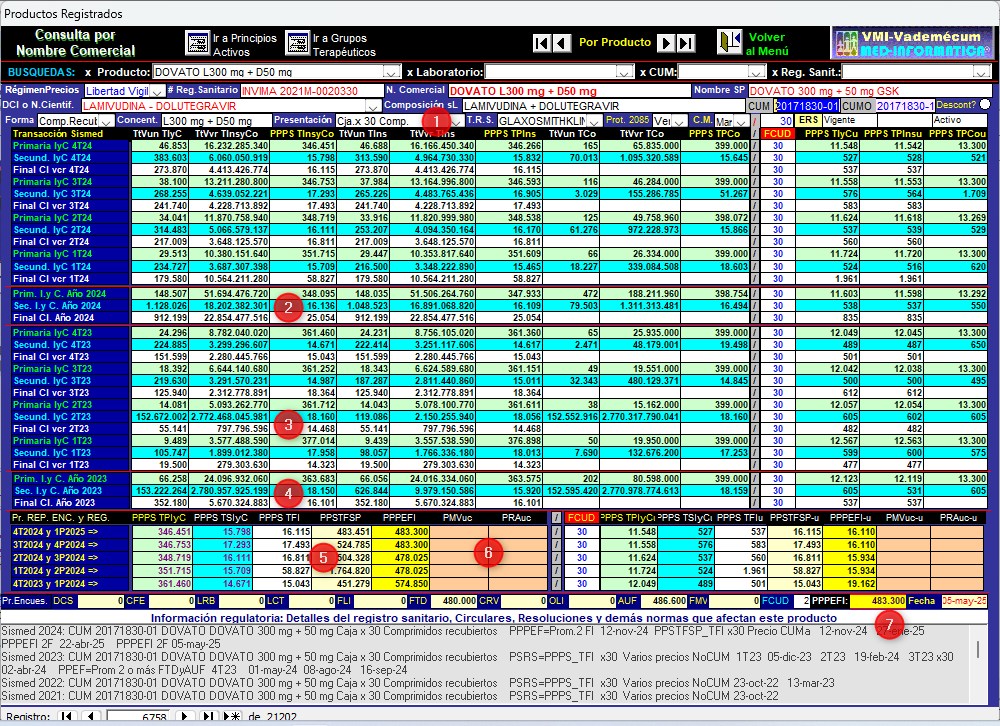
✔ En
2024
DOVATO de
GlaxoSmithKline CUM
20171830-01
sigue sin sre encuentra sometido a régimen de Control Directo
 de la regulación de precios vigente, algo que se
confirma en la parte final de esta pantalla donde los campos de
precios regulados aparecen sin datos.
de la regulación de precios vigente, algo que se
confirma en la parte final de esta pantalla donde los campos de
precios regulados aparecen sin datos.
✔ Actualmente
el sistema de reportes a SISMED sigue sin mecanismos
de validación y analítica de datos   .
Por esta razón, siguen en la plataforma reportes con valores
absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 152.672.002 unidades por un valor
de COP 2.772.468.045.981. En este caso los datos
absurdos de Transacciones
secundarias comerciales del trimestres 2° de 2023,
siguen afectando el
acumulado anual de ese año. .
Por esta razón, siguen en la plataforma reportes con valores
absurdos como del 2° trimestre
de 2023 de Transacciones
secundarias con 152.672.002 unidades por un valor
de COP 2.772.468.045.981. En este caso los datos
absurdos de Transacciones
secundarias comerciales del trimestres 2° de 2023,
siguen afectando el
acumulado anual de ese año.
✔
No existe
proporcionalidad entre reportes de
Precios Reportados, Encuestados y Regulados  .
Nótese que los datos de Transacciones
primarias institucionales y comerciales son "monofuente"
corresponden a la presentación comercial o CUM, mientras los de Transacciones secundarias
institucionales o comerciales y finales son de UniDosis
(comprimidos recubiertos que obligan a calcular precios por CUM)
que son "multifuente" y calculados para permitir las
comparaciones. .
Nótese que los datos de Transacciones
primarias institucionales y comerciales son "monofuente"
corresponden a la presentación comercial o CUM, mientras los de Transacciones secundarias
institucionales o comerciales y finales son de UniDosis
(comprimidos recubiertos que obligan a calcular precios por CUM)
que son "multifuente" y calculados para permitir las
comparaciones.
✔
Como puede verse en la parte inferior  DOVATO
CUM 20171830-01 sigue sin ser sometido al régimen de
Control Directo, por lo tanto, no tiene precio
regulado, ni máximo de venta, ni ajustado para
prestadores (fondo rojo) pese a su precio y falta de
competidores. DOVATO
CUM 20171830-01 sigue sin ser sometido al régimen de
Control Directo, por lo tanto, no tiene precio
regulado, ni máximo de venta, ni ajustado para
prestadores (fondo rojo) pese a su precio y falta de
competidores.
Nota importante: El Precio reportado por el
laboratorio en el último trimestre de 2024 para Tivicay (Dolutegravir
solo) CUM 20071938-01 fue COP 367.657, para
Triumuq (Lamivudina + Abacavir + Dolutegravir)
CUM 20081132-01 fue COP 361.117 y para Dovato (Lamivudina
+ Dolutegravir) COP 346.451. GlaxoSmithKline
reportó precios de Dolutegravir solo Tivicay, superiores a sus
combinaciones Triumeq y Dovato.
2.6.5.
2.6.5. La Combinación Lamivudina+Dolutegravir
está evolucionando más dinámicamente
Existe
suficiente evidencia internacional para el uso de la Combinación LAMIVUDINA + DOLUTEGRAVIR, por tratarse de tratamientos
STR con
✔mayor eficacia,
✔menores efectos secundarios y
✔mejor
relación costo-beneficio, tal como puede verse en esta
presentación del Dr. Boris Revollo B. MD, PhD (Germans Trias i
Pujol University Hospital Infectious Diseases Department). Ver
Archivo de la presentación convertido a PDF.
Gráfico N°14: Presentación de evidencia internacional del
uso de
la Combinación LAMIVUDINA + DOLUTEGRAVIR.
Pulse clich sobre la imagen para ver el PDF

Ver en este punto los gráficos de evolución de ventasen Colombia y esta
presentación que muestra la situación internacional
✔
Resumen de Audio de
la presentación en español:
Dolutegravir_+_Lamivudina__La_Vanguardia_del_Tratamiento_del_VIH.m4a
:✔
Resumen de
Video de la presentación en español:
Dovato__Evidencia_y_Mundo_Real.mp4
Presentación reciente que compara los beneficios de
DTG/3TC sobre Bic/F/TAF
Dolutegravir (DTG) / Lamivudina (3TC) en
el Tratamiento del VIH-1
Fecha: 14 de noviembre de 2023 Presentado por: Boris Revollo B.
MD, PhD, Hospital Universitario Germans Trias i Pujol,
Departamento de Enfermedades Infecciosas
1. Resumen
Ejecutivo
Este documento presenta una revisión de las últimas
actualizaciones de las guías, datos de la vida real y resultados
de estudios clínicos sobre la eficacia y seguridad de la
combinación de Dolutegravir (DTG) y Lamivudina (3TC), conocida
como Dovato, en el tratamiento de la infección por VIH-1. Se
destaca su papel tanto en pacientes naïve como en estrategias de
cambio en pacientes virólogicamente suprimidos, particularmente
en poblaciones con carga viral alta o recuentos bajos de CD4+.
Los datos presentados refuerzan la posición de DTG/3TC como una
opción de tratamiento preferida y eficaz, con bajas tasas de
resistencia emergente y un perfil de seguridad favorable.
2.
Conflictos de Interés
El presentador, Boris Revollo B., ha declarado los siguientes
conflictos de interés:
Becas educativas (Unidad de VIH): UAB, MAG, Primavera Sound
group.
Honorarios y patrocinio de viajes: Merck Sharp & Dohme, Gilead
Sciences, Janssen, ViiV Healthcare.
Co-investigador en ensayos clínicos patrocinados por: Merck
Sharp & Dohme, Gilead Sciences, Janssen, ViiV Healthcare.
No es titular de patentes ni accionista.
No hay revelaciones para ningún miembro de la familia.
3.
Actualización de las Guías y Recomendaciones
Las principales guías clínicas internacionales y nacionales
continúan recomendando o prefiriendo DTG/3TC para el tratamiento
inicial en la mayoría de las personas con VIH-1:
DHHS (Marzo 2023): "Recomendado para la mayoría de las
personas."
EACS (Octubre 2023): "Recomendado."
IAS-USA (Diciembre 2022): "Recomendado."
GESIDA (2022): "Preferido."
Sin embargo, estas recomendaciones vienen con ciertas salvedades
para DTG/3TC en pacientes naïve:
Debe ser HBsAg negativo.
Carga viral de VIH < 500.000 copias/mL (datos limitados en
pacientes con cargas virales > 500.000).
No recomendado para inicio rápido (por datos de TDR y HBV) o
después de un fallo de PrEP (CAB o TDF/FTC).
Se mencionan preocupaciones con ABC y el aumento del riesgo de
infarto agudo de miocardio (AMI), llevando a su retirada en
algunas guías (IAS-USA, BHIVA).
RAL (Raltegravir) también está siendo retirado de las guías para
el inicio (IAS-USA, DHHS, GeSIDA).
Se observa que TAF está asociado con un mayor aumento de peso.
4. DTG/3TC
en Personas Naïve con VIH-1: Éxito en Poblaciones "Especiales"
Estudios clave y análisis de datos de la vida real han
demostrado la eficacia de DTG/3TC en pacientes naïve, incluyendo
aquellos con características que históricamente han sido objeto
de preocupación, como carga viral alta o recuento bajo de CD4+.
4.1.
Estudios GEMINI-1 y GEMINI-2: Resultados Agrupados a la Semana
48
Estos estudios compararon DTG + 3TC con DTG + TDF/FTC. Los
resultados a la Semana 48 mostraron:
Altas tasas de supresión virológica: Ambas combinaciones
demostraron una alta eficacia, con porcentajes de ARN del VIH-1
<50 copias/mL consistentemente altos en diversas
estratificaciones (carga viral basal >100.000 c/mL, ≤100.000 c/mL,
CD4+ >200 células, ≤200 células/mm3).
Bajas tasas de abandono virológico: Se observaron bajas tasas de
abandonos virológicos a la Semana 48.
Sin mutaciones de resistencia emergente: "No se observaron
mutaciones de resistencia emergente a INSTI o NRTI entre los
participantes que cumplieron los criterios de CVW (fallo
virológico confirmado)." Esto subraya la alta barrera genética
de DTG/3TC.
4.2.
Eficacia en un Entorno de "Test-and-Treat" (STAT, REDOLA, CORIS,
TANDEM, DOLAVI)
Varios estudios de la vida real o en entornos de "test-and-treat"
(donde el tratamiento se inicia sin esperar los resultados de la
prueba de resistencia basal) han mostrado resultados
prometedores:
Cero mutaciones de resistencia a la Semana 48 en STAT, REDOLA,
TANDEM y DOLAVI. CORIS reportó 3 pacientes con mutaciones de
resistencia (M184V/I y DRV/c/FTC/TAF en uno).
En el estudio STAT, "131 participantes con ARN del VIH-1 <40 c/mL
a la Semana 7, justo antes del cambio de tratamiento", mostraron
que DTG/3TC es eficaz incluso con una respuesta temprana.
El estudio TANDEM incluyó 126 pacientes, de los cuales 48.4%
iniciaron tratamiento con Dovato con resistencia >100.000 c/mL,
y el 56.2% de los pacientes con >100.000 c/mL no disponían de la
prueba de resistencia. Aún así, los resultados fueron positivos,
con solo un pequeño porcentaje de fallos virológicos.
4.3.
Estudio D2ARLING: DTG+3TC sin prueba de resistencia basal
Este estudio evaluó la eficacia y seguridad de DTG+3TC en PLHIV
naïve sin prueba de resistencia basal al VIH-1.
Diseño: Adultos con infección por VIH-1, ARN del VIH-1 >1000,
sin ART previo, sin infección por HBV ni HCV que requiriera
terapia, sin infecciones oportunistas. Randomizados a DTG 50 mg
+ 3TC 300 mg QD (n=106) o DTG 50 mg + TDF/XTC QD (n=108).
Resultados Virológicos (Semana 24): El 94.34% de los
participantes en el brazo de DTG+3TC y el 95.37% en el brazo de
DTG+TDF/XTC lograron un ARN del VIH-1 <50 copias/mL. La
diferencia fue de -1.03% (IC 95% 7.89% a 5.82%, p=0.97),
demostrando la no inferioridad de DTG-3TC.
"No se observaron mutaciones de resistencia emergentes al
tratamiento a ninguno de los fármacos del estudio en la prueba
genotípica de resistencia al fallo virológico."
4.4. DOLAM-500:
Eficacia en Carga Viral Basal ≥500.000 copias/ml
Este estudio se centró en la eficacia y seguridad de DTG+3TC
como primera línea en pacientes naïve con una carga viral basal
muy alta.
Población: 56 pacientes con ARN del VIH-1 basal ≥500.000 copias/mL.
La mediana de edad fue de 37 años y la mediana de ARN del VIH-1
fue de 1.023.000 copias/mL.
Resultados a Semana 24: 46/56 (82.1%) pacientes alcanzaron ARN
del VIH-1 <50 copias/mL.
Resultados a Semana 48: 35/38 (92.1%) pacientes alcanzaron ARN
del VIH-1 <50 copias/mL.
La supresión virológica fue exitosa incluso en el grupo con ARN
del VIH-1 >3.000.000 copias/mL (7/8 a la Semana 48).
La mediana de CD4+ aumentó de 375.9 a 721.1 células/mm3 a la
Semana 48.
4.5.
Revisión Sistemática de Datos del Mundo Real (Letang et al.)
Una revisión sistemática confirmó la efectividad de DTG+3TC en
pacientes naïve con carga viral alta (≥100.000 copias/mL) o
recuento bajo de CD4+ (<200 células/mm3).
Carga Viral Alta: "la proporción de individuos con carga viral
basal alta que lograron la supresión virológica fue del 76%
(61/80) en la Semana 24, 97% (208/215) en la Semana 48 y 87%
(39/45) en la Semana 96."
CD4+ bajo: Proporciones similares de supresión virológica en la
Semana 24 (88%), Semana 48 (94%) y Semana 96 (70%) en pacientes
con CD4+ <200 células/mm3.
Estos datos demuestran que DTG+3TC es eficaz en estas
poblaciones "especiales" en un entorno de la vida real.
5. Nuevos
Datos sobre Estrategias de Cambio de Tratamiento
DTG/3TC también se está utilizando con éxito como estrategia de
cambio en pacientes virólogicamente suprimidos.
5.1. El
Estudio SOUND: Cambio de Biktarvy a Dovato (Análisis Interino
Semana 48)
Este estudio evaluó a pacientes virológicamente suprimidos con
bictegravir/emtricitabina/tenofovir-alafenamida (B/F/TAF) que
cambiaron a DTG/3TC.
Criterios de inclusión: Carga viral del VIH < 50 copias/mL
durante ≥ 6 meses, tomando B/F/TAF ≥24 semanas, sin prueba de
resistencia conocida, sin antecedentes de fallo virológico en
los 12 meses anteriores.
Resultados a Semana 48: El 92% de los pacientes permanecieron
virológicamente suprimidos después de cambiar a DTG/3TC.
5.2.
Estudio TANGO: No Inferioridad de DTG/3TC frente a Regímenes
Basados en TAF (Semana 196)
Un estudio fase 3, aleatorizado, abierto, multicéntrico y de no
inferioridad.
Diseño: Adultos virólogicamente suprimidos (ARN del VIH-1 <50 c/mL
durante ≥6 meses) con un régimen basado en TAF estable. Se
randomizaron a DTG/3TC (cambio temprano) o a continuar el
régimen basado en TAF, con la opción de cambiar a DTG/3TC en la
Semana 144 (cambio tardío).
Resultados de eficacia a Semana 196: "Pocos participantes del
grupo ES (3/369 [<1%]; IC 95% 0.0%-1.7%) y 0/298 (95% CI,
0.0%-0.0%) participantes del grupo LS tuvieron ARN del VIH-1 ≥50
c/mL en la población general en la Semana 196 por análisis
Snapshot (ITT-E)."
"Los criterios de abandono virológico confirmado fueron
cumplidos por 1/369 (<1%) participante del grupo ES y ningún
participante del grupo LS hasta la Semana 196, sin observarse
resistencia."
Conclusiones: "Estos resultados apoyan que el cambio a DTG/3TC
desde regímenes basados en TAF mantiene eficazmente la supresión
virológica en diferentes subgrupos demográficos y de
características basales en las semanas 48 y 196."
5.3. Datos
del Mundo Real sobre el Cambio: DTG/3TC versus BIC/FTC/TAF
Varios estudios de la vida real (Tordi et al., Cheng et al.,
Troya et al., Farinacci et al., Long et al.) demuestran una
eficacia similar de DTG/3TC en comparación con BIC/FTC/TAF en
pacientes con experiencia en el tratamiento y un perfil de
seguridad y tolerabilidad favorable, incluyendo un impacto
neutral o mejorado en los parámetros lipídicos y un menor riesgo
de ganancia de peso asociado a TAF.
6.
Conclusiones Generales
DTG/3TC es preferido/recomendado en la mayoría de las guías para
el tratamiento inicial del VIH-1, con consideraciones
específicas para pacientes HBsAg negativos y cargas virales.
Eficacia robusta en pacientes naïve: Los estudios GEMINI 1 y 2,
D2ARLING, DOLAM-500 y las revisiones sistemáticas de la vida
real confirman que DTG/3TC es altamente efectivo para lograr la
supresión virológica, incluso en poblaciones con carga viral
alta (incluyendo >500,000 copias/mL) o recuentos bajos de CD4+,
con una baja tasa de desarrollo de resistencia.
Eficacia y seguridad en el cambio de tratamiento: Los estudios
SOUND y TANGO demuestran que el cambio a DTG/3TC es una
estrategia segura y eficaz para mantener la supresión virológica
en pacientes previamente suprimidos con regímenes basados en TAF
o Biktarvy.
Baja emergencia de resistencia: Una característica destacada en
todos los estudios presentados es la muy baja o nula aparición
de mutaciones de resistencia emergente al tratamiento con DTG/3TC,
lo que subraya su alta barrera genética.
Consideraciones en el cambio: Es crucial revisar el historial de
ART para asegurar la viabilidad del cambio y mantener la
supresión virológica sin comprometer futuras opciones de
tratamiento, especialmente si hay resistencia a los NRTI.
En resumen, la evidencia actual respalda firmemente la
combinación de Dolutegravir y Lamivudina como una opción de
tratamiento central y versátil para el VIH-1, tanto para el
inicio del tratamiento como para las estrategias de cambio,
ofreciendo alta eficacia, durabilidad y un perfil favorable de
resistencia.
2.7.
2.7. Validación y
análisis Ventas Trimestrales Dolutegravir y Combinaciones 1T20a4T24
El
análisis de los reportes trimestrales a SISMED durante la
vigencia de la
Circular 06 de 2018 que
cambió sistema de reportes
(fue publicado en el Diario Oficial No. 50.677 del 6 de agosto
del 2018 e implementado a partir del 4° trimestre de 2019)
muestra que el crecimiento de ventas en
unidades y valores de la molécula DOLUTEGRAVIR (TIVICAY®)
y su Combinación con LAMIVUDINA y ABACAVIR (TRIUMEQ®).fue
igualmente dinámico. El ingreso de la
Combinación LAMIVUDINA + DOLUTEGRAVIR (DOVATO®)
en el trimestre 4° de 2021 acentuó claramente esa tendencia, tal
como puede verse en el siguiente gráfico:
2.7.1.
2.7.1. Validación y análisis Ventas Trimestrales Dolutegravir y
Combinaciones 1T20a4T23
El
análisis de los reportes trimestrales a SISMED durante la
vigencia de la
Circular 06 de 2018 que
cambió sistema de reportes
(fue publicado en el Diario Oficial No. 50.677 del 6 de agosto
del 2018 e implementado a partir del 4° trimestre de 2019)
muestra que el crecimiento de ventas en
unidades y valores de la molécula DOLUTEGRAVIR (TIVICAY®)
y su Combinación con LAMIVUDINA y ABACAVIR (TRIUMEQ®).fue
igualmente dinámico. El ingreso de la
Combinación LAMIVUDINA + DOLUTEGRAVIR (DOVATO®)
en el trimestre 4° de 2021 acentuó claramente esa tendencia, tal
como puede verse en el siguiente gráfico:
Gráfico N°15: DOLUTEGRAVIR y
Combinaciones. Evolución de ventas trimestrales en unidades y
valores de Trimestres 1° de 2020 a 4° de 2023
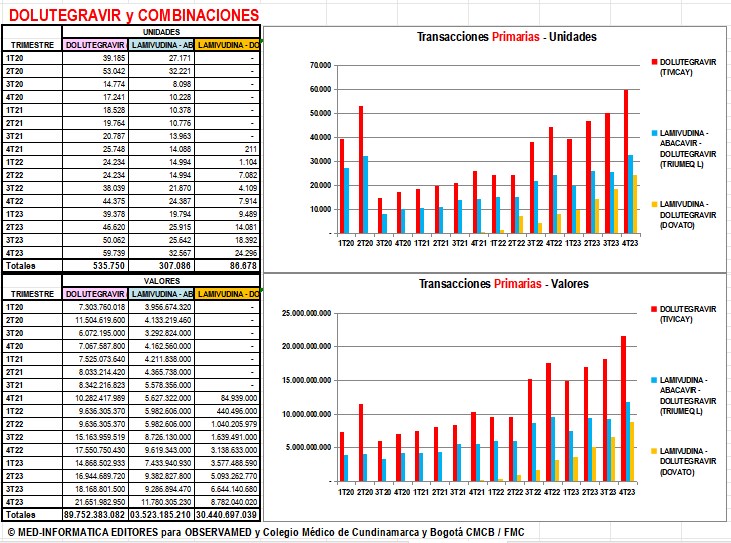
A
partir del 4° trimestre de 2019)
muestra que el crecimiento de ventas en
unidades y valores de la molécula DOLUTEGRAVIR (TIVICAY®)
y su Combinación con LAMIVUDINA y ABACAVIR (TRIUMEQ®).fue
igualmente dinámico. El ingreso de la
Combinación LAMIVUDINA + DOLUTEGRAVIR (DOVATO®)
en el trimestre 4° de 2021 acentuó claramente esa tendencia, tal
como puede verse en el siguiente gráfico:
A
partir del 4° trimestre de 2019)
muestra que el crecimiento de ventas en
unidades y valores de la molécula DOLUTEGRAVIR (TIVICAY®)
y su Combinación con LAMIVUDINA y ABACAVIR (TRIUMEQ®).fue
igualmente dinámico. El ingreso de la
Combinación LAMIVUDINA + DOLUTEGRAVIR (DOVATO®)
en el trimestre 4° de 2021 acentuó claramente esa tendencia, tal
como puede verse en el siguiente gráfico:
2.7.2.
2.7.2. Validación
y análisis Ventas Trimestrales Dolutegravir y Combinaciones 1T21a4T24
A
partir del 4° trimestre de 2019)
muestra que el crecimiento de ventas en
unidades y valores de la molécula DOLUTEGRAVIR (TIVICAY®)
y su Combinación con LAMIVUDINA y ABACAVIR (TRIUMEQ®).fue
igualmente dinámico. El ingreso de la
Combinación LAMIVUDINA + DOLUTEGRAVIR (DOVATO®)
en el trimestre 4° de 2021 acentuó claramente esa tendencia, tal
como puede verse en el siguiente gráfico
Gráfico N°16: DOLUTEGRAVIR y
Combinaciones. Evolución de ventas trimestrales en unidades y
valores de Trimestres 1° de 2021 a 4° de 2024
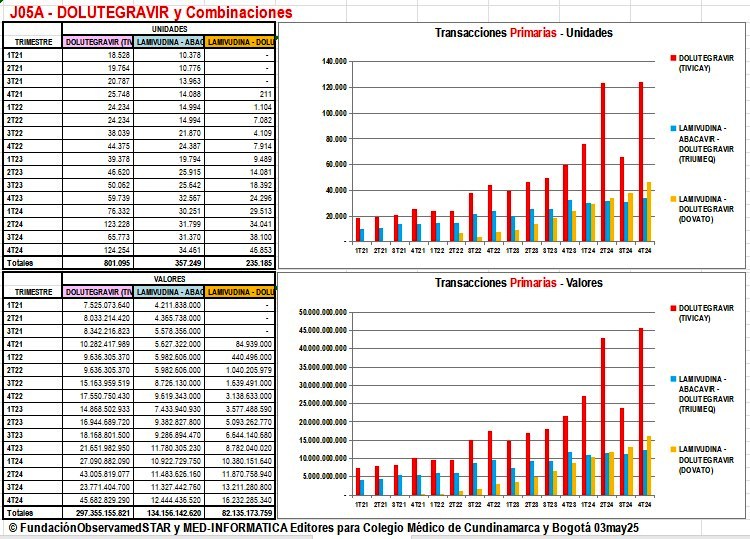
A
partir del 4° trimestre de 2019)
muestra que el crecimiento de ventas en
unidades y valores de la molécula DOLUTEGRAVIR (TIVICAY®)
y su Combinación con LAMIVUDINA y ABACAVIR (TRIUMEQ®).fue
igualmente dinámico. El ingreso de la
Combinación LAMIVUDINA + DOLUTEGRAVIR (DOVATO®)
en el trimestre 4° de 2021 acentuó claramente esa tendencia, tal
como puede verse en el siguiente gráfico:
A
partir del 4° trimestre de 2019)
muestra que el crecimiento de ventas en
unidades y valores de la molécula DOLUTEGRAVIR (TIVICAY®)
y su Combinación con LAMIVUDINA y ABACAVIR (TRIUMEQ®).fue
igualmente dinámico. El ingreso de la
Combinación LAMIVUDINA + DOLUTEGRAVIR (DOVATO®)
en el trimestre 4° de 2021 acentuó claramente esa tendencia, tal
como puede verse en el siguiente gráfico:
2.7.3.
2.7.3. Prescripciones
de Dolutegravir y sus Combinaciones en MiPres de años 2021a2025
El análisis de las
prescripciones de DOLUTEGRAVR y sus combinaciones en la
plataforma MiPres también muestra inconsistencias prominentes
que invalidan cualquier evaluación con las modalidades que
permitía la misma. Mostramos aquí lo poco que puede verse para 5
regiones y 5 EPSs más importantes :
Gráfico N°17. Prescripciones
reportadas a MiPres de DOLUTEGRAVIR y Combinaciones de 2021 a 2023 en 5 regiones
y 5 EPS
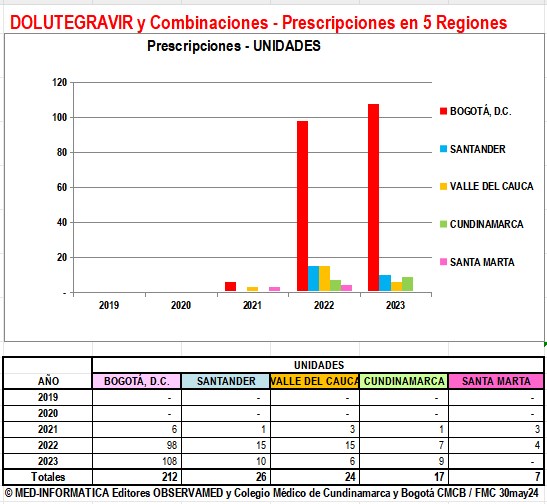 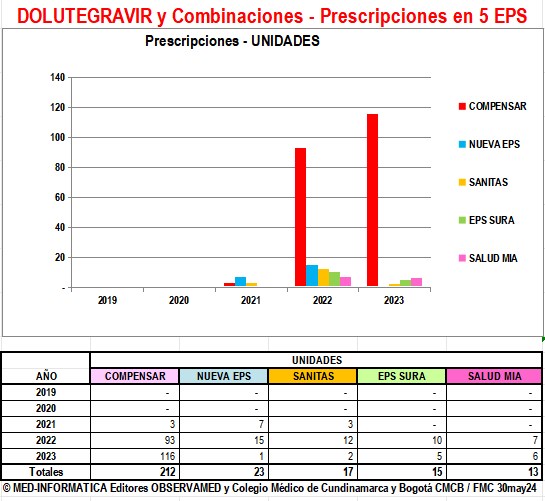
El problema está en que el número de prescripciones
reportadas por regiones es mínimo y las cifras resultan tan
insignificantes que no alcanzan ni siquiera para configurar una
muestra mínimamente significativa.
El problema está en que el número de prescripciones
reportadas por EPSs es mínimo y las cifras resultan tan
insignificantes que no alcanzan ni siquiera para configurar una
muestra mínimamente significativa.
Gráfico N°18. Prescripciones
reportadas a MiPres de DOLUTEGRAVIR y Combinaciones de 2021 a 2025 en 5 regiones
y 5 EPS
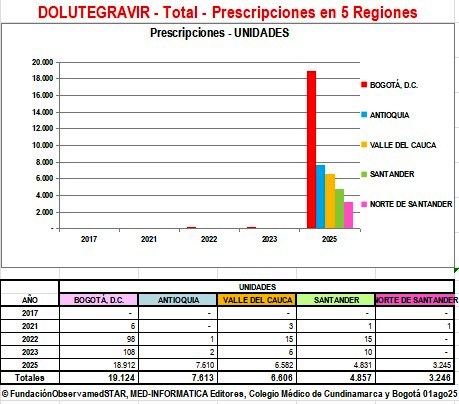 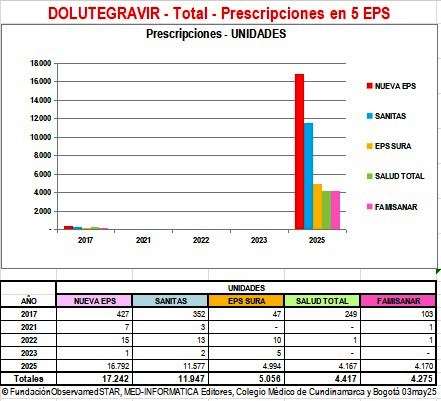
El problema está en que el número de prescripciones
reportadas por regiones es mínimo y las cifras resultan tan
insignificantes que no alcanzan ni siquiera para configurar una
muestra mínimamente significativa.
El análisis de las
prescripciones de DOLUTEGRAVR y sus combinaciones en la
plataforma MiPres muestra que de 2021 a 2023 el mayor número de
prescripciones se habría generado en las 5 EPSs más importantes
muestra a Compensar, Nueva EPS, Sánitas, EPS Sura y Salud Mía.
2.7.4.
2.7.4.
Evolución de
ventas anuales de GlaxoSmithKline reportadas a SISMED 2014 a
2024
Finalmente, es
interesante conocer la importancia de DOLUTEGRAVIR y sus
Combinaciones para GlaxoSmithKline en Colombia, algo que
permitiría estimar el nivel de recursos que empleará para
defender esta patente. Para tal fin, mostramos las ventas de
esta multinacional farmacéutica en los años 2014 a 2023 y los
totales de ventas reportadas por esta firma en el último
trimestre de 2023.
Gráfico N°19. Evolución de ventas
anuales de GlaxoSmithKline reportadas a SISMED. Toda la línea de
2014 a 2023 y solo Antivirales VIH de 2015 a 2024
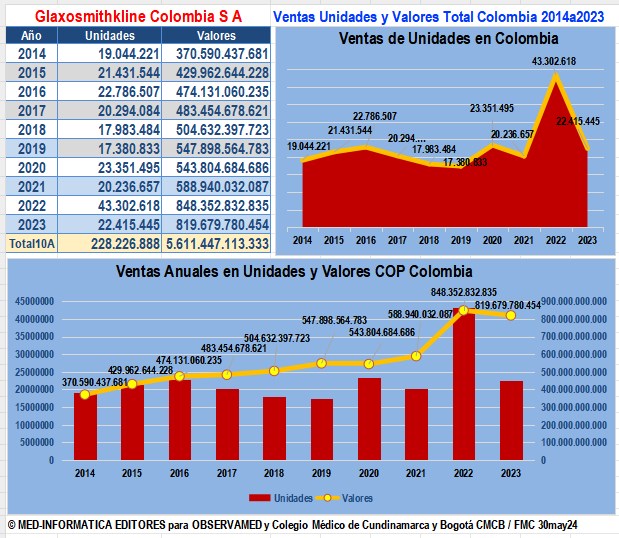 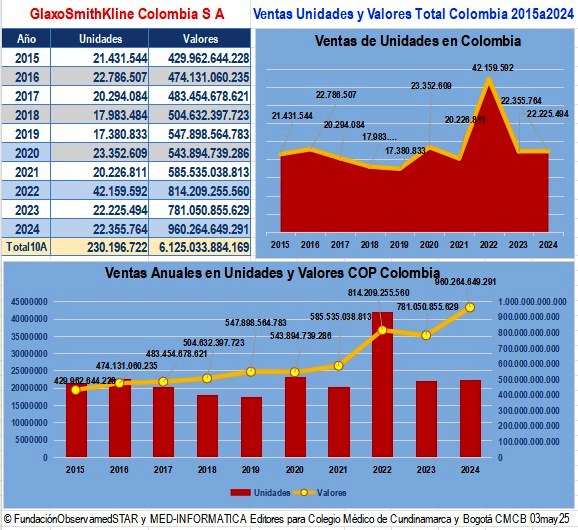
La evolución de las
ventas de GlaxoSmithKline en Colombia, de acuerdo con sus
reportes a SISMED de los años 2014 a 2023, puede considerarse
estable en unidades y creciente en valores hasta el año 2021. En
2022 se observa un incremento considerable, también en unidades
y valores que podría atribuirse a ventas de Dolutegravir y sus
combinaciones. En 2023 se habrían desplomado las ventas en
unidades, con solo una pequeña disminución de las ventas en
valores.
La interpretación de estos cambios
tan grandes debe tomar en cuenta la posibilidad de errores
graves, ya reconocidos por esta farmacéutica en sus reportes de
años anteriores.
2.7.5.
2.7.5.
Importancia DOLUTEGRAVIR y Combinaciones para GlaxoSmithKline
4T23 y 4T24
Tal como puede verse en el Gráfico
N°10 DOLUTEGRAVIR y sus Combinaciones son extremadamente Importantes
para GlaxoSmithKline en Colombia. Según reportes a SISMED del
4°trimestre de 2023, 3 de las 5 presentaciones más vendidas en
valores corresponden a DOLUTEGRAVIR TIVICAY CUM 20071938-01 y
sus combinaciones TRIUMEQ CUM 20081132-01 y DOVATO CUM
20171830-01.
Gráfico N°20. Importancia de DOLUTEGRAVIR y sus Combinaciones para GlaxoSmithKline en
Colombia según reportes del 4° trimestre de 2023
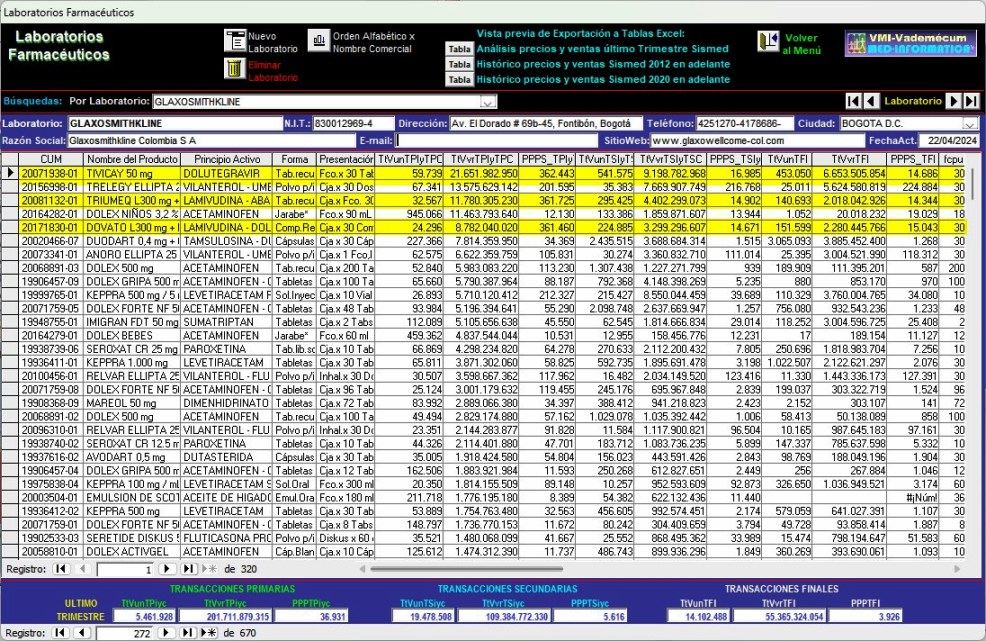
Según
reportes de GlaxoSmithKline a SISMED del 2° trimestre de
2024, TIVICAY 50 mg
CUM 20071938-01 vendió 123.228 unidades por más de
$43.000 millones con Precio PPPS de $348.994. Casi
duplicó las ventas del trimestre anterior y
prácticamente la totalidad de estas ventas correspondió
al canal institucional.
Gráfico N°21. Importancia de DOLUTEGRAVIR y sus Combinaciones para GlaxoSmithKline en
Colombia según reportes del 4° trimestre de 2024
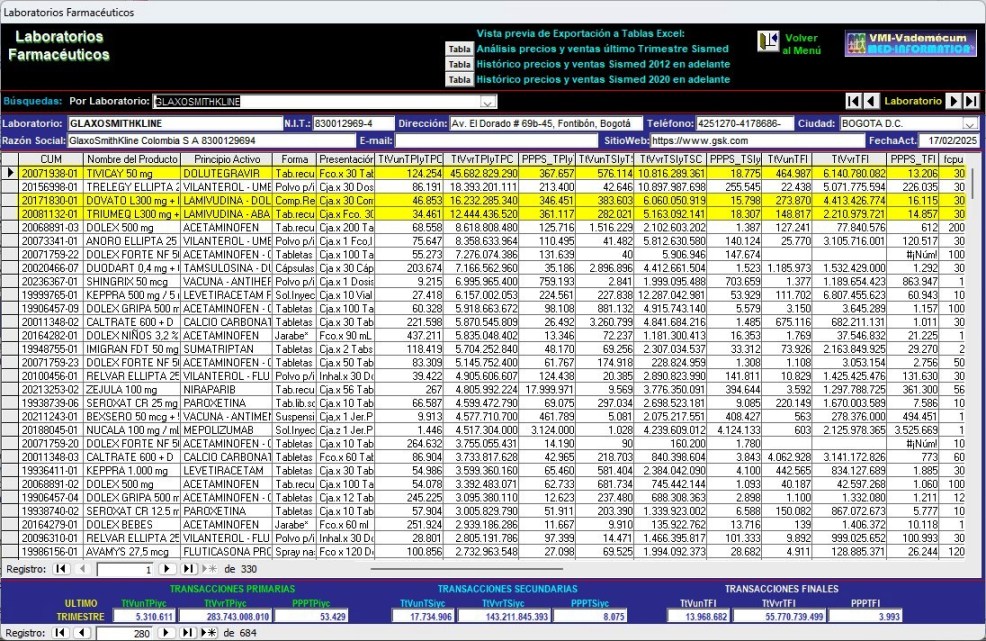
El total
de ventas del semestre, en unidades y valores,
prácticamente igualó el total de ventas del año 2023.
Este incremento sugiere que GlaxoSmithKline adelantó
alguna estrategia de ventas para mitigar el efecto de la
Licencia Obligatoria. Se incrementaron más las
Transacciones Primarias por canal institucional.
Los reportes
absurdos del 2° trimestre de 2023 con Transacciones
secundarias de 531.937.970 unidades por COP 9.575.398.029.459
en canal comercial no se corrigieron. El sistema de reportes a SISMED
sigue sin mecanismos
de validación y analítica de datos. No existe
proporcionalidad entre transacciones.
La falta de
mecanismos de validación y analítica de datos en SISMED
y falta de proporcionalidad entre los datos de Transacciones
primarias institucionales y comerciales que son "monofuente"
con los de Transacciones secundarias
institucionales o comerciales y finales que son "multifuente" es
más que evidente.
Al comparar
solo Precios PPPS de Transacciones primarias, secundarias
y finales puede verse que el Laboratorio
reporta precios de cajas por 30 tabletas pero los
precios de
los demás actores y de cobros y recobros finales son por tableta.
Esto obliga a calcular precios por CUM que aparecen en los campos amarillos..
Los precios
regulados, el máximo de venta y el ajustado para
prestadores (fondo rojo) siguen más que triplicando los
precios reportados por el Laboratorio. Los
listados de precios regulados del 01ago24 y 02sep24 NO corrigen estos
errores. Este incremento injustificado de precios
regulados se ve a su lado (6).
El Precio
Público Promedio Encuestado PPPE en 5 plataformas de
Internet el trimestre 2° de 2024 fue $725.487
caja de 30 tabletas ($24.183 cada tableta). Por
lo tanto, los precios regulados de TIVICAY 50 mg de
GlaxoSmithKline siguen más que duplicando los precios de venta al
público. Este seguimiento no
incluye CUM 20166850-01 TIVICAY Dolutegravir Base 10mg/1U Sólido
Oral x 30, o CUM 20166851-01 TIVICAY Dolutegravir Base 25mg/1U
Sólido Oral x 30 de GLAXOSMITHKLINE porque no reportaron ventas
ni precios a SISMED, al igual que CUM 20208612-01 TIVICAY
Dolutegravir Base 5mg/1U Sólido Oral x 60 y CUM
20208612-02 TIVICAY Dolutegravir Base 5mg/1U Sólido Oral x 60
muestra médica también de VIIV HEALTHCARE.
|
En resumen:
2. Contexto General
y Calidad de la Información en SISMED
- Evolución de
Ventas: Las ventas de antivirales para
VIH-SIDA en Colombia oscilaron entre 4.2 millones de
unidades por casi 132.5 mil millones de COP en 2015
y casi 6 millones de unidades por 180 mil millones
de COP en 2020. En 2021, hubo una reducción a 1.97
millones de unidades, posiblemente debido a la
pandemia de COVID-19, pero luego experimentaron un
crecimiento dinámico hasta alcanzar 6.13 millones de
unidades por COP 396.4 mil millones en 2024. El
acumulado de la década 2015-2024 sumó 45.7 millones
de unidades por 1.98 billones de COP en valores
corrientes.
-
Concentración del Mercado: Este mercado
muestra un alto grado de concentración,
con GlaxoSmithKline (48%) y Gilead (16%, en
co-marketing con Biotoscana y Stendhal) sumando el
64% de participación.
2. Antivirales
Específicos y sus Ventas
- Análisis de
Reportes de Antivirales VIH (Punto 2.2 y 2.3):
- Entre el 1T2021
y el 4T2024, la opción más vendida en
unidades fue Tenofovir Disoproxil +
Emtricitabina (Seven Pharma). Le siguieron
Dolutegravir solo (Tivicay), y sus combinaciones
con Lamivudina (Dovato) y con Lamivudina +
Abacavir (Triumeq), todos de Glaxosmithkline.
- En
valores, Dolutegravir (Tivicay) y sus
combinaciones (Dovato, Triumeq) de
Glaxosmithkline fueron las más vendidas,
prácticamente monopolizando el mercado con
precios más elevados. Esta dominancia
se ha hecho más evidente desde la introducción
de Triumeq (2015) y Dovato (2021).
- Evolución de
Ventas de Dolutegravir y Combinaciones (Punto 2.4):
- Dolutegravir (Tivicay)
obtuvo registro sanitario en 2014 e inició
reportes a SISMED en 2015.
- La combinación
Lamivudina + Abacavir + Dolutegravir (Triumeq)
se registró en 2015, y Lamivudina + Dolutegravir
(Dovato) en 2021.
- Entre 2015 y
2023, las ventas acumuladas superaron el millón
de unidades y los $400,000 millones de COP. En
2024, las ventas ascendieron a 665,808 unidades
por casi COP $237.4 mil millones.
- La estrategia de
combinaciones de dosis fija ("Single Treatment
Regimen - STR") ha sido muy beneficiosa para
GlaxoSmithKline, aunque son criticables las
técnicas de "evergreening" y la "protección de
datos del Decreto 2085" para extender la
propiedad intelectual.
- Análisis
Detallado de Tivicay (Punto 2.5 y 2.6):
- Dolutegravir (Tivicay
50 mg) está incluido en normas farmacológicas y
su precio aparece regulado, con el Plan de
Beneficios (PBS) incluyendo todas sus
concentraciones. La protección de datos de
prueba del Decreto 2085 para Dolutegravir venció
el 5 de enero de 2020, aunque GlaxoSmithKline
sigue reclamando la patente internacional.
- Se observaron
inconsistencias en los reportes de
SISMED, como valores absurdos en
Transacciones Secundarias y Finales, así como la
facturación de "muestras médicas sin
valor comercial" (CUM 20071938-02) al
sistema de salud, lo cual es ilegal y persiste
hasta 2024.
- Los
precios regulados de Tivicay 50 mg de
GlaxoSmithKline más que cuadruplican los precios
reportados por el laboratorio y más que
triplican los precios encuestados en farmacias
de internet.
- La falta de
mecanismos de validación y análisis de datos en
SISMED es una debilidad institucional que
favorece la protección de la propiedad
intelectual de las farmacéuticas y deteriora el
sistema de información. La implementación de
la Licencia Obligatoria es vista como un paso
correcto para corregir estas inconsistencias.
- Análisis
Detallado de Triumeq (Punto 2.6.3):
- La combinación
Triumeq (GlaxoSmithKline CUM 20081132-01)
también está bajo régimen de Control Directo de
precios, y su precio regulado es casi
cuatro veces superior al precio de venta
reportado por el laboratorio.
- Se reproducen
las inconsistencias en los reportes, con valores
absurdos en Transacciones Secundarias que
afectan la calidad de los datos. Nuestros
análisis se basan en Transacciones Primarias
debido a la fiabilidad de los datos monofuente.
- Análisis
Detallado de Dovato (Punto 2.6.4):
- Dovato (GlaxoSmithKline
CUM 20171830-01) no está sometido a
régimen de Control Directo de precios,
por lo que no tiene precio regulado, a pesar de
su costo y la falta de competidores.
- Persisten los
valores absurdos en los reportes de
Transacciones Secundarias.
- Se destaca
que los precios reportados por GlaxoSmithKline
para Dolutegravir solo (Tivicay) en el 4T2024
fueron superiores a sus combinaciones Triumeq y
Dovato.
- Dinamismo de
Lamivudina+Dolutegravir (Punto 2.6.5):
- Existe una
fuerte evidencia internacional
que respalda la combinación Lamivudina +
Dolutegravir (Dovato) como un tratamiento STR
por su mayor eficacia, menores efectos
secundarios y mejor relación costo-beneficio.
- Las guías
clínicas internacionales y nacionales lo
recomiendan o prefieren para el tratamiento
inicial, con algunas salvedades (HBsAg negativo,
carga viral < 500.000 copias/mL).
- Estudios como
GEMINI-1, GEMINI-2, D2ARLING y DOLAM-500
confirman su robusta eficacia en pacientes
naïve, incluso con carga viral alta o
recuentos bajos de CD4+, y una baja tasa
de desarrollo de resistencia.
- También es una
estrategia segura y eficaz para el cambio de
tratamiento en pacientes virológicamente
suprimidos, como lo demuestran los estudios
SOUND y TANGO.
- Ventas
Trimestrales de Dolutegravir y Combinaciones (Punto
2.7):
- El análisis de
los reportes trimestrales a SISMED desde el
1T2020 hasta el 4T2024 muestra un
crecimiento dinámico de las ventas de
Dolutegravir (Tivicay) y Triumeq, acentuado con
el ingreso de Dovato en el 4T2021.
-
Prescripciones en MiPres (Punto 2.7.3):
- El análisis de
las prescripciones de Dolutegravir y sus
combinaciones en la plataforma MiPres también
revela inconsistencias prominentes
que invalidan cualquier evaluación. El número de
prescripciones reportadas por regiones y EPS es
mínimo e insuficiente para configurar una
muestra representativa.
- Importancia
para GlaxoSmithKline (Punto 2.7.4 y 2.7.5):
- Las ventas de
GlaxoSmithKline en Colombia fueron estables en
unidades y crecientes en valores hasta 2021, con
un incremento considerable en 2022 atribuible a
Dolutegravir y sus combinaciones. Aunque en 2023
las ventas en unidades "se desplomaron", los
valores solo disminuyeron ligeramente. Grandes
cambios en los reportes podrían indicar errores
graves.
- Dolutegravir y
sus combinaciones son extremadamente
importantes para GlaxoSmithKline en Colombia,
representando 3 de sus 5 presentaciones más
vendidas en valores en el 4T2023. En el 2T2024,
Tivicay 50 mg casi duplicó las ventas del
trimestre anterior, mayormente por el canal
institucional, sugiriendo una estrategia para
mitigar el efecto de la Licencia Obligatoria.
- La persistencia
de reportes absurdos y la falta de
validación en SISMED siguen siendo
evidentes. Los precios regulados no se han
corregido y siguen cuadruplicando los precios
reportados por el laboratorio y triplicando los
precios de venta al público.
En síntesis, el punto 2
revela un mercado de antivirales para VIH-SIDA en
Colombia dominado por GlaxoSmithKline con Dolutegravir y
sus combinaciones, caracterizado por un crecimiento
dinámico de ventas y la persistencia de graves
inconsistencias y "datos absurdos" en el sistema de
información SISMED. Estas deficiencias afectan
la calidad de los datos, la efectividad de la regulación
de precios, con precios regulados que superan
significativamente los precios de venta y encuestados
(en los casos mostrados y varios más)
y deterioran la transparencia del sistema. El documento subraya la
debilidad institucional frente a
prácticas que favorecen la propiedad intelectual de las
farmacéuticas y el daño al sistema de información. La
Licencia Obligatoria para Dolutegravir
se presenta como una medida crucial para abordar
estructuralmente estas inconsistencias. |
3.
3. VIH-SIDA
en Colombia según Informes de la CAC, GPC, IETS, SIVIGILA y el INS
a 2024
Desde la perspectiva de la evidencia internacional el énfasis en
DOLUTEGRAVIR de la política del actual gobierno resulta
pertinente, pero desde la perspectiva de la realidad nacional
ese sesgo puede no ser lo única única opción pertinente, tal
como puede verse en los hechos que se describen a continuación.
Gráfico N°22. Ejemplo de
percepción de pacientes de dificultades e incumplimientos en su
atención farmacéutica
Entrevistas con pacientes,
cuidadores y organizaciones de Cali y Medellín sirven de ejemplo
de lo que puede estar sucediendo en Colombia
El cumplimiento de las resoluciones de implementación de la
Licencia Obligatoria para Dolutegravir y su correcta aplicación
en el sistema de atención farmacéutica,, seguramente contribuirá
a la solución estructural de este problema en el sistema de
salud colombiano. Por el contrario, la revocatoria de estas
medidas por orden judicial se constituirá en una verdadera
catástrofe sanitaria para la salud pública y económica para ewl
sistema de salud.
3.1.
3.1. VIH-SIDA en Colombia según Informes Cuenta de Alto Costo de
los años 2022 a 2024
De acuerdo con los
documentos de "Situación del VIH en Colombia" de los años 2022,
2023 y 2024 que publicó la Cuenta de Alto Costo CAC podemos
conocer la evolución de esta patología en el país. Por su
importancia, sometimos estas 3 fuentes a las posibilidades de
análisis y presentación que ofrece NotebookLM de Google.
Gráfico N°23. Publicaciones de la
Cuenta de Alto Costo CAC "Situación del VIH en Colombia" de los
años
2022,
2023 y
2024

Copias "Archivo Reserva Med-Informática ARMI" de los Informes
publicados por la cuenta de Alto Costo CAC de los años
2022,
2023 y
2024 que aquí se usaron
Ver Boletín de la Cuenta de Alto Costo del 01dic24:
https://cuentadealtocosto.org/noticias/dia-mundial-de-la-concientizacion-y-respuesta-al-vih/
✔ Resumen
de Video Inicial:
VIH_en_Colombia__Resumen_minimo_Informes_2022_2023_2024_de_la_Cuenta_de_Alto_Costo_01ago25.mp4
✔
Resumen de Audio del Informe del
año 2022:
VIH_en_Colombia_2022__Retos_y_Avances_en_Diagnóstico_y_Tratamiento_.m4a
✔ Resumen
de Video del Informe de 2022:
HIV_in_Colombia__2022_CAC_Video_Report_Analysis.mp4
✔
Resumen de Audio del Informe del
año 2023:
VIH_en_Colombia_2023__Retos_y_Avances_en_Tratamiento_y_Cobertura.m4a
✔
Resumen de Audio 2 del
año 2023: VIH_en_Colombia_2023__Radiografía_de_la_Epidemia_y_el_Desafío_de_la_Cobertura_y_Diagnóstico_Tardío.m4a
✔ Resumen
de Video del Informe de la Cuenta de Alto Costo de
2023:
VIH_en_Colombia__Análisis_del_Informe_2023.mp4
✔
Resumen de Audio del Informe del
año 2024:
VIH_en_Colombia_2024__Retos_y_Avances_en_Tratamiento_y_Cobertura.m4a
✔ Resumen
de Video del Informe de la Cuenta de Alto Costo de 2024:
VIH_en_Colombia__Claves_del_Informe_Alto_Costo_2024.mp4
Importante:
NoteBookLM aún no es perfecto. Si encuentra inconsistencias por
favor infórmenos al correo
andiarey.samaytatiana@gmail.com
Este documento ofrece una cronología
del VIH en
Colombia, revelando la evolución de la respuesta del país
ante la epidemia. La cronología resalta hitos legislativos,
normativas de salud pública y datos epidemiológicos, como la
tasa de casos incidentes y la mortalidad asociada al VIH a lo
largo de los años, evidenciando tanto avances en prevención y
tratamiento como desafíos persistentes, como el diagnóstico
tardío.
✔
Cronología VIH en Colombia
según informes de la Cuenta de Alto Costo
• Desde 1999, cuando el Ministerio de Salud t Protección
Social MSPS publica la Resolución 1995 de 1999, que reglamenta
el manejo de la historia clínica, después de 2002 cuando a nivel
mundial, los programas de prevención de la transmisión vertical
del VIH habían evitado 4 millones de nuevas infecciones en
niños:
• En 2010, se publica la Ley 1403 de 2010 en Colombia.
Desde este año, se observó una disminución del 37% en las
muertes anuales por VIH en la región de las Américas, y los
datos globales mostraron una reducción del 69% al 51% de
muertes relacionadas con la infección por VIH.
• En enero de 2011, se publica "Late presentation of
HIV infection: a consensus definition" en HIV Med.
• En septiembre de 2011, se publican las "Orientaciones
terminológicas de ONUSIDA".
• En 2012, la Cuenta de Alto Costo (CAC) inició el
registro de casos incidentes de VIH con 5.275 casos reportados.
También se publicaron la Resolución Número 0783 de 2012 del MSPS
y la Ley Estatutaria de habeas data 1581 de 2012 para la
protección de datos personales.
• En 2013, se publicó el Decreto Nacional 1377 de 2013,
regulando el manejo de datos sensibles, y la Declaración de
Helsinki de la AMM sobre principios éticos para la investigación
médica. El número de casos incidentes de VIH fue de 5.558.
• En enero de 2014, se publicó "Marco conceptual y legal
sobre la gestión de riesgo en Colombia: Aportes para su
implementación".
• En 2014, la CAC estableció un consenso de indicadores
para evaluar la gestión del riesgo en la atención de personas
viviendo con el VIH en Colombia. El número de casos incidentes
de VIH fue de 4.882.
• En 2015, el MSPS publicó la Resolución 1912 de 2015, y
se registraron 7.437 casos incidentes de VIH.
• En enero de 2016, se publicó "Epidemiología de la
infección por el virus de inmunodeficiencia humana en pacientes
hospitalizados...".
• En 2016, UNAIDS publicó "The need for routine viral
load testing", y los casos incidentes de VIH aumentaron a
8.209.
• En junio de 2017, CIOMS y la OMS publicaron "Pautas
éticas internacionales para la investigación relacionada con la
salud con seres humanos".
• En 2017, se observó una tendencia ascendente en la
detección temprana de pacientes incidentes de VIH, con 9.399
casos.
• En 2018, se publicó "Interventions to significantly
improve service uptake and retention...", y los casos
incidentes de VIH alcanzaron los 10.246.
• En 2019, se inició la medición en el grupo intersexual
para el conteo de linfocitos T CD4+, y el MSPS estableció la
obligatoriedad del reporte anual de la población con VIH/sida
mediante la Resolución 0273 de 2019. Los casos incidentes de VIH
llegaron a 10.930. Además, el tamizaje para el VIH en mujeres
embarazadas en América Latina alcanzó el 80%.
• En 2020 los casos incidentes de VIH fueron 12.528, y a
nivel mundial se produjeron casi 65.000 infecciones infantiles
debido a la ausencia de diagnóstico durante el embarazo.
• En marzo de 2021, ONUSIDA publicó la "Estrategia
mundial contra el sida 2021-2026".
• En 2021, la pandemia de COVID-19 afectó la tendencia
ascendente de casos incidentes de VIH. El MSPS publicó la guía
de práctica clínica para la atención de la infección por
VIH/sida en personas adultas, gestantes y adolescentes. ONUSIDA
estimó 38.4 millones de personas viviendo con VIH a nivel
mundial, y los casos incidentes de VIH disminuyeron a 9.210. El
INS notificó 17.647 casos nuevos de VIH en Colombia, un aumento
del 29,70% respecto a 2020. ONUSIDA reportó que el 82%
de las embarazadas con VIH tenían acceso a antirretrovirales.
También se publicó la "ETMI-PLUS Estrategia Nacional para la
Eliminación de la Transmisión Materno Infantil del VIH, Sífilis,
Hepatitis B y Enfermedad de Chagas, Colombia, 2019-2030".
• El periodo de reporte del 1 de febrero de 2021 al 31 de
enero de 2022 para el informe "Situación del VIH en Colombia
2022" mostró:
- 141.787 personas viviendo con VIH en el SGSSS.
- 12.919 casos nuevos de VIH diagnosticados, un aumento del
40.27%.
- Una incidencia estandarizada por la edad de 24,78 por
100.000 habitantes.
- 2.098 muertes por todas las causas en personas con VIH.
- La mortalidad general estandarizada por la edad disminuyó de
4,20 a 4,10 por cada 100.000 habitantes.
- Se identificaron 561.688 mujeres gestantes, con 1.129
diagnosticadas con VIH.
- Se reportaron 980 niños menores de 12 meses hijos de madres
con VIH, con 5 casos positivos.
- Se diagnosticaron 9.640 casos de TB activa, de los cuales
1.512 (15,68%) tenían coinfección con VIH.
- La proporción de gestantes tamizadas para VIH fue del
93,90%, sin alcanzar la meta del 95%.
- La proporción de menores de 6 meses con profilaxis postnatal
para VIH disminuyó del 4,10% al 77,30%.
- El costo promedio nacional anual de atención ambulatoria fue
de $5.33 millones, y el costo hospitalario promedio de
$17.02 millones.
- Se evidenció un descenso en la indetectabilidad de la carga
viral y una drástica disminución de la cobertura de la Terapia
Antirretroviral (TAR) en la población privada de la libertad (PPL).
• En 2022, ONUSIDA estimó que 39.0 millones de personas
vivían con el virus en todo el mundo, y el 81% de las
personas con TB en la región de las Américas conocían su estado
de VIH. El Instituto Nacional de Salud confirmó 18.766 pacientes
nuevos con VIH en Colombia.
• En marzo de 2023, la CAC publicó la "Actualización de
consenso basado en la evidencia: Indicadores mínimos para
evaluar la gestión del riesgo en las personas viviendo con VIH
atendidas en el marco del sistema de salud colombiano".
• En julio de 2023, se publicó "The U.S. Presidentʼs
Emergency Plan for AIDS Relief (PEPFAR)" por KKF.
• En noviembre de 2023, la OPS publicó "Epidemia de VIH y
respuesta en América Latina y el Caribe".
• El periodo de reporte del 1 de febrero de 2022 al 31 de
enero de 2023 para el informe "Situación del VIH en Colombia
2023" detalló:
- 165.405 personas viviendo con VIH en Colombia, un aumento del
16,66%.
- 14.670 casos incidentes diagnosticados, un aumento del
13,5%.
- El 34.46% de los casos incidentes fueron diagnosticados
en fase SIDA.
- La mediana del tiempo entre el diagnóstico y el inicio de la
TAR fue de 32 días.
- El 57.93% de los casos incidentes fueron diagnosticados
con un conteo de linfocitos T CD4+ menor a 350 CD4/mm³
(diagnóstico tardío).
- La prevalencia del VIH a nivel nacional fue del 0.33 por
100 habitantes.
- Se registraron 2.117 muertes por todas las causas en personas
con VIH; el 29% por complicaciones directas del VIH.
- La mortalidad general estandarizada fue de 4.08 por 100.000
habitantes.
- La tasa de letalidad aumentó al 3,64 muertes por 1.000
habitantes, un incremento del 34,81%.
- La cobertura de TAR en PVV reportadas fue del 83.49%,
una disminución del 4.86%.
- El 72.27% de PVV con TAR tenían carga viral
indetectable (< 50 copias/ml).
- El número de pacientes con falla viral disminuyó un 8.90%.
- Se informaron 535.470 mujeres gestantes, una disminución del
5.02%.
- Se diagnosticaron 1.168 mujeres con VIH durante la gestación.
- Se reportaron 1.002 niños menores de 12 meses hijos de madres
con VIH, con 7 casos positivos, lo que representa un
aumento del 40%.
- Se reportaron 13.301 casos de TB, un aumento del 37.97%.
- El 13.59% de los casos de TB tuvieron coinfección con
VIH.
- La oportunidad de tamización para VIH en TB activa fue de 3
días (mediana).
- La proporción de gestantes tamizadas para VIH fue del
91,58% (rango medio).
- La cobertura de TAR en gestantes con VIH fue del 73,27%
(desempeño bajo).
- La adherencia a las nuevas indicaciones terapéuticas de TAR
fue menor del 30%.
- La proporción de personas privadas de la libertad (PPL) con
detección temprana, realización de paraclínicos y supresión
viral siguió siendo inferior.
• En 2023, ONUSIDA estimó que 39.0 millones de personas
vivían con el virus en todo el mundo. También se publicó
"Viremia baja y las implicaciones en el control de los pacientes
VIH en tratamiento con antirretrovirales: scoping review".
En resumen, la cronología del VIH en Colombia refleja un
esfuerzo continuo para abordar la epidemia, con la promulgación
de leyes y resoluciones, el establecimiento de sistemas de
monitoreo como el de la CAC, y la implementación de guías de
atención. A pesar de logros significativos, como la reducción de
muertes relacionadas con el VIH a nivel global y regional, y un
aumento en la captación de casos prevalentes y la cobertura de
TAR en algunos periodos, persisten desafíos importantes,
especialmente en el diagnóstico tardío, la adherencia a nuevas
guías de tratamiento, la profilaxis de coinfecciones, y la
atención en poblaciones vulnerables como las privadas de la
libertad y las gestantes.
✔
VIH en Colombia: Situación y
Retos 2023
1. ¿Cuál es el panorama general de la situación del VIH en
Colombia para 2023, en comparación con años anteriores?
En 2023, Colombia registró 14.670 nuevos casos de VIH, lo que
representa un aumento del 13,55% en comparación con 2022 (12.919
casos). Esta cifra retoma la tendencia ascendente observada
entre 2012 y 2020, que se vio interrumpida en 2021 debido a la
pandemia de COVID-19, la cual afectó la notificación y detección
de nuevas infecciones. La prevalencia de personas que viven con
el VIH (PVV) también continuó su incremento, alcanzando 165.405
casos reportados en 2023, un aumento del 16,66% respecto a los
141.787 casos de 2022. A nivel mundial, ONUSIDA estima que 39
millones de personas vivían con el VIH en 2022, con 1.3 millones
de nuevas infecciones, mostrando un aumento en regiones como
Europa del Este, Asia, África del Norte y América Latina.
2. ¿Cómo se distribuye la población con VIH en Colombia según
características sociodemográficas y clínicas?
En Colombia, la epidemia del VIH se concentra principalmente en
hombres (78,48% de los casos prevalentes y 83,01% de los
incidentes) y en el grupo de edad de 25 a 39 años. La mediana de
edad para las PVV prevalentes fue de 38 años, siendo ligeramente
mayor en mujeres (41 años) que en hombres (37 años). Las
principales entidades territoriales con el mayor número de casos
incidentes y prevalentes son Bogotá, D.C., Antioquia y Valle del
Cauca, mientras que la región Central concentra la mayor
proporción de casos prevalentes.
Clínicamente, el 34,46% de los casos incidentes en 2023 fueron
diagnosticados en fase sida, lo que indica un diagnóstico
tardío. La principal vía de transmisión sigue siendo la sexual
(92,83% de los casos incidentes). Las comorbilidades más
frecuentes en las PVV prevalentes fueron otras infecciones de
transmisión sexual (3,35%) y discapacidad funcional (1,74%). Las
enfermedades definitorias de sida más comunes fueron el síndrome
de desgaste asociado al VIH (12,08%) y la tuberculosis pulmonar
o extrapulmonar (6,37%).
3. ¿Cuál es la situación de la mortalidad y letalidad por VIH
en Colombia?
En 2023, se registraron 2.117 muertes por todas las causas en
personas con VIH. De estas, el 29% fueron directamente
atribuidas a complicaciones del VIH, el 17,71% a otras
patologías no definitorias de sida y el 41,28% a causas
externas. La mortalidad general estandarizada fue de 4,08 por
100.000 habitantes, con una tasa más alta en hombres que en
mujeres. A nivel regional, Caribe, Central y Pacífica mostraron
las mayores tasas de mortalidad. La letalidad nacional por VIH
aumentó de 2,70 a 3,64 muertes por cada 1.000 PVV en 2023,
siendo mayor en mujeres (3,94 por 1.000 PVV) que en hombres
(3,56 por 1.000 PVV). La letalidad fue más alta en los grupos de
edad de 80 años y más.
4. ¿Cómo está la cobertura del tratamiento antirretroviral (TAR)
y la supresión viral en Colombia?
De las PVV prevalentes reportadas en 2023, el 83,49% estaba
recibiendo TAR, lo que cumple con el segundo indicador 95 de
ONUSIDA (95% de las PVV diagnosticadas con acceso a TAR). Sin
embargo, esto representa un ligero descenso en la cobertura en
comparación con 2022 (88,35%). Entre quienes recibían TAR, el
77,68% logró una carga viral indetectable (<50 copias/ml), y el
88,89% tuvo una carga viral suprimida (<1.000 copias/ml),
mostrando una ligera mejoría en la indetectabilidad respecto al
año anterior (75,98%).
A pesar de estos avances, existe un reto significativo en la
implementación de los esquemas de TAR recomendados por la Guía
de Práctica Clínica (GPC) de 2021, ya que la adherencia a las
nuevas indicaciones es inferior al 30% a nivel nacional y en los
regímenes contributivo y subsidiado. La mediana del tiempo entre
el diagnóstico y el inicio de la TAR fue de 32 días en 2023.
5. ¿Cuál es la situación de la transmisión materno-infantil (TMI)
del VIH en Colombia?
En 2023, se diagnosticaron 1.168 mujeres embarazadas con VIH, lo
que representa un aumento del 3,42% en comparación con 2022
(1.129 casos). El 95,12% de estas gestantes recibió TAR durante
el embarazo, y el 85,92% recibió antirretrovirales durante el
parto. La mediana de la edad gestacional al momento de la
detección del VIH fue de 14 semanas, más oportuna que en 2022
(16 semanas). El 72,35% de las gestantes con VIH tuvieron una
carga viral indetectable.
Se reportaron 1.002 niños menores de 12 meses hijos de madres
con VIH, de los cuales 7 resultaron positivos para el virus, un
aumento del 40% respecto al periodo anterior. Sin embargo, el
país cumple la meta de mantener la TMI por debajo del 2%. Se
identificó que el 1,40% de los niños expuestos no recibió
profilaxis antirretroviral posnatal, y el 3,49% no recibió
suministro de fórmula láctea.
6. ¿Cómo se aborda la coinfección de VIH y tuberculosis (TB)
en Colombia?
En 2023, se reportaron 13.301 casos de TB, un aumento del 37,97%
en comparación con 2022 (9.640 casos). De estos, el 13,59% tuvo
coinfección con VIH. La mediana de edad de los pacientes
coinfectados TB/VIH fue de 37 años. La mayoría de los casos de
TB coinfectada con VIH son hombres (80,59%) y se concentran en
el grupo de edad de 30 a 34 años. El 91,54% de los casos de TB
fueron sensibles a los medicamentos.
La cobertura del tratamiento para la TB activa en pacientes
coinfectados TB/VIH fue del 90,67%. El esquema antituberculoso
más frecuente fue Etambutol, Isoniazida, Pirazinamida,
Rifampicina (73,20%). La cobertura del TAR en pacientes con
coinfección TB/VIH aumentó al 88,23% en 2023. Sin embargo, se
reportó un 7,63% de fallecidos entre los coinfectados TB/VIH.
7. ¿Cuáles son los principales retos y áreas de mejora
identificadas en la gestión del riesgo del VIH en Colombia?
Uno de los principales desafíos es la detección tardía de la
infección por VIH, con un porcentaje significativo de casos
incidentes diagnosticados en fase sida. Es crucial aumentar la
oferta de pruebas de tamizaje y autotests para mejorar el acceso
al diagnóstico. La adherencia a las nuevas GPC para la
prescripción de TAR es baja (menos del 30%), lo que indica la
necesidad de fortalecer la implementación de estas
recomendaciones.
Además, la cobertura de profilaxis para infecciones oportunistas
como Mycobacterium avium complex (MAC) y Pneumocystis jirovecii
es inferior a lo esperado, y se requiere mayor especificidad en
la justificación médica para ciertas prescripciones. La calidad
del reporte de información, aunque ha mejorado, aún presenta
inconsistencias en la validación de diagnósticos y en la
disponibilidad de soportes clínicos.
8. ¿Qué grupos de población requieren mayor atención y
estrategias específicas en la respuesta al VIH?
Los hombres que tienen relaciones sexuales con otros hombres (HSH)
representan la mayor proporción de casos incidentes (53,65%) y
prevalentes (46,71%) dentro de las poblaciones clave,
requiriendo estrategias de prevención y detección focalizadas.
Los consumidores de sustancias psicoactivas también son un grupo
importante a considerar.
La población privada de la libertad (PPL) y las personas no
afiliadas al sistema de salud muestran resultados
significativamente inferiores en indicadores clave como la
detección temprana, realización de paraclínicos, cobertura de
TAR y supresión viral. Estas poblaciones enfrentan barreras
socioeconómicas, geográficas y culturales, así como la
fragmentación de la atención en salud, lo que subraya la
necesidad de intervenciones específicas y fortalecimiento del
sistema de salud penitenciario. Las gestantes con VIH también
requieren atención continua para garantizar la profilaxis
postnatal universal y el suministro de fórmula láctea para sus
hijos.
9. ¿Cuál la situación de 1º de febrero de 2021 y el 31 de
enero de 2022?
En el periodo comprendido entre el 1º de febrero de 2021
y el 31
de enero de 2022, de las personas viviendo con VIH con
tratamiento antirretroviral, el 78,12% presentó una carga viral
menor de 50 copias/mL y en el 87,60% fue menor a 1.000 copias/mL.
La cobertura de
tratamiento antirretroviral en las PVV fue del 88,35 %
presentando una disminución del
3,46% con respecto al periodo anterior. La región Caribe tuvo la
mayor cobertura con un 90,33% de personas recibiendo TAR. Se
presentó mayor cobertura de terapia antirretroviral en el
régimen de excepción (89,59%), seguido por el contributivo
(89,32%).
10. ¿Cuál Tenofovir fue el
más usado según el Informe de la Cuenta de Alto Costo de 2022
En
esta imagen, de 21 esquemas
de tratamiento antirretroviral
reportados con mayor frecuencia en las PVV incidentes
Colombia 2022, 14 incluyen
TENOFOVIR, sin que se sepa si
corresponden a TENOFOVIR ALAFENAMIDA (con patente
vigente en 2022) o TENOFOVIR DISOPROXIL Fumarato (sin patente vigente)
La Importancia de diferenciar TENOFOVIR
Disoproxil
de TENOFOVIR
Alafenamida
En la Tabla 28 del informe
Situación del VIH en Colombia 2022
de la Cuenta de Alto costo, el TENOFOVIR aparece como el
medicamento más reportado en las PVV Colombia 2022. No se
precisa cuánto corresponde a TENOFOVIR ALAFENAMIDA o TENOFOVIR DISOPROXIL
Fumarato, pese a que esta diferencia no es menor
Gráfico N°24: El informe "Situación del VIH en
Colombia 2022" muestra TENOFOVIR como el medicamento más
reportado en las PVV

En
esta tabla puede verse que TENOFOVIR es la molécula más
importante entre los medicamentos reportados en las PVV,
Colombia 2022, pero no se aclara cuánto corresponde a cuál Tenofovir, Tenofovir Alafenamida con protección de patente vigente
o Tenofovir Disoproxil fumarato con protección de
patente vencida.
3.2.
3.2.
Situación del
VIH-SIDA en Colombia según Guías de Práctica Clínica de 2021 y
2024
La siguiente cronología
proporciona recomendaciones basadas en evidencia sobre la
prevención del VIH, el diagnóstico en adultos, adolescentes,
niños y gestantes, y el manejo del tratamiento y el seguimiento.
La GPC también aborda aspectos como la terapia antirretroviral (TAR),
la monitorización de la carga viral, la profilaxis contra
infecciones oportunistas y las estrategias de vacunación,
siempre considerando la realidad epidemiológica y de costos en
Colombia para optimizar la atención integral a las personas que
viven con VIH. Ver Enlaces:
•
https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/VS/PP/ET/gpc-vih-adultos-version-profesionales-salud.pdf
ARMI.
•
https://www.minsalud.gov.co/sites/rid/Lists/BibliotecaDigital/RIDE/VS/PP/ET/via-clinica-vih-2024.pdf
ARMI
✔
Resumen Audio de Guías de
Práctica Clínica:
VIH_en_Colombia_La_Revolución_del_Tratamiento_Antirretroviral,_de_la_Inmediatez_a_la_Supresión_Viral.m4a
✔
Resumen Video de
Guía de Práctica Clínica (2021):
VIH_Guía_de_Práctica_Clínica_en_Colombia.mp4
✔
Resumen Video de
Vía del IETS (2024):
Vía_Clínica_VIH_2024__Claves_para_Colombia.mp4
Importante:
NoteBookLM aún no es perfecto. Si encuentra inconsistencias por
favor infórmenos al correo
andiarey.samaytatiana@gmail.com
✔
Cronología VIH en Colombia
en relación con Guías de
Práctica Clínica
•
Pre-1947: Inició la indexación de artículos biomédicos en
PubMed de la Biblioteca Nacional de Medicina de Estados Unidos,
que incluye citas de MEDLINE y otras publicaciones de ciencias
de la vida.
•
1986: Se observó una disminución en la proporción de
casos de SIDA notificados en Colombia desde este año, con un
aumento simultáneo en la notificación de casos en estadio VIH.
También se estableció una clasificación para infecciones
oportunistas, incluyendo la categoría IV C1 para el SIDA.
•
1987: Se definió el caso de SIDA, abarcando las primeras
23 clasificaciones.
•
1991: Se promulgó la Constitución Política de Colombia,
que en su artículo 49 establece la atención de la salud y el
saneamiento ambiental como servicios públicos a cargo del
Estado, garantizando el acceso a los servicios de promoción,
protección y recuperación de la salud.
•
1993: Se introdujo la categoría C en la clasificación del
SIDA.
•
1995: Se incorporaron nuevos medicamentos
antirretrovirales con mecanismos de acción novedosos, logrando
por primera vez la supresión sostenida de la carga viral del VIH
en plasma. Esto sentó las bases de una filosofía de manejo
antirretroviral temprano y agresivo.
•
2000: El Ministerio de Salud emitió la Resolución Número
412, la cual establece actividades, procedimientos e
intervenciones de cumplimiento obligatorio para la protección
específica y detección temprana de enfermedades de interés en
salud pública, incluyendo el VIH y los laboratorios obligatorios
en el control prenatal.
•
2002: La razón hombre/mujer de casos de VIH/SIDA en
Colombia, sin diferenciación por estadio, se mantuvo constante
hasta 2013, con un promedio de 2,3 hombres por cada mujer.
•
2003: Naciones Unidas/ONUSIDA publicó "El VIH/SIDA y los
derechos humanos". El Acuerdo 245 de 2003 reconoció el VIH/SIDA
como una patología de alto costo.
•
2004-2014: Durante este período, se realizaron estudios
que evaluaron la mortalidad temprana y tardía, así como la
pérdida de seguimiento en pacientes atendidos en clínicas
urbanas especializadas en VIH.
•
2005: Se promulgó la Ley 972 de 2005. Además, ONUSIDA
creó la metodología de Medición del Gasto en SIDA (MEGAS),
conocida en inglés como National AIDS Spending Assessment
(NASA), para identificar los flujos de recursos destinados a
financiar las respuestas nacionales frente a la epidemia del
VIH.
•
2006: Este año marcó varios hitos importantes en
Colombia:
- Se publicó la primera guía oficial del Ministerio de la
Protección Social para el manejo del VIH, que incorporó la
tecnología de pruebas de resistencia y consideraciones para el
manejo de la enfermedad.
- Se adoptaron Guías de Práctica Clínica (GPC) basadas en
evidencia para la prevención, diagnóstico y tratamiento de
pacientes con VIH/SIDA y Enfermedad Renal Crónica, mediante la
Resolución 3442 de 2006.
- Se creó y reglamentó el Sistema de Vigilancia en Salud Pública
(SIVIGILA) a través del Decreto 3518 de 2006.
- La Asociación Colombiana de Infectología (ACIN) publicó la
"Guía de práctica clínica de VIH/SIDA. Recomendaciones basadas
en la evidencia".
- El Ministerio de Salud emitió la Circular No. 0063.
•
2011: Se estimó que 157.500 personas vivían con VIH en
Colombia, con aproximadamente 10.159 nuevas infecciones en 2013.
•
2012: Se observó una disminución de tres puntos
porcentuales en la Transmisión Materno-Infantil (TMI) del VIH
entre 2013 y 2018. La Resolución 016 de 2012 definió los
lineamientos para la Estrategia de Eliminación de la TMI del
VIH. También se realizaron talleres en Sudáfrica para explorar
la percepción sobre la terapia antirretroviral (TAR) en salud
materna e infantil. El Ministerio de Salud y UNFPA encargaron a
ACIN el desarrollo de una GPC.
•
2013: Se publicó la Resolución NÚMERO 00002338 DE 2013,
relacionada con la realización de pruebas rápidas para VIH.
•
2014: Se publicó la "Guía Metodológica para la
elaboración de Guías de Práctica Clínica con Evaluación
Económica en el Sistema General de Seguridad Social en Salud
Colombiano". La GPC-VIH 2014 es referenciada en varios
documentos.
•
2015: Se publicó la Encuesta Nacional de Demografía y
Salud, utilizada para la construcción de la Hoja de Ruta para la
Prevención Combinada del VIH/SIDA en Colombia. Se evaluó la
costo-efectividad de Tenofovir/Emtricitabina. La Resolución 5593
de 2015 también fue publicada. La Resolución 1912 de 2015 fue
mencionada para el ajuste del punto de corte para el diagnóstico
temprano del VIH.
•
2016: Se publicaron herramientas metodológicas como
ROBINS-I y los marcos GRADE Evidence to Decision (EtD). Las
guías para la profilaxis post-exposición antirretroviral en EE.
UU. fueron actualizadas. La Organización Panamericana de la
Salud (OPS) publicó el Plan de Acción para la prevención y el
control de la infección por el VIH y las ITS 2016-2021. La
Resolución 3280 de 2018 del Minsalud estipula poblaciones
vulnerables para las pruebas de VIH.
•
Febrero 2017 - Enero 2018: Un informe de la Cuenta de
Alto Costo (CAC) indicó que la prevalencia de VIH en menores de
13 años en Colombia fue de 0.05 casos por cada 1.000 menores.
•
2017: Se estableció la Coalición Global de Prevención del
VIH/SIDA (GPC). Se renovaron las guías de atención de VIH/SIDA
en Colombia por el MSPS. El Protocolo para la atención por
exposición de riesgo biológico laboral o no laboral fue
publicado. La TMI del VIH en 2017 fue del 2.2%.
•
2018: El porcentaje neto de TMI VIH en Colombia fue del
1.7%. La OPS publicó el "Marco de monitoreo de los servicios
relacionados con el VIH y las ITS para grupos de población clave
en América Latina y el Caribe". "El Proceso de Quito" fue
iniciado en septiembre.
•
2019: ONUSIDA informó que en Colombia vivían 190.000
personas mayores de 15 años con VIH, con una prevalencia
nacional del 0.5%. La Resolución 273 de 2019 estableció
disposiciones para el reporte de información a la Cuenta de Alto
Costo.
•
Marzo 2020: El documento de consenso de GeSIDA para la
evaluación y el tratamiento de las enfermedades renales en
pacientes con VIH fue publicado.
•
Julio 2020: Se publicaron las escalas clínicas aplicables
en personas con VIH y un documento de consenso sobre el manejo
clínico de la comorbilidad neuropsiquiátrica y cognitiva
asociada a VIH-1.
•
Octubre 2020: Se publicó un documento de consenso sobre
Teleconsulta (TC) con personas que viven con VIH.
•
Enero 2021: Se realizó la trazabilidad de la asistencia
al panel para la dimensión de diagnóstico en la GPC.
•
25 de Enero de 2021: Se recomendó la valoración semestral
por parte del químico farmacéutico para niños y niñas con VIH.
•
Febrero 2021: Se publicaron los indicadores de calidad
asistencial de GeSIDA para la atención de personas que viven con
VIH.
•
9 de Febrero de 2021: Se sugirió la inclusión de un
ginecólogo y obstetra en el equipo interdisciplinario para el
caso de niñas o adolescentes gestantes con VIH.
•
16 de Febrero de 2021: Se recomendó la evaluación
metabólica en la valoración nutricional de niños, niñas y
adolescentes con VIH, y la realización de pruebas de genotipo
para evaluar los genes de resistencia antirretroviral en casos
de falla virológica.
•
2021: Se publicaron las Guías de Práctica Clínica (GPC)
actualizadas para la atención de la infección por VIH/SIDA en
personas adultas, gestantes y adolescentes, así como una guía
específica para niñas, niños y adolescentes. El Ministerio de
Salud y Protección Social también publicó la "Vía Clínica para
la prevención, diagnóstico, tratamiento y seguimiento de
personas viviendo con VIH". La prevalencia del VIH en la
población general de Colombia se estimó en 0.6%. El esquema TDF/3TC/DTG
fue identificado como primera elección de tratamiento. Se aprobó
el registro sanitario INVIMA 2021M-0020165 para Dolutegravir (DTG)/Lamivudina
(3TC). Se actualizó el documento sobre Prevención y Tratamiento
de infecciones oportunistas y otras coinfecciones.
•
2022: El "Informe de evento VIH, SIDA y muerte por SIDA,
2022" del Instituto Nacional de Salud (INS) reportó 19.183 casos
de VIH en Colombia, con una tasa de incidencia de 36.3 casos por
100.000 habitantes. La prevalencia de VIH en gestantes fue del
0.15% y en personas privadas de la libertad del 0.5%. El Decreto
441 de 2022 eliminó los procesos de autorización para la
atención del VIH. El Plan Nacional de Respuesta ante las ITS, el
VIH, la Coinfección TB/VIH y las Hepatitis B y C 2022-2025 fue
publicado. El Protocolo de Vigilancia VIH/SIDA (código 850) se
actualizó.
•
2023: El Fondo Colombiano de Enfermedades de Alto Costo,
Cuenta de Alto Costo (CAC) publicó la "Situación del VIH en
Colombia, 2023" que cubre el período del 1 de febrero de 2022 al
31 de enero de 2023. Se publicaron varios documentos de consenso
y guías relacionadas con el seguimiento de la infección,
estudios de resistencia y profilaxis.
•
2024: Se publicó el Protocolo de Vigilancia de VIH/SIDA
(Código 850, Versión 08). La "Vía Clínica para la prevención,
diagnóstico, tratamiento y seguimiento de personas viviendo con
VIH" fue publicada en junio de 2024 por el Ministerio de Salud y
Protección Social y el IETS. La "Hoja de Ruta para la Prevención
Combinada del VIH/SIDA en Colombia 2024-2025" fue emitida en
octubre de 2024. También se publicó un Protocolo para la
atención por exposición de riesgo biológico. La Cuenta de Alto
Costo (CAC) publicó la "Situación del VIH en Colombia 2024", que
cubre el período del 1 de febrero de 2023 al 31 de enero de
2024.
•
2025 (Proyectado): Se espera la publicación de varios
documentos de consenso sobre inmunización en adultos con VIH,
lactancia materna en recién nacidos expuestos al VIH, y
profilaxis post-exposición. También se mencionan noticias en
agosto de 2025 relacionadas con el VIH y su atención.
La Hoja de Ruta para la Prevención Combinada del VIH/Sida en
Colombia 2024-2025 es un esfuerzo integral y colaborativo
del Ministerio de Salud y Protección Social, buscando optimizar
los logros del país y generar nuevas estrategias para una
respuesta más efectiva y eficiente en la reducción de nuevas
infecciones, alineada con las metas de ONUSIDA para 2025. Se ha
enfatizado la importancia de un diagnóstico temprano y el
inicio oportuno del tratamiento antirretroviral para
reducir las infecciones oportunistas y la mortalidad por
VIH/SIDA. El manejo interdisciplinario de los pacientes
con VIH es una recomendación clave en las guías.
|
En síntesis, intentará obtener
conclusiones a partir de un proceso de Validación,
Analítica e Integración (VAI) de datos to
|
3.3.
3.3.
Situación del
VIH-SIDA en Colombia según el IETS y SIVIGILA del INS de 2022 a
2024
La información de resultados en salud que aparece en los
informes de la Cuenta de Alto Costo debe necesariamente
complementarse con los informes epidemiológicos de SIVIGILA del
Instituto Nacional de Salud. Mostramos a continuación dos
ejemplos de los contenidos que deberían relacionarse para
optimizar la pertinencia en el uso de recursos del sistema de
salud, que siempre serán escasos.
✔
Situación VIH SIDA en Colombia
según IETS, INS y SIVIGILA:
VIH_en_Colombia__Guías,_Fármacos_Clave_y_el_Desafío_del_Acceso_Real.m4a
✔
VIH SIDA en Colombia según IETS,
INS y SIVIGILA:
VIH_en_Colombia__La_Cruda_Realidad,_Tratamientos_y_la_Batalla_por_el_Acceso_al_Dolutegravir.m4a
Importante:
NoteBookLM aún no es perfecto. Si encuentra inconsistencias por
favor infórmenos al correo
andiarey.samaytatiana@gmail.com
✔
Cronología VIH en Colombia
según informes del IETS y SIVIGILA del INS
Previo a 2004:
•
Se inician esfuerzos de vigilancia del VIH/SIDA en Colombia. El
Instituto Nacional de Salud (INS) registra informes de eventos
de VIH-SIDA desde al menos 2004, aunque con un menor número de
informes en los primeros años.
2004:
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Cólera, Dengue, Difteria, Encefalitis
Equina, Fiebre Amarilla, Hepatitis B y C, IRA, Intoxicaciones,
Leishmaniasis, Lepra, Malaria, Meningitis, Mortalidad Perinatal
y Neonatal, Parálisis Flácida Aguda, Parotiditis, Tos Ferina,
Tuberculosis, Varicela.
2005:
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Dengue, Leishmaniasis, Lepra, Malaria,
Mortalidad Materna, Parálisis Flácida Aguda, Rabia, Sarampión y
Rubéola, Sífilis Gestacional y Congénita, Síndrome de Rubéola
Congénita, Tétanos Accidental.
2006:
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Cólera, Dengue, Fiebre Amarilla,
Leishmaniasis, Lepra, Lesiones por Artefactos Explosivos,
Malaria, Sarampión y Rubéola, Sífilis Gestacional y Congénita,
Síndrome de Rubéola Congénita, Tétanos Accidental.
2007:
•
El INS registra 1 informe de evento de VIH-SIDA. El único otro
evento registrado es Mortalidad Perinatal y Neonatal.
2008:
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Cáncer en menores de 18 años, Cólera,
Defectos Congénitos, Dengue, Difteria, Enfermedad Diarreica
Aguda, Enfermedades Transmitidas por Alimentos, Evento Adverso
Grave Posterior a la Vacunación, Fiebre Amarilla, Fiebre
Tifoidea y Paratifoidea, Hepatitis B y C, Intoxicaciones,
Leptospirosis, Lesiones por Artefactos Explosivos, Malaria,
Meningitis, Parálisis Flácida Aguda, Parotiditis, Rabia, Sífilis
Gestacional y Congénita, Síndrome de Rubéola Congénita, Tos
Ferina, Varicela.
2009:
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Cáncer en menores de 18 años, Dengue,
Difteria, Enfermedad Diarreica Aguda, Enfermedades Transmitidas
por Alimentos, Evento Adverso Grave Posterior a la Vacunación,
Fiebre Amarilla, Fiebre Tifoidea y Paratifoidea, Infección
Respiratoria Aguda, Intoxicaciones, Leishmaniasis, Lepra,
Leptospirosis, Malaria, Meningitis, Mortalidad Perinatal y
Neonatal, Parálisis Flácida Aguda, Parotiditis, Rabia, Sarampión
y Rubéola, Tos Ferina, Tuberculosis, Varicela.
2010:
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Cólera, Dengue, Difteria, Enfermedad
Diarreica Aguda, Enfermedades Transmitidas por Alimentos, Evento
Adverso Grave Posterior a la Vacunación, Fiebre Amarilla, Fiebre
Tifoidea y Paratifoidea, Hepatitis B y C, Infección Respiratoria
Aguda, Intoxicaciones, Leishmaniasis, Lepra, Leptospirosis,
Malaria, Meningitis, Parálisis Flácida Aguda, Parotiditis,
Rabia, Sarampión y Rubéola, Sífilis Gestacional y Congénita,
Síndrome de Rubéola Congénita, Tétanos Accidental, Tos Ferina,
Tuberculosis, Varicela.
•
13 de agosto de 2010: Se crea la versión 2 del "Protocolo de
vigilancia en salud pública VIH/SIDA" del Instituto Nacional de
Salud, con Diana Landaeta como referente de vigilancia de
hepatitis B y parte del Equipo Funcional Infecciones de
Transmisión Sexual.
2011:
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Cáncer en menores de 18 años, Cólera,
Defectos Congénitos, Dengue, Difteria, Enfermedad Diarreica
Aguda, Enfermedades Transmitidas por Alimentos, Evento Adverso
Grave Posterior a la Vacunación, Fiebre Amarilla, Fiebre
Tifoidea y Paratifoidea, Hepatitis B y C, Infección Respiratoria
Aguda, Intoxicaciones, Leishmaniasis, Lepra, Leptospirosis,
Lesiones por Artefactos Explosivos, Malaria, Meningitis,
Mortalidad Materna, Mortalidad Perinatal y Neonatal, Parálisis
Flácida Aguda, Parotiditis, Rabia, Sarampión y Rubéola, Sífilis
Gestacional y Congénita, Síndrome de Rubéola Congénita, Tétanos
Accidental, Tos Ferina, Tuberculosis, Varicela.
2012:
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Cáncer en menores de 18 años, Cólera,
Defectos Congénitos, Dengue, Difteria, Enfermedad Diarreica
Aguda, Enfermedades Transmitidas por Alimentos, Evento Adverso
Grave Posterior a la Vacunación, Fiebre Amarilla, Fiebre
Tifoidea y Paratifoidea, Hepatitis B y C, Infección Respiratoria
Aguda, Infecciones Asociadas a Dispositivos (IAD), Infecciones
Asociadas a la Atención en Salud - Consumo de Antibióticos,
Intoxicaciones, Leishmaniasis, Lepra, Leptospirosis, Lesiones
por Artefactos Explosivos, Malaria, Meningitis, Mortalidad
Materna, Mortalidad Perinatal y Neonatal, Parálisis Flácida
Aguda, Parotiditis, Rabia, Sarampión y Rubéola, Sífilis
Gestacional y Congénita, Síndrome de Rubéola Congénita, Tétanos
Accidental, Tos Ferina, Tuberculosis, Tuberculosis
Farmacorresistente, Varicela.
2013:
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Bajo Peso al Nacer,
Cáncer en menores de 18 años, Chagas, Cólera, Defectos
Congénitos, Dengue, Desnutrición en menores de 5 años, Difteria,
Enfermedad Diarreica Aguda, Enfermedades Transmitidas por
Alimentos, Evento Adverso Grave Posterior a la Vacunación,
Exposición a Flúor (suspendido temporalmente), Fiebre Amarilla,
Fiebre Tifoidea y Paratifoidea, Hepatitis B y C, Infección
Respiratoria Aguda, Infecciones Asociadas a Dispositivos (IAD),
Infecciones Asociadas a la Atención en Salud - Consumo de
Antibióticos, Intoxicaciones, Leishmaniasis, Lepra,
Leptospirosis, Lesiones por Artefactos Explosivos, Malaria,
Meningitis, Morbilidad Materna Extrema, Mortalidad Materna,
Mortalidad Perinatal y Neonatal, Parálisis Flácida Aguda,
Parotiditis, Rabia, Sarampión y Rubéola, Sífilis Gestacional y
Congénita, Síndrome de Rubéola Congénita, Tétanos Accidental,
Tos Ferina, Tuberculosis, Tuberculosis Farmacorresistente,
Varicela.
2014:
•
11 de junio de 2014: Se complementan las acciones específicas
para la vigilancia de VIH/SIDA y muerte por SIDA en el protocolo
del INS, con la adición de definiciones del decreto 3518 e
indicadores. Norma C. Cuéllar Espitia es la Líder del Equipo
Funcional ITS.
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Bajo Peso al Nacer,
Cáncer en menores de 18 años, Chagas, Chikungunya, Cólera,
Defectos Congénitos, Dengue, Desnutrición en menores de 5 años,
Difteria, Enfermedad Diarreica Aguda, Enfermedades Transmitidas
por Alimentos, Evento Adverso Grave Posterior a la Vacunación,
Exposición a Flúor (suspendido temporalmente), Fiebre Amarilla,
Fiebre Tifoidea y Paratifoidea, Hepatitis B y C, Infección
Respiratoria Aguda, Infecciones Asociadas a Dispositivos (IAD),
Infecciones Asociadas a la Atención en Salud - Consumo de
Antibióticos, Intoxicaciones, Leishmaniasis, Lepra,
Leptospirosis, Lesiones por Artefactos Explosivos, Malaria,
Meningitis, Morbilidad Materna Extrema, Mortalidad Materna,
Mortalidad Perinatal y Neonatal, Parálisis Flácida Aguda,
Parotiditis, Rabia, Sarampión y Rubéola, Sífilis Gestacional y
Congénita, Síndrome de Rubéola Congénita, Tétanos Accidental,
Tos Ferina, Tuberculosis, Tuberculosis Farmacorresistente,
Varicela.
2015:
•
10 de marzo de 2015: Se realiza un cambio en los algoritmos
diagnósticos del protocolo del INS. Norma C. Cuéllar Espitia
sigue como Líder del Equipo Funcional ITS.
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Bajo Peso al Nacer,
Cáncer en menores de 18 años, Chagas, Chikungunya, Cólera,
Defectos Congénitos, Dengue, Desnutrición en menores de 5 años,
Difteria, Enfermedad Diarreica Aguda, Enfermedades Transmitidas
por Alimentos, Evento Adverso Grave Posterior a la Vacunación,
Exposición a Flúor (suspendido temporalmente), Fiebre Amarilla,
Fiebre Tifoidea y Paratifoidea, Hepatitis B y C, Infección
Respiratoria Aguda, Infecciones Asociadas a Dispositivos (IAD),
Infecciones Asociadas a la Atención en Salud - Consumo de
Antibióticos, Intoxicaciones, Lepra, Leptospirosis, Lesiones por
Artefactos Explosivos, Malaria, Meningitis, Morbilidad Materna
Extrema, Mortalidad Perinatal y Neonatal, Parálisis Flácida
Aguda, Parotiditis, Rabia, Sarampión y Rubéola, Sífilis
Gestacional y Congénita, Síndrome de Rubéola Congénita, Tétanos
Accidental, Tos Ferina, Tuberculosis, Tuberculosis
Farmacorresistente, Varicela, Violencia de Género.
2016:
•
30 de septiembre de 2016: Se actualizan las estadísticas
mundiales y nacionales, y se ajustan las definiciones de la
ficha 850 y las acciones individuales en el protocolo del INS.
Norma C. Cuéllar Espitia continúa como Líder del Equipo
Funcional ITS.
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Bajo Peso al Nacer,
Cáncer de Mama y Cuello Uterino, Cáncer en menores de 18 años,
Chagas, Chikungunya, Defectos Congénitos, Dengue, Desnutrición
en menores de 5 años, Difteria, Encefalitis Equina, Enfermedad
Diarreica Aguda, Enfermedades Huérfanas - Raras, Enfermedades
Transmitidas por Alimentos, Evento Adverso Grave Posterior a la
Vacunación, Exposición a Flúor (suspendido temporalmente),
Fiebre Amarilla, Fiebre Tifoidea y Paratifoidea, Hepatitis A,
Hepatitis B y C, Infección Respiratoria Aguda, Infecciones
Asociadas a la Atención en Salud - Consumo de Antibióticos,
Intento de Suicidio, Intoxicaciones, Leishmaniasis, Lepra,
Leptospirosis, Lesiones de Causa Externa, Lesiones por
Artefactos Explosivos, Malaria, Meningitis, Morbilidad Materna
Extrema, Mortalidad en menores de 5 años, Mortalidad Materna,
Mortalidad Perinatal y Neonatal, Parálisis Flácida Aguda,
Parotiditis, Rabia, Sarampión y Rubéola, Sífilis Gestacional y
Congénita, Síndrome de Rubéola Congénita, Tétanos Accidental,
Tos Ferina, Tuberculosis, Tuberculosis Farmacorresistente,
Varicela, Violencia de Género, Zika.
2017:
•
30 de mayo de 2017: Actualización general del protocolo del INS.
Norma C. Cuéllar Espitia sigue siendo la Líder del Equipo
Funcional ITS.
•
22 de noviembre de 2017: Revisión y actualización del protocolo
del INS. Norma C. Cuéllar Espitia continúa como Líder del Equipo
Funcional ITS.
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Bajo Peso al Nacer,
Cáncer de Mama y Cuello Uterino, Cáncer en menores de 18 años,
Chagas, Chikungunya, Defectos Congénitos, Dengue, Desnutrición
en menores de 5 años, Difteria, Encefalitis Equina, Enfermedad
Diarreica Aguda, Enfermedades Huérfanas - Raras, Enfermedades
Transmitidas por Alimentos, Evento Adverso Grave Posterior a la
Vacunación, Exposición a Flúor (suspendido temporalmente),
Fiebre Amarilla, Fiebre Tifoidea y Paratifoidea, Hepatitis A,
Hepatitis B y C, Infección Respiratoria Aguda, Infecciones
Asociadas a Dispositivos (IAD), Infecciones Asociadas a la
Atención en Salud - Consumo de Antibióticos, Infecciones
Asociadas a Procedimientos Médico Quirúrgicos (IAPMQ), Intento
de Suicidio, Intoxicaciones, Leishmaniasis, Lepra, Leptospirosis,
Lesiones de Causa Externa, Lesiones por Artefactos Explosivos,
Malaria, Meningitis, Morbilidad Materna Extrema, Mortalidad en
menores de 5 años, Mortalidad Materna, Mortalidad Perinatal y
Neonatal, Parálisis Flácida Aguda, Parotiditis, Rabia, Sarampión
y Rubéola, Sífilis Gestacional y Congénita, Síndrome de Rubéola
Congénita, Tétanos Accidental, Tétanos Neonatal, Tos Ferina,
Tuberculosis, Tuberculosis Farmacorresistente, Varicela,
Violencia de Género, Zika.
2018:
•
Inicia el periodo de estudio para la carga de enfermedad por
VIH/SIDA en los departamentos de Colombia (2018-2022).
•
Colombia se une a "El Proceso de Quito" en septiembre de 2018,
una iniciativa para fortalecer la coordinación regional y la
cooperación para mejorar la protección de los derechos de las
personas refugiadas y migrantes venezolanas, incluyendo el
acceso a servicios de salud como la terapia antirretroviral (TARV).
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Bajo Peso al Nacer,
Cáncer de Mama y Cuello Uterino, Cáncer en menores de 18 años,
Chagas, Chikungunya, Defectos Congénitos, Dengue, Desnutrición
en menores de 5 años, Difteria, Encefalitis Equina, Enfermedad
Diarreica Aguda, Enfermedades Huérfanas - Raras, Enfermedades
Transmitidas por Alimentos, Evento Adverso Grave Posterior a la
Vacunación, Exposición a Flúor (suspendido temporalmente),
Fiebre Amarilla, Fiebre Tifoidea y Paratifoidea, Hepatitis A,
Hepatitis B y C, Infección Respiratoria Aguda, Infecciones
Asociadas a Dispositivos (IAD), Infecciones Asociadas a la
Atención en Salud - Consumo de Antibióticos, Infecciones
Asociadas a Procedimientos Médico Quirúrgicos (IAPMQ), Intento
de Suicidio, Intoxicaciones, Leishmaniasis, Lepra, Leptospirosis,
Lesiones de Causa Externa, Lesiones por Artefactos Explosivos,
Malaria, Meningitis, Morbilidad Materna Extrema, Mortalidad en
menores de 5 años, Mortalidad Materna, Mortalidad Perinatal y
Neonatal, Parálisis Flácida Aguda, Parotiditis, Rabia, Sarampión
y Rubéola, Sífilis Gestacional y Congénita, Síndrome de Rubéola
Congénita, Tétanos Accidental, Tétanos Neonatal, Tos Ferina,
Tracoma, Tuberculosis, Tuberculosis Farmacorresistente,
Varicela, Violencia de Género, Zika.
2019:
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Bajo Peso al Nacer,
Cáncer en menores de 18 años, Chagas, Chikungunya, Defectos
Congénitos, Dengue, Desnutrición en menores de 5 años, Difteria,
Encefalitis Equina, Enfermedad Diarreica Aguda, Enfermedades
Huérfanas - Raras, Enfermedades Transmitidas por Alimentos,
Evento Adverso Grave Posterior a la Vacunación, Exposición a
Flúor (suspendido temporalmente), Fiebre Amarilla, Fiebre
Tifoidea y Paratifoidea, Hepatitis A, Hepatitis B y C, Infección
Respiratoria Aguda, Infecciones Asociadas a Dispositivos (IAD),
Infecciones Asociadas a la Atención en Salud - Consumo de
Antibióticos, Infecciones Asociadas a Procedimientos Médico
Quirúrgicos (IAPMQ), Intento de Suicidio, Intoxicaciones,
Leishmaniasis, Lepra, Leptospirosis, Lesiones de Causa Externa,
Lesiones por Artefactos Explosivos, Malaria, Meningitis,
Morbilidad Materna Extrema, Mortalidad en menores de 5 años,
Mortalidad Materna, Mortalidad Perinatal y Neonatal, Parálisis
Flácida Aguda, Parotiditis, Rabia, Sarampión y Rubéola, Sífilis
Gestacional y Congénita, Síndrome de Rubéola Congénita, Tétanos
Accidental, Tétanos Neonatal, Tos Ferina, Tracoma, Tuberculosis,
Tuberculosis Farmacorresistente, Violencia de Género.
2020:
•
A finales de 2020: Aproximadamente 37.7 millones de personas
vivían con VIH (PVVIH) en todo el mundo, según ONUSIDA.
•
El INS registra 1 informe de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Bajo Peso al Nacer,
Cáncer en menores de 18 años, Chagas, Chikungunya, Defectos
Congénitos, Dengue, Desnutrición en menores de 5 años, Difteria,
Encefalitis Equina, Enfermedad Diarreica Aguda, Enfermedades
Huérfanas - Raras, Enfermedades Transmitidas por Alimentos,
Evento Adverso Grave Posterior a la Vacunación, Exposición a
Flúor (suspendido temporalmente), Fiebre Amarilla, Fiebre
Tifoidea y Paratifoidea, Hepatitis A, Hepatitis B y C, Infección
Respiratoria Aguda, Infecciones Asociadas a Dispositivos (IAD),
Infecciones Asociadas a la Atención en Salud - Consumo de
Antibióticos, Infecciones Asociadas a Procedimientos Médico
Quirúrgicos (IAPMQ), Intento de Suicidio, Intoxicaciones,
Leishmaniasis, Lepra, Leptospirosis, Lesiones de Causa Externa,
Lesiones por Artefactos Explosivos, Malaria, Meningitis,
Morbilidad Materna Extrema, Mortalidad en menores de 5 años,
Mortalidad Materna, Mortalidad Perinatal y Neonatal, Parálisis
Flácida Aguda, Parotiditis, Rabia, Sarampión y Rubéola, Sífilis
Gestacional y Congénita, Síndrome de Rubéola Congénita, Tétanos
Accidental, Tétanos Neonatal, Tos Ferina, Tracoma, Tuberculosis,
Tuberculosis Farmacorresistente, Varicela, Violencia de Género,
Zika.
2021:
•
Hasta enero de 2021: La Cuenta de Alto Costo (CAC) estima
134.902 personas viviendo con VIH en Colombia.
•
1.5 millones de personas fueron infectadas con VIH globalmente.
•
2021 (sin especificar mes): El Ministerio de Salud y Protección
Social publica la actualización de las Guías de Práctica Clínica
(GPC) elaboradas por el Instituto de Evaluación Tecnológica en
Salud (IETS) para la atención del VIH/SIDA.
•
23 de marzo de 2022: Luis Enrique Mayorga Mogollón actualiza el
protocolo de vigilancia del INS.
•
El INS registra 14 informes de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Bajo Peso al Nacer,
Cáncer en menores de 18 años, Chagas, Chikungunya, Cólera,
Defectos Congénitos, Dengue, Desnutrición en menores de 5 años,
Difteria, Encefalitis Equina, Enfermedad Diarreica Aguda,
Enfermedades Huérfanas - Raras, Enfermedades Transmitidas por
Alimentos, Evento Adverso Grave Posterior a la Vacunación,
Eventos de Baja Frecuencia, Fiebre Amarilla, Fiebre Tifoidea y
Paratifoidea, Hepatitis A, Hepatitis B y C, Infección
Respiratoria Aguda, Infecciones Asociadas a Dispositivos (IAD),
Infecciones Asociadas a la Atención en Salud - Consumo de
Antibióticos, Infecciones Asociadas a la Atención en Salud-
Brotes de IAAS, Infecciones Asociadas a Procedimientos Médico
Quirúrgicos (IAPMQ), Intento de Suicidio, Intoxicaciones,
Leishmaniasis, Lepra, Leptospirosis, Lesiones de Causa Externa,
Lesiones por Artefactos Explosivos, Malaria, Meningitis,
Morbilidad Materna Extrema, Mortalidad en menores de 5 años,
Mortalidad Materna, Mortalidad Perinatal y Neonatal, Parálisis
Flácida Aguda, Parotiditis, Rabia, Sarampión y Rubéola, Sífilis
Gestacional y Congénita, Síndrome de Rubéola Congénita, Tétanos
Accidental, Tétanos Neonatal, Tos Ferina, Tuberculosis,
Tuberculosis Farmacorresistente, Unidad de Análisis, Varicela,
Violencia de Género, Zika.
•
Cifras de cumplimiento de metas 95-95-95 en Colombia: 77.3%
diagnosticado, 88.3% en tratamiento, 87.6% con supresión viral.
•
Estudio Bienvenir (2021-2022): Encuentra una prevalencia de VIH
del 0.9% en la población venezolana refugiada y migrante en
Colombia. La cascada de atención revela que 47.9% fueron
diagnosticados, 38% recibían TARV, y 35.2% tenían carga viral
suprimida.
2022:
•
En Sivigila: Se reportan 19.183 casos de VIH en Colombia, un
8.7% más que en 2021.
•
El INS registra 15 informes de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Baja Frecuencia de
Notificación, Bajo Peso al Nacer, Cáncer en menores de 18 años,
Chagas, Chikungunya, COVID-19, Defectos Congénitos, Dengue,
Desnutrición en menores de 5 años, Difteria, Encefalitis Equina,
Enfermedad Diarreica Aguda, Enfermedades Huérfanas - Raras,
Enfermedades Transmitidas por Alimentos, Evento Adverso Grave
Posterior a la Vacunación, Fiebre Amarilla, Fiebre Tifoidea y
Paratifoidea, Hepatitis A, Hepatitis B y C, Infección
Respiratoria Aguda, Infecciones Asociadas a Dispositivos (IAD),
Infecciones Asociadas a la Atención en Salud - Consumo de
Antibióticos, Infecciones Asociadas a la Atención en Salud-
Brotes de IAAS, Infecciones Asociadas a Procedimientos Médico
Quirúrgicos (IAPMQ), Intento de Suicidio, Intoxicaciones,
Leishmaniasis, Lepra, Leptospirosis, Lesiones de Causa Externa,
Lesiones por Artefactos Explosivos, Malaria, Meningitis,
Morbilidad Materna Extrema, Mortalidad en menores de 5 años,
Mortalidad Materna, Mortalidad Perinatal y Neonatal, Mpox,
Parálisis Flácida Aguda, Parotiditis, Rabia, Sarampión y
Rubéola, Sífilis Gestacional y Congénita, Síndrome de Rubéola
Congénita, Síndrome Inflamatorio Multisistémico en Niños
Asociados a SARS-COV2, Tétanos Accidental, Tos Ferina,
Tuberculosis, Tuberculosis Farmacorresistente, Unidad de
Análisis, Varicela, Violencia de Género, Zika.
•
La tasa de casos notificados de VIH en Colombia aumenta a 39.2
por 100.000 habitantes.
•
Se reportan aproximadamente 12.178 casos de acceso carnal,
explotación sexual y trata de personas en Colombia. De estos,
8.004 ingresaron a servicios de salud en las primeras 72 horas,
y solo el 58.3% recibió profilaxis para VIH.
•
Fin del periodo de estudio (2018-2022) para la carga de
enfermedad por VIH/SIDA. Los habitantes de los departamentos de
Colombia perdieron 1,051,599 (II 95% 849,217.41-1,253,980) Años
de Vida Ajustados por Discapacidad (AVAD) por VIH/SIDA. Quindío
registra la tasa más alta de AVAD (4,029.8), mientras Vichada la
más baja (297.2). Los hombres pierden en promedio 23,833.48 AVAD,
y las mujeres 8,033. El 75% de los AVAD en hombres ocurren entre
los 20 y 49 años, y en mujeres el 71.4% en el mismo grupo de
edad.
2023:
•
Noviembre de 2023: Se estima que aproximadamente 2,875,743
personas refugiadas y migrantes venezolanas han llegado a
Colombia.
•
Resolución 1579 de 2023 (sin fecha de publicación específica,
pero referenciada como de 2023): El Ministerio de Salud y
Protección Social declara de interés público someter una patente
de medicamentos con Dolutegravir a licencia obligatoria en la
modalidad de uso gubernamental. Esta resolución también incluye
a personas migrantes regulares e irregulares en las poblaciones
a las que se refiere.
•
El INS publica manuales de "Vigilancia basada en comunidad".
•
El INS registra 15 informes de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Baja Frecuencia de
Notificación, Cáncer en menores de 18 años, Chagas, Chikungunya,
COVID-19, Defectos Congénitos, Dengue, Desnutrición en menores
de 5 años, Difteria, Encefalitis Equina, Enfermedad Diarreica
Aguda, Enfermedades Huérfanas - Raras, Enfermedades Transmitidas
por Alimentos, Evento Adverso Grave Posterior a la Vacunación,
Fiebre Amarilla, Fiebre Tifoidea y Paratifoidea, Hepatitis A,
Hepatitis B y C, Infección Respiratoria Aguda, Infecciones
Asociadas a Dispositivos (IAD), Infecciones Asociadas a la
Atención en Salud - Consumo de Antibióticos, Infecciones
Asociadas a la Atención en Salud- Brotes de IAAS, Infecciones
Asociadas a Procedimientos Médico Quirúrgicos (IAPMQ), Intento
de Suicidio, Intoxicaciones, Leishmaniasis, Lepra, Leptospirosis,
Lesiones de Causa Externa, Lesiones por Artefactos Explosivos,
Malaria, Meningitis, Morbilidad Materna Extrema, Mortalidad en
menores de 5 años, Mortalidad Materna, Mortalidad Perinatal y
Neonatal, Mpox, Parálisis Flácida Aguda, Parotiditis, Rabia,
Sarampión y Rubéola, Sífilis Gestacional y Congénita, Síndrome
de Rubéola Congénita, Síndrome Inflamatorio Multisistémico en
Niños Asociados a SARS-COV2, Tétanos Accidental, Tos Ferina,
Tuberculosis, Tuberculosis Farmacorresistente, Unidad de
Análisis, Varicela, Violencia de Género, Zika.
•
29 y 30 de mayo de 2023: Se llevan a cabo espacios virtuales
para la validación externa de los algoritmos de la "Vía clínica
para la prevención, diagnóstico, tratamiento y seguimiento de
personas viviendo con VIH" con el financiador y otras partes
interesadas.
2024:
•
Junio de 2024: Se publica el documento final "Vía clínica para
la prevención, diagnóstico, tratamiento y seguimiento de
personas viviendo con VIH" por el Ministerio de Salud y
Protección Social y el IETS.
•
30 de junio de 2024: Henry Sepúlveda Medina actualiza la
introducción, estado del arte, y plan decenal de salud pública
2022-2031 en la versión 8 del Protocolo de Vigilancia en Salud
Pública de VIH/SIDA del INS.
•
El INS registra 7 informes de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Agresiones por Animales
Potencialmente Transmisores de la Rabia, Cáncer en menores de 18
años, Chagas, Chikungunya, COVID-19, Defectos Congénitos,
Dengue, Desnutrición en menores de 5 años, Difteria, Encefalitis
Equina, Enfermedad Diarreica Aguda, Enfermedades Huérfanas -
Raras, Enfermedades Transmitidas por Alimentos, Fiebre Amarilla,
Fiebre Tifoidea y Paratifoidea, Hepatitis A, Hepatitis B y C,
Infección Respiratoria Aguda, Infecciones Asociadas a
Dispositivos (IAD), Infecciones Asociadas a la Atención en
Salud- Brotes de IAAS, Infecciones Asociadas a Procedimientos
Médico Quirúrgicos (IAPMQ), Intento de Suicidio, Intoxicaciones,
Leishmaniasis, Lepra, Leptospirosis, Lesiones de Causa Externa,
Lesiones por Artefactos Explosivos, Malaria, Meningitis,
Morbilidad Materna Extrema, Mortalidad en menores de 5 años,
Mortalidad Materna, Mortalidad Perinatal y Neonatal, Mpox,
Parálisis Flácida Aguda, Parotiditis, Rabia, Sarampión y
Rubéola, Sífilis Gestacional y Congénita, Síndrome de Rubéola
Congénita, Tétanos Accidental, Tos Ferina, Tuberculosis,
Tuberculosis Farmacorresistente, Varicela, Violencia de Género,
Zika.
2025:
•
La publicación "Carga de la enfermedad por VIH/sida en los
departamentos de Colombia, 2018-2022" está fechada en 2025,
indicando su publicación.
•
El INS registra 7 informes de evento de VIH-SIDA. Otros eventos
registrados incluyen Accidente Ofídico, Agresiones por Animales
Potencialmente Transmisores de la Rabia, Cáncer en menores de 18
años, Chagas, Chikungunya, COVID-19, Defectos Congénitos,
Dengue, Desnutrición en menores de 5 años, Difteria, Encefalitis
Equina, Enfermedad Diarrea Aguda, Enfermedades Huérfanas -
Raras, Enfermedades Transmitidas por Alimentos, Fiebre Amarilla,
Fiebre Tifoidea y Paratifoidea, Hepatitis A, Hepatitis B y C,
Infección Respiratoria Aguda, Infecciones Asociadas a
Dispositivos (IAD), Infecciones Asociadas a la Atención en
Salud- Brotes de IAAS, Infecciones Asociadas a Procedimientos
Médico Quirúrgicos (IAPMQ), Intento de Suicidio, Intoxicaciones,
Leishmaniasis, Lepra, Leptospirosis, Lesiones de Causa Externa,
Lesiones por Artefactos Explosivos, Malaria, Meningitis,
Morbilidad Materna Extrema, Mortalidad en menores de 5 años,
Mortalidad Materna, Mortalidad Perinatal y Neonatal, Mpox,
Parálisis Flácida Aguda, Parotiditis, Rabia, Sarampión y
Rubéola, Sífilis Gestacional y Congénita, Síndrome de Rubéola
Congénita, Tétanos Accidental, Tos Ferina, Tuberculosis,
Tuberculosis Farmacorresistente, Varicela, Violencia de Género,
Zika.
2030 (Meta a futuro):
•
ONUSIDA propone que el 95% de todas las personas con VIH
conozcan su estado serológico, el 95% de todas las personas con
VIH diagnosticadas reciban tratamiento antirretroviral, y el 95%
de todas las personas que reciben tratamiento antirretroviral
tengan supresión viral.
•
El Plan Decenal de Salud Pública 2022 - 2031 tiene como meta
para 2031 mantener la Tasa de Transmisión Materno-Infantil (TMI)
de VIH en al menos 2% y que al menos el 55% de las personas que
viven con VIH sean diagnosticadas en estados tempranos.
Seguimiento SIVIGILA del Instituto Nacional de Salud INS: Informes de Evento VIH-SIDA y muerte por SIDA
Semestre1/23 y Semana8/24
El Instituto Nacional de Salud
produce varios informes de carácter epidemiológico que debe
relacionarse con los resultados en salud y la pertinencia en la
destinación de recursos del sistema de salud. Por ejemplo,
Informes de Evento como
VIH, SIDA y muerte por SIDA Colombia 2020
armi y especialmente del
Primer Semestre de 2023
armi, deben correlacionarse con los datos de la Cuenta de
Alto Costo y complementar y actualizar la
documentación que aparece en las páginas de MinSalud, por
ejemplo en el punto "Situación actual y estudios relevantes"
que se encuentra bastante desactualizado. Aunque en tema
de actualizaciones resulta aún más urgente la revisión de la
Guía de Práctica Clínica (GPC) basada en la evidencia científica
para la atención de la infección por VIH/SIDA en niñas, niños y
adolescentes así como
en personas adultas, gestantes y adolescentes que aparecen
en las páginas del IETS con fecha 19 de mayo de 2021.
Gráfico N°25: Ejemplo de
seguimiento por SIVIGILA este informe de Evento
Primer Semestre VIH, SIDA y muerte por SIDA, SIVIGILA INS 2023
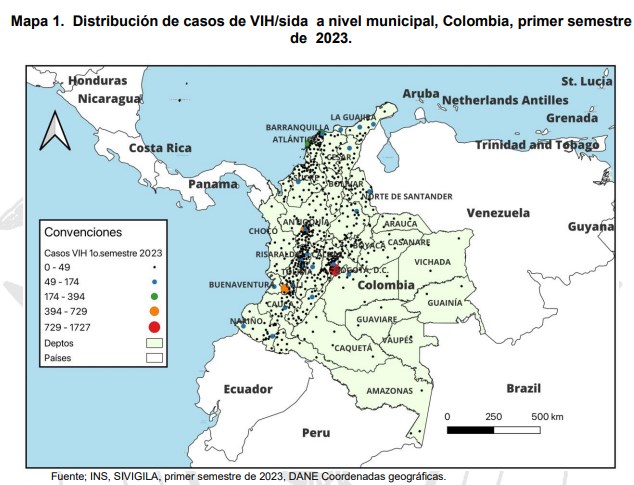
Pulse click en la imagen para
activar el enlace al
Archivo de Reserva de Med-Informática (armi)
Aunque más deseable aún sería la
correlación pertinente con los Indicadores de evolución por
semanas epidemiológicas como de la
Semana 8 de 2024 en Cartagena
armi.
Gráfico N°26: Ejemplo de
seguimiento por SIVIGILA Indicador 4 de
Evento VIH, SIDA y muerte por SIDA, Semana 8 de 2024 en
Cartagena SIVIGILA INS 2024

Pulse click en la imagen
para activar el enlace al Archivo de Reserva de Med-Informática
(armi)
3.4.
3.4. Litigio en curso y
alternativas en caso de Derogatoria de la Licencia Obligatoria
Se
completará en colaboración con el equipo jurídico.
¿Incluir aquí la secuencia normativa de
la
Licencia Obligatoria para Uso Gubernamental de DOLUTEGRAVIR: Después de la
Resolución N° 01579 de 2023
armi del 23 de abril de
2024, la Superintendencia de Industria y Comercio SIC expidió la
Resolución No. 20049 de 2024
armi, que concedió la
Licencia Obligatoria para Uso Gubernamental (LOUG) de
DOLUTEGRAVIR. Frente a esta medida se interpusieron
acciones legales
por parte de AFIDRO
armi. y otros actores
interesados. La
Resolución SIC 34716 del 28jun24
armi resolvió el recurso de reposición presentado por los
titulares de la patente 07115501A de DOLUTEGRAVIR (SHIONOGI & CO.
y VIIV HEALTHCARE CO.) y ratificó la medida. El 20ago24,
MinSalud publicó el
Proyecto de Resolución
armi con su respectiva
Memoria Justificativa
armi, estableciendo un período de consulta pública hasta el
Miércoles 28 de agosto de 2024. (Completar con apoyo del
equipo jurídico)?
|
En
Síntesis,
el punto 3 del documento,
titulado "VIH-SIDA en Colombia según Informes de
la CAC, GPC, IETS, SIVIGILA y el INS de los años 2022 a
2024", aborda la situación del VIH-SIDA en
Colombia desde múltiples perspectivas, incluyendo datos
epidemiológicos, guías de práctica clínica y el impacto
de la Licencia Obligatoria para Dolutegravir. Se destaca
que, si bien el enfoque en Dolutegravir puede ser
pertinente a nivel internacional, es crucial considerar
la realidad nacional.
3.1. VIH-SIDA en
Colombia según Informes de la Cuenta de Alto Costo (CAC)
de los años 2022 a 2024
- Contexto y
Cronología: Este apartado utiliza informes
de la CAC de 2022, 2023 y 2024 para describir la
evolución de la epidemia de VIH en el país,
incluyendo hitos legislativos y normativas de salud
pública. Se menciona una disminución del 37% en
muertes anuales por VIH en las Américas desde 2010 y
que la CAC inició el registro de casos incidentes de
VIH en 2012.
- Datos
Epidemiológicos (Reporte 2022, período feb 2021-ene
2022):
- 141.787 personas
viviendo con VIH (PVV) en el SGSSS.
- 12.919 casos
nuevos diagnosticados, un aumento del
40.27%.
- Tasa de
incidencia de 24.78 por 100.000 habitantes.
- Reducción de la
indetectabilidad de la carga viral y la
cobertura de la Terapia Antirretroviral (TAR) en
la población privada de la libertad.
- Datos
Epidemiológicos (Reporte 2023, período feb 2022-ene
2023):
- 165.405 PVV en
Colombia, un aumento del 16.66%.
- 14.670 casos
incidentes diagnosticados, un aumento del
13.5%.
- El
34.46% de los casos incidentes fueron
diagnosticados en fase SIDA, indicando un
diagnóstico tardío.
- La adherencia a
las nuevas indicaciones de TAR fue inferior al
30% a nivel nacional.
- Se
diagnosticaron 1.168 mujeres con VIH durante la
gestación y se reportaron 7 casos positivos en
niños menores de 12 meses hijos de madres con
VIH, un aumento del 40%.
- El
13.59% de los casos de tuberculosis (TB)
tuvieron coinfección con VIH.
- Retos:
Persisten desafíos significativos en el
diagnóstico tardío, la adherencia a las
guías de tratamiento y la atención en poblaciones
vulnerables.
- Tenofovir:
El informe de la CAC de 2022 identificó Tenofovir
como el medicamento más reportado, pero no
diferenció entre Tenofovir Alafenamida (con patente
vigente) y Tenofovir Disoproxil Fumarato (sin
patente vigente), una distinción importante.
3.2. Situación
del VIH-SIDA en Colombia según Guías de Práctica Clínica
(GPC) de 2021 y 2024
- Esta sección
presenta una cronología de las GPC en Colombia,
destacando hitos como la introducción de
antirretrovirales en 1995 y la primera guía oficial
en 2006.
- Las GPC actualizadas
en 2021 y la "Vía Clínica para la prevención,
diagnóstico, tratamiento y seguimiento de personas
viviendo con VIH" publicada en junio de 2024, hacen
hincapié en el diagnóstico temprano, el
inicio oportuno de la TAR y el manejo
interdisciplinario.
- La GPC de 2021
identificó la combinación TDF/3TC/DTG como la
primera opción de tratamiento.
3.3. Situación
del VIH-SIDA en Colombia según el IETS y SIVIGILA del
INS de 2022 a 2024
- Esta sección
complementa la información de la CAC con informes
epidemiológicos de SIVIGILA del Instituto Nacional
de Salud (INS).
- Datos de
SIVIGILA/INS:
- En 2022,
SIVIGILA reportó 19.183 casos de VIH, un aumento
del 8.7% respecto a 2021, con una tasa de
incidencia de 39.2 por 100.000 habitantes.
- Entre 2018 y
2022, se perdieron 1.051.599 Años de Vida
Ajustados por Discapacidad (AVAD) por VIH/SIDA
en Colombia.
- La
Resolución 1579 de 2023 del Ministerio
de Salud declaró el interés público para someter
la patente del Dolutegravir a licencia
obligatoria para uso gubernamental, incluyendo a
migrantes regulares e irregulares.
- Se señala que los
informes del Ministerio de Salud y las GPC del IETS
a menudo están desactualizados, lo
que subraya la necesidad de correlacionar los datos
de SIVIGILA con los de la CAC para optimizar la
asignación de recursos.
3.4. Litigio en
curso y alternativas posibles en caso de Derogatoria de
la Licencia Obligatoria
- Esta sección, que se
completará con el equipo jurídico, detalla el
proceso legal de la Licencia Obligatoria
para Uso Gubernamental (LOUG) de DOLUTEGRAVIR.
- La Superintendencia
de Industria y Comercio (SIC) emitió la Resolución
No. 20049 de 2024, concediendo la LOUG para
DOLUTEGRAVIR (TIVICAY®), y posteriormente ratificó
esta medida con la Resolución SIC 34716 del 28 de
junio de 2024, a pesar de las acciones legales
interpuestas por AFIDRO y otros actores.
- El Ministerio de
Salud y Protección Social publicó un Proyecto de
Resolución y su Memoria Justificativa el 20 de
agosto de 2024, abriendo un período de consulta
pública.
- La implementación de
la LOUG es vista como una medida pertinente del
gobierno para promover este tratamiento debido a su
mayor eficacia, menores efectos secundarios
y mejor relación costo-beneficio, en
defensa de la salud pública. Su revocación sería una
"catástrofe sanitaria".
El análisis de las prescripciones de la
Combinación EMTRICITABINA + TENOFOVIR ALAFENAMIDA +
BICTEGRAVIR (BIKTARVY®
de GILEAD) en los años 2021 a 2023 tanto por 5 principales
regiones como por 5 principales EPSs muestra que el
número de prescripciones reportadas por regiones y por
EPSs es mínimo y las cifras resultan tan insignificantes
que no alcanzan ni siquiera para configurar una muestra
representativa.
En
síntesis, BIKTARVY®
CUM 20151774-01
de GILEAD, la combinación de EMTRICITABINA + TENOFOVIR
ALAFENAMIDA + BICTEGRAVIR sigue siendo monopólica y sus
reportes a SISMED muestran inconsistencias
similares a las descritas con DOLUTEGRAVIR que tampoco se validaron ni analizaron.
GILEAD es muy activo en demandas de protección de la
propiedad intelectual como con Tenofovir Alafenamida,
así pierda como el caso de Bictegravir. |
4.
4. Lamivudina+Tenofovir Disoproxil + Dolutegravir
la opción
STR
disponible por OPS
De acuerdo con el
Proyecto de Resolución
armi con su respectiva
Memoria Justificativa
armi la opción elegida será la de la Organización
Panamericana de la Salud:
El Gráfico N°28
muestra una captura de la pantalla de la Combinación LAMIVUDINA+TENOFOVIR DISOPROXIL+DOLUTEGRAVIR
en la páginas de la OPS sobre el tema
Gráfico N°27: La Combinación LAMIVUDINA + TENOFOVIR DISOPROXIL + DOLUTEGRAVIR
ea la opción
elegida por la OPS

4.1.
4.1. Combinación Biktarvy monopólica y sin precio regulado pero
con patente discutible
Las pantallas de seguimiento de principios
activos y presentaciones reportadas a SISMED de BICTEGRAVIR y
BIKTARVY muestran la evolución de este competidor directo de
DOLUTEGRAVIR y también las mismas inconsistencias
observadas en el sistema de información.
La pantalla de búsqueda de principios activos del Sistema VMI-CFN
muestra 4 opciones de combinación de EMTRICITABINA con TENOFOVIR
ALAFENAMIDA. todas con productos de Gilead (casi todas
monopólicas) mientras las combinaciones con TENOFOVIR DISOPROXIL
son múltiples y además con moléculas distintas de la opción
EMTRICITABINA. La opción de Combinación EMTRICITABINA +
TENOFOVIR ALAFENAMIDA + BICTEGRAVIR es la competidora directa de
DOLUTEGRAVIR y sus combinaciones. Las multinacionales
propietarias de DOLUTEGRAVIR entablaron y ganaron el litigio
internacional llegando a un arreglo económico que está
vigente.
Gráfico N°28: La Combinación
EMTRICITABINA + TENOFOVIR ALAFENAMIDA + BICTEGRAVIR competidora
directa de DOLUTEGRAVIR y Combinaciones
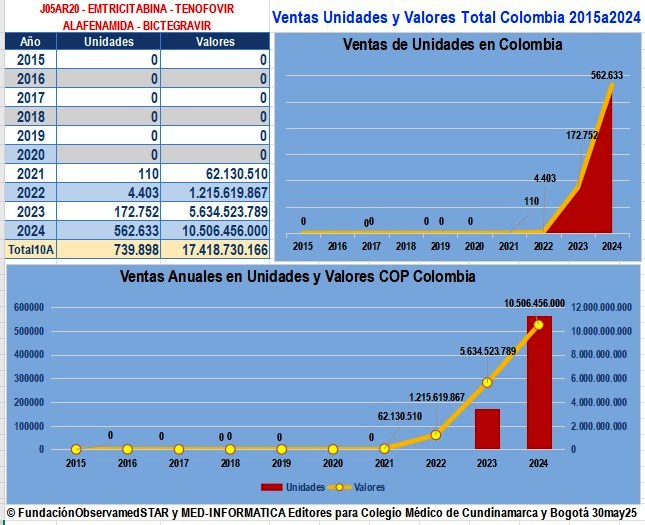
Gráfico N°29: La Combinación EMTRICITABINA+TENOFOVIR ALAFENAMIDA+BICTEGRAVIR
es la opción competidora directa de Dolutegravir y Combinaciones
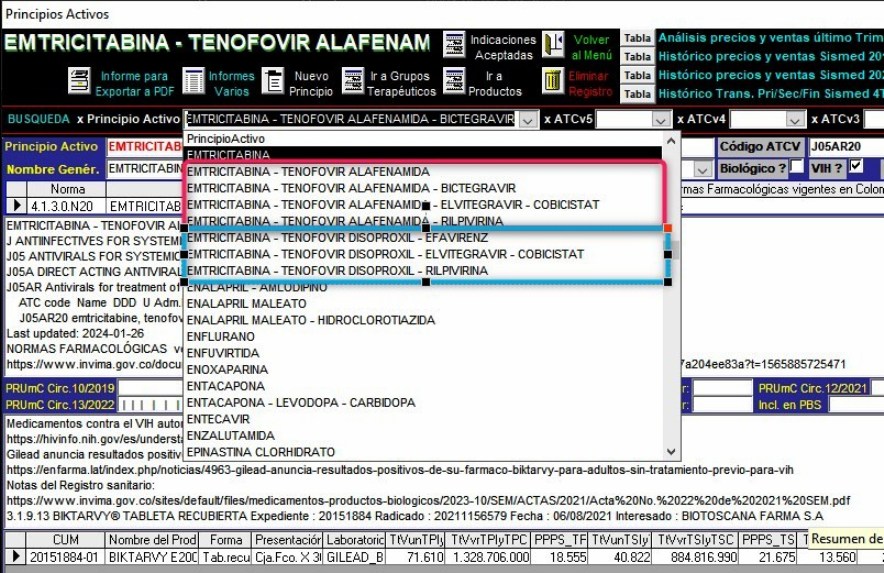
Aunque
el volumen de ventas de BIKTARVY no es aún muy significativo, el
análisis de las mismas variables analizadas con DOLUTEGRAVIR
permiten deducir que el impacto de las opciones de Gilead
terminará siendo superior.
Gráfico N°30: La Combinación EMTRICITABINA + TENOFOVIR ALAFENAMIDA + BICTEGRAVIR
de Gilead es monopólica y no tiene regulación de precios
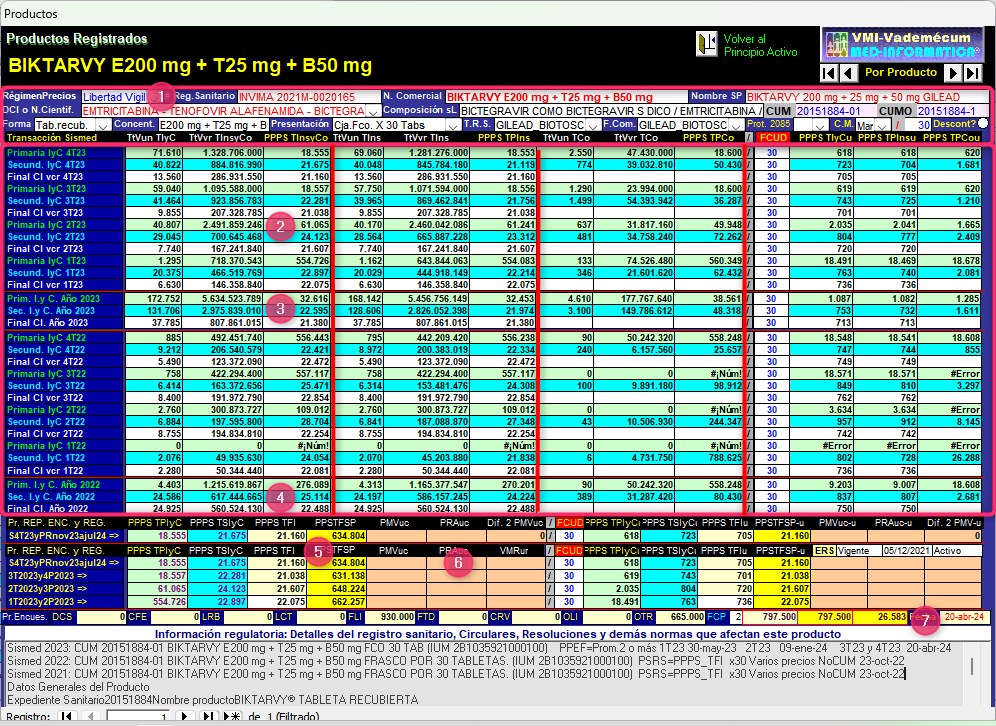
Nótese que BIKTARVY 1) Está en régimen de Libertad Vigilada, es
decir no tiene regulación de precios; 2) Muestra grandes
diferencias entre Transacciones Primarias de canal institucional
y comercial, Secundarias de canal institucional y comercial y
Finales de canal institucional; 4) Dichas diferencias afectan
los diferentes cálculos del sistema; 5) Los reportes deben ser
por CUM o presentación, pero generalmente corresponden a
unidosis, en este caso a tabletas, que deben ajustarse a la
presentación; 6) La falta de regulación afecta a toda la cadena
de distribución y 7) Obviamente la desregulación afecta el gasto
del consumidor final, al institucional y al gasto de bolsillo.
Gráfico N°31: BIKTARVY Combinación EMTRICITABINA + TENOFOVIR ALAFENAMIDA + BICTEGRAVIR
de Gilead sigue monopólica y sin regulación de precios
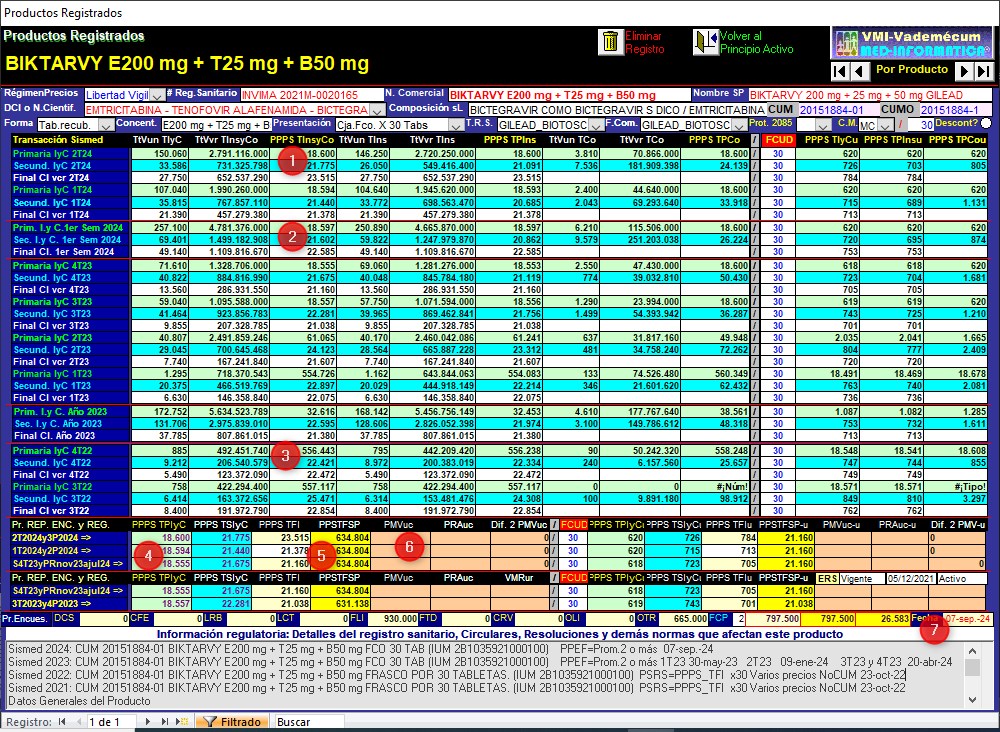
Nótese que BIKTARVY 1) Sigue en
régimen de Libertad Vigilada, es decir no tiene regulación de
precios; 2) Sigue mostrando grandes diferencias entre
Transacciones Primarias de canal institucional y comercial,
Secundarias de canal institucional y comercial y Finales de
canal institucional; 4) Los precios deben corresponder al CUM o
presentación, pero siguen correspondiendo a unidosis, en este
caso tabletas, que deben ajustarse a la presentación; 6) La
falta de regulación sigue afectando a toda la cadena de
distribución y 7) La desregulación de precios sigue afectando el
gasto del consumidor final, sea institucional o gasto de
bolsillo de los pacientes.
Prescripciones de
BIKTARVY
de 2021 a 2023 y a 2025 en 5 Regiones y 5 EPS
El análisis de las
prescripciones de la Combinación EMTRICITABINA + TENOFOVIR
ALAFENAMIDA + BICTEGRAVIR (BIKTARVY® de GILEAD) en la plataforma
MiPres también muestra inconsistencias prominentes que invalidan
cualquier evaluación con las modalidades que permitía la misma.
Mostramos aquí lo poco que puede verse para 5 regiones y 5 EPSs
más importantes
Gráfico N°32. Prescripciones de BIKTARVY® de GILEAD de 2021 a 2025 en 5 Regiones
y 5 EPS
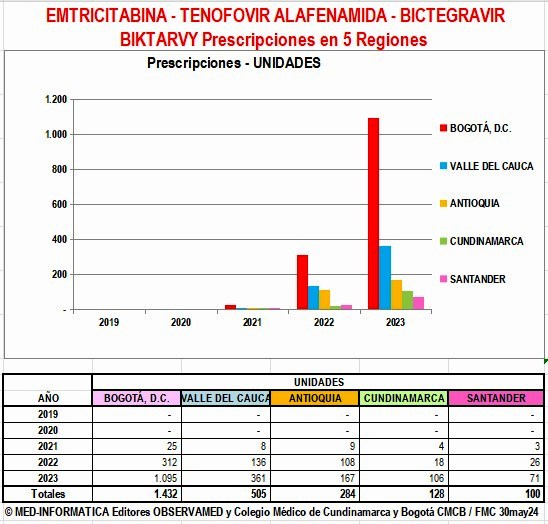 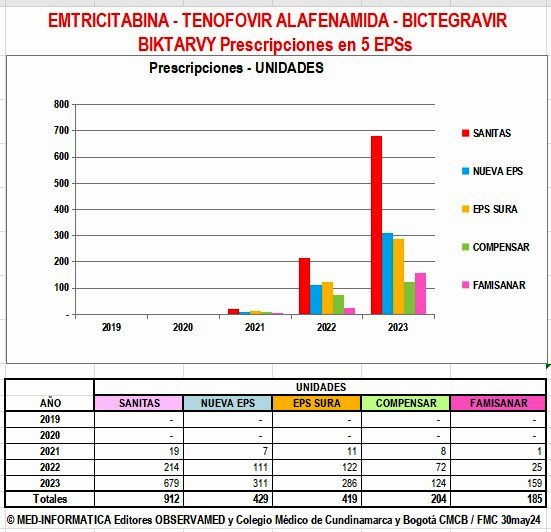
El análisis de las prescripciones de
BIKTARVY® de GILEAD en la plataforma MiPres muestra que de 2021
a 2023 el mayor número de prescripciones se habría generado en
las regiones de Bogotá, Valle del Cauca, Antioquia, Cundinamarca
y Santander..El problema está en que el número de prescripciones
reportadas por regiones es mínimo y las cifras resultan tan
insignificantes que no alcanzan ni siquiera para configurar una
muestra mínimamente significativa.
Gráfico N°33. Prescripciones de BIKTARVY® de GILEAD de 2020 a 2025 en 5 Regiones
y 5 EPS
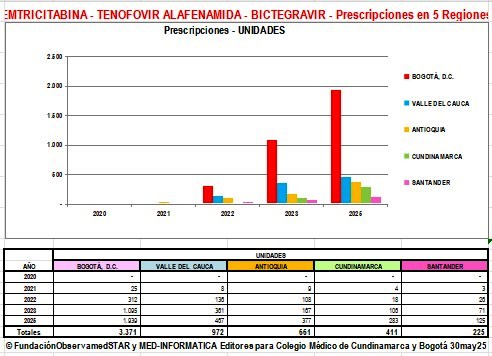 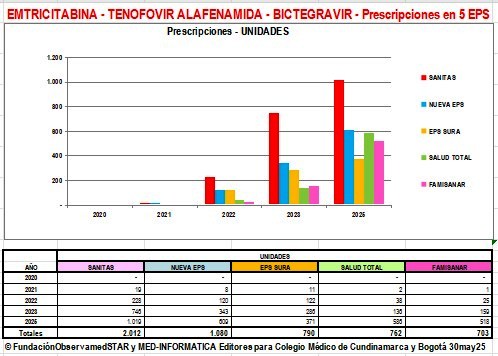
El análisis de las
prescripciones de BIKTARVY® de GILEAD en la plataforma MiPres
muestra que de 2021 a 2023 el mayor número de prescripciones se
habría generado en las 5 EPSs más importantes muestra a Sánitas,
Nueva EPS, EPS Sura, Compensar y Famisanar. El problema está en que el número
de prescripciones reportadas por EPSs es mínimo y las cifras
resultan tan insignificantes que no alcanzan ni siquiera para
configurar una muestra mínimamente significativa.
4.2.
4.2.
Lamivudina+Tenofovir Disoproxil+Dolutegravir:
Opción
similar a
opciónOPS conDTG
combinación de EMTRICITABINA con TENOFOVIR
ALAFENAMIDA. todas con productos de Gilead (casi todas
monopólicas) mientras las combinaciones
El Gráfico N°29
muestra otras opciones de suministro de la Combinación LAMIVUDINA+TENOFOVIR DISOPROXIL+DOLUTEGRAVIR
que podrían estar disponibles
Gráfico N°34: Otras opciones de
la Combinación LAMIVUDINA + TENOFOVIR DISOPROXIL + DOLUTEGRAVIR
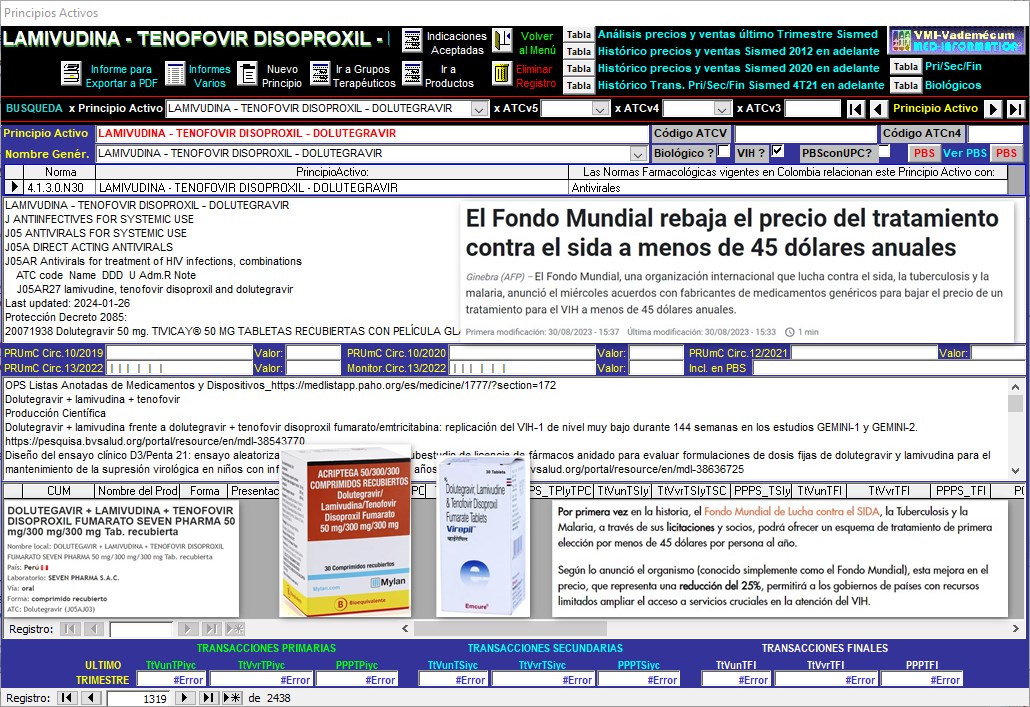
Las licencias obligatorias en curso fueron solicitadas por:
1. MINISTRO DE SALUD Y PROTECCIÓN SOCIAL 2. LABORATORIOS
RICHMOND COLOMBIA S.A.S y 3. HETERO LABS LIMITED y SEVEN PHARMA
COLOMBIA S.A.S. Otras dos fueron negadas por extemporáneas: 1.
PHARMA COLOMBIA S.A.S. y 2. EXELTIS COLOMBIA SAS
La Licencia
Obligatoria de
DOLUTEGRAVIR para uso gubernamental, está en el núcleo de
una política pública ajustada a la
tendencia mundial de
Tratamientos de dosis diaria STR,
que se consideran de
✔mayor eficacia,
✔menores efectos secundarios y
✔mejor
relación costo-beneficio. Según el
Proyecto de Resolución
armi con su respectiva
Memoria Justificativa
armi esta política se implementará con DOLUTEGRAVIR
y sus
combinaciones con
LAMIVUDINA y TENOFOVIR DISOPROXIL Fumarato..
4.3.
4.3.
Combinaciones
disponibles con Emtricitabina y
Tenofovir Disoproxil o Alafenamida
Las combinaciones monopóllicas de EMTRICITABINA y TENOFOVIR
Disoproxil o Alafenamida, de GILEAD, reportaron ventas a SISMED
del 2° trimestre de 2024 de 832.740 unidades por
COP $13.433.070.159, algo que tampoco puede ser ignorado al
momento de implementar una política pública basada en
DOLUTEGRAVIR de GSK.
|
Combinaciones monopólicas de Emtricitabina y Tenofovir
|
MP? |
Productos |
Laboratorio |
Unidades2T24 |
Valores2T24 |
| EMTRICITABINA - TENOFOVIR ALAFENAMIDA -
ELVITEGRAVIR - COBICISTAT |
SI |
GENVOYA E200 mg + TA10 mg + E150 mg + C150 mg |
GILEAD_BIOTOSCANA |
224.490 |
3.676.930.937 |
| EMTRICITABINA - TENOFOVIR ALAFENAMIDA -
RILPIVIRINA |
SI |
ODEFSEY E200 mg + TA25 mg + R25 mg |
GILEAD_BIOTOSCANA |
310.350 |
4.745.221.192 |
| EMTRICITABINA - TENOFOVIR DISOPROXIL -
ELVITEGRAVIR - COBICISTAT |
SI |
STRIBILD E200 mg + TD300 mg + E150 mg + C150 mg |
GILEAD_BIOTOSCANA |
60.390 |
1.018.189.831 |
| EMTRICITABINA - TENOFOVIR DISOPROXIL -
RILPIVIRINA |
SI |
COMPLERA E200 mg + TD245 mg + R25 mg |
GILEAD_STENDHAL |
165.900 |
2.664.022.199 |
| |
|
|
|
832.740 |
13.433.070.159 |
Si asumimos el
hecho de la existencia de una confrontación mundial de
multinacionales farmacéuticas por este mercado, es importante
observar que -tal como puede verse en el Gráfico N°24- en
Colombia, el dinamismo de EMTRICITABINA es evidente. Si a este
hecho se suma la dinámica de TENOFOVIR ALAFENAMIDA y la
exclusividad de BICTEGRAVIR, puede concluirse que existe una
realidad de mercado que contradice la exclusividad de la
política pública que se está adelantando con DOLUTEGRAVIR y
plantea la necesidad de buscar soluciones más ajustadas a la
realidad nacional e internacional
4.4.
4.4. Emtricitabinas
disponibles en
Colombia sin Bictegravir que podría ser no patentable
Si asumimos el
hecho de la existencia de una confrontación mundial de
multinacionales farmacéuticas por este mercado, es importante
observar que -tal como puede verse en el Gráfico N°18- en
Colombia, el dinamismo de EMTRICITABINA es evidente. Si a este
hecho se suma la dinámica de TENOFOVIR ALAFENAMIDA y la
exclusividad de BICTEGRAVIR, puede concluirse que existe una
realidad de mercado que contradice la exclusividad de la
política pública que se está adelantando con DOLUTEGRAVIR y
plantea la necesidad de buscar soluciones más ajustadas a la
realidad nacional e internacional.
Gráfico N°29. Ventas de EMTRICITABINAS sin BITEGRAVIR en Colombia - Años 2014 a 2023
Gráfico N°35. Ventas de EMTRICITABINAS sin BITEGRAVIR en Colombia - Años 2014 a 2023
y 2015 a 2024
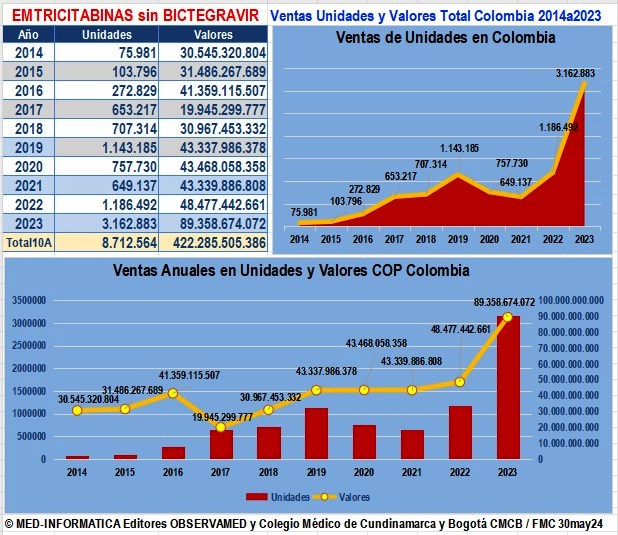 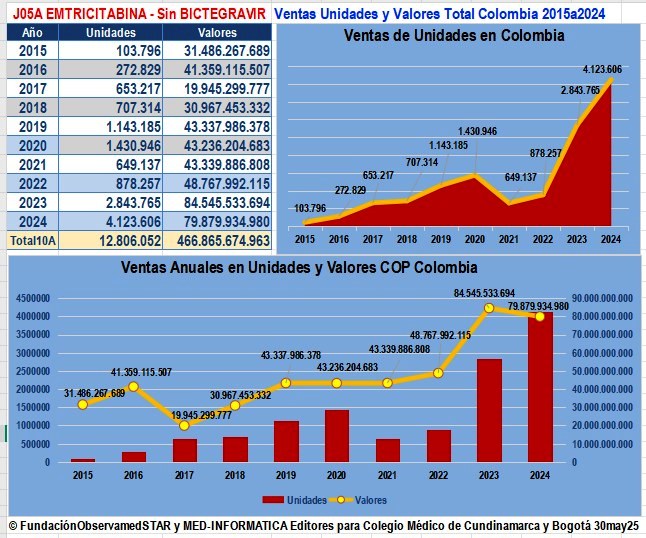
Tal como puede verse en el Gráfico N°30 la Combinación EMTRICITABINA + TENOFOVIR ALAFENAMIDA de DESCOVY CUM 20131470-01
de GILEAD, estuvo disponible también como VYVALTO CUM 20148969-01
de Laboratorios RICHMOND de Colombia. En la actualidad existe
una demanda de GILEAD ante la SIC por este producto.
4.5.
4.5.
Combinación Emtricitabina y
Tenofovir Alafenamida ahora sin protección de patente
Tal como puede verse en el Gráfico N°30 la Combinación EMTRICITABINA + TENOFOVIR ALAFENAMIDA de DESCOVY CUM 20131470-01
de GILEAD, estuvo disponible también como VYVALTO CUM 20148969-01
de Laboratorios RICHMOND de Colombia. En la actualidad existe
una demanda de GILEAD ante la SIC por este producto.
Gráfico N°36. Reportes trimestrales de VYVALTO CUM
20148969-01 de Laboratorios RICHMOND de Colombia - Años 2022 a 2023
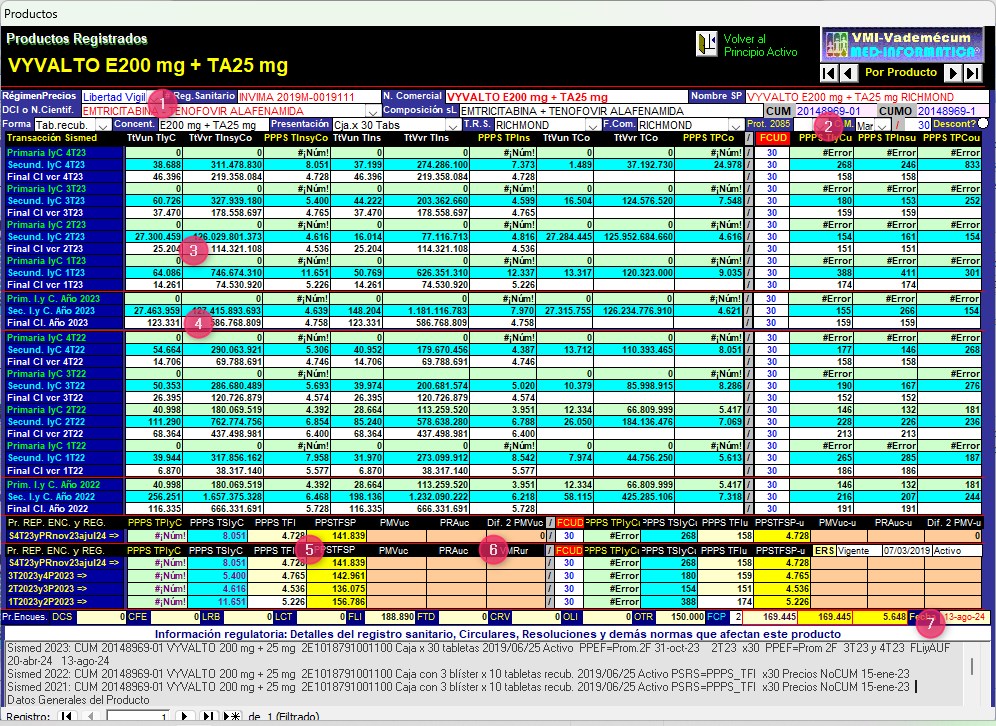
Como sucede con muchos reportes a SISMED, los datos de
VYVALTO CUM 20148969-01 de Laboratorios RICHMOND también tienen
inconsistencias tales como:
a) Al igual que DESCOVY CUM 20131470-01 de GILEAD está en
régimen de Libertad de precios (es decir, no tiene precio
regulado),
b) Sus reportes de Transacciones Primarias, Secundarias y
Finales no guardan coherencia (las diferencias resultan
realmente excesivas),
c) Todos sus Precios reportados son por Tableta o UniDosis y no
por CUM. Esto hace necesario recalcular el PPPS para poder
comparar con el precio en Farmacias,
d) Obviamente, los datos reportados no están validados ni
analizados, algo que deteriora mucho la calidad de la
información.
Gráfico N°37. Reportes trimestrales de VYVALTO CUM
20148969-01 de Laboratorios RICHMOND de Colombia - Años 2023 a 2024
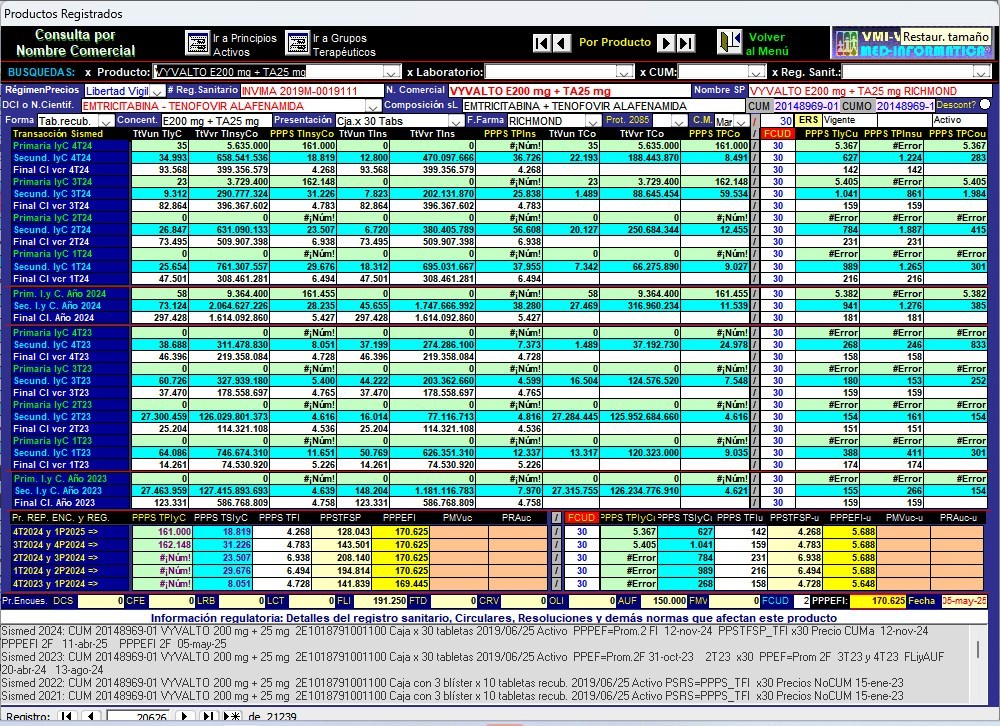
4.6.
4.6.
Total Tenofovir Disoproxil
sin protección de patente para combinaciones diversas
El Gráfico N°25 muestra la evolución de las ventas de TENOFOVIR
DISOPROXIL en la última década. Puede verse que
luego de una evolución dinámica de sus ventas en unidades y
valores hasta el año 2020, se produjo una caída extraordinaria
el año 2021 y una recuperación muy dinámica hasta el año 2023,
La caída del 2021 fue más manifiesta en unidades que en valores
y es posible que se hayan añadido inconsistencias en los
reportes.
Gráfico N°38. Ventas de TENOFOVIR
DISOPROXIL en Colombia - Años 2014 a 2023
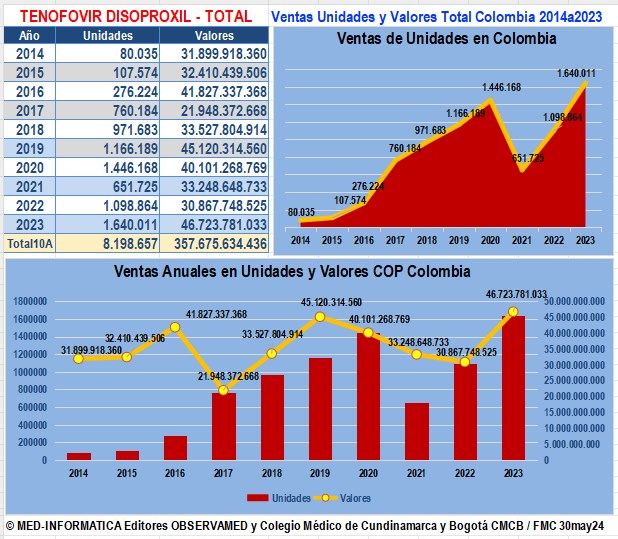 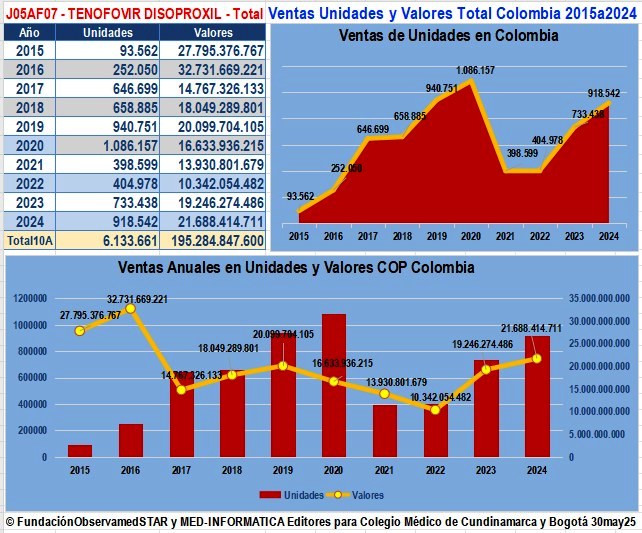
Tal como puede verse en el Gráfico N°30 la Combinación EMTRICITABINA + TENOFOVIR ALAFENAMIDA de DESCOVY CUM 20131470-01
de GILEAD, estuvo disponible también como VYVALTO CUM 20148969-01
de Laboratorios RICHMOND de Colombia. En la actualidad existe
una demanda de GILEAD ante la SIC por este producto.
4.7.
4.7. Ventas de Lamivudina sin Dolutegravir reportadas a SISMED
de 2014 a 2023 y 2024
El Gráfico N°19 muestra la evolución de las ventas de LAMIVUDINA
sin DOLUTEGRAVIR en la última década. Puede verse que luego de
una evolución dinámica de sus ventas en unidades y valores hasta
el año 2016, se produjo una caída constante hasta el año 2023,
mucho más manifiesta en unidades que en valores.
Gráfico N°39. Ventas de LAMIVUDINA sin DOLUTEGRAVIR en Colombia - Años 2014 a 2023
y 2015 a 2024
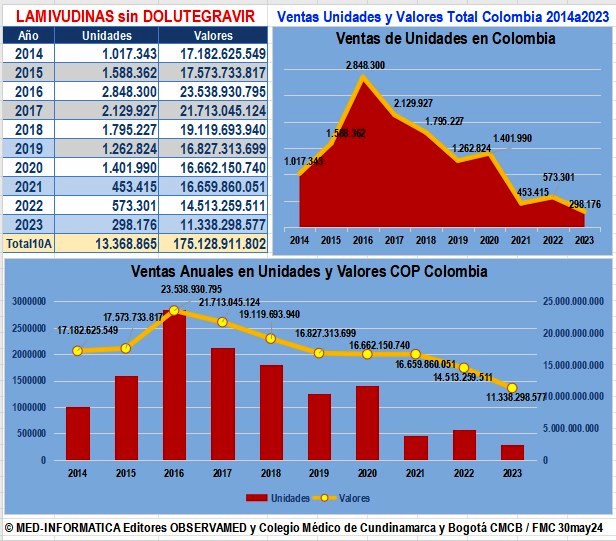 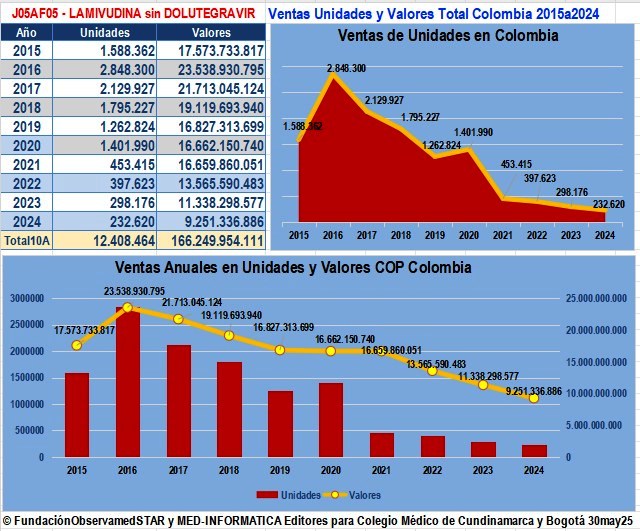
Tal como puede verse en el Gráfico N°30 la Combinación EMTRICITABINA + TENOFOVIR ALAFENAMIDA de DESCOVY CUM 20131470-01
de GILEAD, estuvo disponible también como VYVALTO CUM 20148969-01
de Laboratorios RICHMOND de Colombia. En la actualidad existe
una demanda de GILEAD ante la SIC por este producto.
A continuación, se
resumen los aspectos clave del punto 4.:
- Opción
Estratégica y Política Pública: La
combinación Lamivudina + Tenofovir
Disoproxil + Dolutegravir es la opción
elegida para implementar la política pública,
conforme al Proyecto de Resolución y su Memoria
Justificativa. Esta elección se alinea con la
tendencia mundial de tratamientos STR (Single
Treatment Regimen) que ofrecen mayor
eficacia, menores efectos secundarios y una mejor
relación costo-beneficio. La Organización
Panamericana de la Salud (OPS) también dispone de
documentación que evalúa el uso de esta combinación
(TLD) para el inicio y la transición en personas con
VIH.
- Competencia
Directa: Biktarvy de Gilead:
- La combinación
Emtricitabina + Tenofovir Alafenamida +
Bictegravir (BIKTARVY®) de Gilead es
identificada como un competidor directo de
Dolutegravir y sus combinaciones.
-
Monopólica y sin Regulación de Precios:
BIKTARVY® es un producto monopólico que opera
bajo un régimen de "Libertad Vigilada", lo que
significa que carece de regulación de
precios, lo cual afecta la cadena de
distribución y el gasto del consumidor final, ya
sea institucional o de bolsillo.
-
Inconsistencias en SISMED y MiPres: Los
reportes de BIKTARVY® a SISMED muestran
inconsistencias similares a las de Dolutegravir,
incluyendo grandes diferencias entre
transacciones primarias, secundarias y finales,
así como problemas de reportes por unidosis en
lugar de por CUM (presentación comercial).
Además, el análisis de prescripciones de
BIKTARVY® en la plataforma MiPres revela
inconsistencias prominentes y un número de
prescripciones tan mínimo que invalida cualquier
evaluación y no configura una muestra
representativa.
- Litigios
y Propiedad Intelectual: Las
multinacionales propietarias de Dolutegravir
entablaron y ganaron un litigio internacional
contra Gilead por Bictegravir, llegando a un
arreglo económico. Gilead, a su vez, es muy
activa en demandas de protección de la propiedad
intelectual.
- Otras
Combinaciones de Emtricitabina y Tenofovir:
- Gilead mantiene
una importancia significativa en el mercado con
otras combinaciones monopólicas
de Emtricitabina con Tenofovir Disoproxil o
Tenofovir Alafenamida (como Genvoya, Odefsey,
Stribild, Complera). Las ventas de estas
combinaciones en el segundo trimestre de 2024
fueron significativas, ascendiendo a 832.740
unidades por más de COP 13.433 millones.
- El
dinamismo de Emtricitabina y Tenofovir
Alafenamida, junto con la exclusividad
de Bictegravir, plantea que una política pública
que se base exclusivamente en Dolutegravir
podría contradecir la realidad del mercado
nacional e internacional.
- La combinación
Emtricitabina + Tenofovir Alafenamida (Descovy
de Gilead y Vyvalto de Richmond)
también presenta inconsistencias en sus reportes
a SISMED, como la falta de regulación de
precios, incoherencia entre tipos de
transacciones y problemas de precios por tableta
en lugar de por CUM.
- Tenofovir
Disoproxil y Lamivudina sin Dolutegravir:
- Las ventas de
Tenofovir Disoproxil (sin
protección de patente para diversas
combinaciones) mostraron una evolución dinámica
hasta 2020, una caída extraordinaria en 2021
(más en unidades que en valores, sugiriendo
inconsistencias) y una recuperación dinámica
hasta 2023.
- Las ventas de
Lamivudina sin Dolutegravir
tuvieron una evolución dinámica hasta 2016,
seguida de una caída constante hasta 2023, más
pronunciada en unidades que en valores.
En resumen, el punto 4
subraya la intención del gobierno de implementar una
política pública basada en la combinación Lamivudina +
Tenofovir Disoproxil + Dolutegravir debido a su perfil
beneficioso. Sin embargo, este enfoque se ve desafiado
por la realidad de un mercado de antivirales
altamente concentrado y competitivo, con la
presencia de otras combinaciones monopólicas de Gilead
(como Biktarvy) que no están reguladas en precios y para
las cuales los sistemas de información (SISMED y MiPres)
muestran graves y persistentes inconsistencias,
"datos absurdos" y falta de validación, lo que
dificulta el análisis preciso y la formulación de
políticas. Estas deficiencias estructurales en los
sistemas de información afectan la transparencia y la
eficacia de la política de precios y la toma de
decisiones. |
5.
5. Proyección de acciones
coyunturales desde
gremios de la salud
Tomando en cuenta que los hechos planteados en este documento
constituyen INDUCCIONES PERVERSAS que generan insuficiencias e
inconsistencias graves en el funcionamiento del sistema de salud
colombiano, es necesario adelantar urgentemente correctivos que
no requieren cambios normativos y pueden adelantarse al margen
de la aprobación de una reforma estructural. Para este fin, son
necesarios correctivos inmediatos en el sistema de información
que no pueden adelantarse sin conocer datos elementales del
sistema vigente. Por esta razón, iniciaremos acciones de litigio
estratégico, presentando Derechos de Petición dirigidos a:
✔ADRES,
sobre microdato de valores pagados por Régimen, CUM, Región,
EPS, IPS, Operador Farmacéutico y posibles estudios de
pertinencia
✔Ministerio
de Salud - OTIC, sobre inconsistencias en datos reportados a
SISMED, falta de validaciones y analítica
✔Ministerio
de Salud - MiPres, sobre inconsistencias en datos de
Prescripciones y efectos de la Política de Presupuestos Máximos
✔Ministerio
de Salud - Cuenta de Alto Costo, sobre inconsistencias en
Informes publicados y posibles estudios de pertinencia
✔Ministerio
de Salud - Med-Col-STAT, sobre inconsistencias en la Plataforma,
Informes generados y posibles estudios de pertinencia
✔Instituto
Nacional de Salud - Informes publicados y posibles estudios de
pertinencia
✔INVIMA,
sobre inconsistencias en su base de datos, posibles estudios de
pertinencia y Farmacovigilancia
Acuerdo No.15 de Política Farmacéutica en
Proyecto de Reforma a la Salud ANM
Las organizaciones más representativas de los médicos
colombianos, presentaron los 14 ACUERDOS FUNDAMENTALES de lo que
consideran esencial para el pleno desarrollo de la Ley
Estatutaria 1751 de 2015 y el Sistema de Salud en ella
establecido.
Gráfico N°40:
Acuerdo
Fundamental N°13 de POLÍTICA FARMACÉUTICA con firma de 21
organizaciones médicas

Acuerdo 13. Política farmacéutica
Avanzar en el desarrollo de la Política
Farmacéutica Nacional (PFN) establecida en el CONPES Social 155
de agosto de 2012, formulada con anterioridad a la expedición de
la Ley Estatutaria en Salud, de tal manera que, la nueva
política despliegue lo ordenado en el artículo 23 de esta ley:
“El Gobierno
Nacional establecerá una Política Farmacéutica Nacional,
programática e integral en la que se identifiquen las
estrategias, prioridades, mecanismos de financiación,
adquisición, almacenamiento, producción, compra y distribución
de los insumos, tecnologías y medicamentos, así como los
mecanismos de regulación de precios de medicamentos. Esta
política estará basada en criterios de necesidad, calidad, costo
efectividad, suficiencia y oportunidad”.
Para el efecto, se propone que la PFN sea:
• Programática,
con metodología científica y objetivos a corto, mediano y largo
plazo.
• Integral,
con elementos de integración horizontal y vertical de las
tecnologías en salud.
• Estratégica,
con vocación de soberanía tecnológica y mecanismos de
transferencia.
• Priorizada,
hacia la defensa de la salud pública y el derecho fundamental a
la salud.
• Optimizada,
en todos sus procesos de adquisición y uso pertinente.
• Sostenible,
con base en la detección y eliminación de falsas innovaciones
tecnológicas, el freno a abusos de posición dominante y la
erradicación de todas las formas de corrupción.
• Sistema
Único e Integrado de Información en Salud, para
garantizar trasparencia con acceso público a la información
epidemiológica y de todas las transacciones económicas.
Después de 9 años de proferido el CONPES 155, el
INVIMA aún mantiene inconsistencias graves en su base de datos
de medicamentos, como el manejo de códigos únicos de
medicamentos para los registros sanitarios vigentes (ATC),
coincidencias de indicaciones por principio activo, data de
titularidad de registros sanitarios, oportunidad de renovaciones
y manejo de fechas de vigencia. A cinco años del Decreto de
apertura de competencia con Biotecnológicos, la plataforma de
Biológicos aún no funciona a la perfección. No muestra la
información de registros sanitarios, no completó la asignación
del Identificador Único del Medicamento (IUM), persiste la falta
de parametrización de datos clave, entre otros aspectos.
Estas deficiencias se transmiten a otros sistemas
de información como el Sistema de Información de Precios de
Medicamentos (SISMED) y la herramienta tecnológica para
prescripción -MIPRES.
En cumplimiento del artículo 23 de la LES, el
INVIMA deberá adelantar políticas de mejor información y
educación sanitaria para la población, exigir mayor
transferencia de tecnología y contribuir al desarrollo de
capacidades nacionales crecientes en pro de mayor seguridad y en
pro de la soberanía farmacéutica.
Así mismo, se avanzará en el control de precios
de medicamentos con base en comparaciones internacionales; se
extenderá progresivamente a medicamentos de alto costo,
innovadores, genéricos, biológicos y biosimilares; control de
precios a insumos de alto costo y a ciertas tecnologías en
salud. Se considerarán las negociaciones centralizadas como
parte de esta política.
Impulsar y promover alianzas y mecanismos de
producción nacional de vacunas, de medicamentos e insumos y
productos básicos en salud, para avanzar en los conceptos de
seguridad, soberanía e independencia farmacéutica y tecnológica.
Declarar exentos de IVA los medicamentos, insumos
y tecnologías básicas en el Sistema de Salud.
Firman:
✔Academia Nacional de Medicina.
Presidente: Gabriel Carrasquilla
Gutiérrez, en representación del grupo de Acuerdos
Fundamentales.
✔Asociación Colombiana de Sociedades Científicas -ACSC. Agamenón
Quintero Villarreal, presidente.
✔Colegio Médico Colombiano -CMC. Stevenson
Marulanda Plata, presidente.
✔Asociación de Profesiones de la Salud -ASSOSALUD. Mauricio
Echeverri Diez, presidente.
✔Federación Odontológica Colombiana -FOC. María
Fernanda Atuesta Mondragón, presidente.
✔Sociedad Colombiana de Anestesiología y
Reanimación -SCARE. Olga Lucía
Herrera Losada, presidente.
✔Asociación Médica Sindical, ASMEDAS Cundinamarca. Jaime
Cuervo Saavedra, secretario general.
✔Colegio Médico de Cundinamarca y Bogotá -CMCB. Clemencia
Mayorga Ramírez, presidente.
✔Colegio Médico de Antioquia. Carlos
Eduardo Valdivieso Gelves, presidente.
✔Colegio Médico de Santander. Sandra
Milena Acevedo Rueda, presidente.
✔Colegio Médico del Cauca. Martha
Sofía Bedoya, presidente.
✔Federación Colombiana de Sindicatos Médicos -FECOLMED. Jorgenrique
Enciso Sánchez, presidente.
✔Academia Nacional de Medicina, Capítulo Nariño. Emma
Guerra Nieto, presidente.
✔Academia de Medicina de Medellín. Giovanni
García Martínez, presidente.
✔Asociación Gremial y Sindical de Cirujanos de
Ortopedia y Traumatología. Roberto
Díaz González, presidente.
✔Federación de Sindicatos de Anestesiología -FSA.
Luis Mauricio García Borrero, presidente.
✔Asociación de Epidemiología de Colombia -ASOCEPIC.
Luis Jorge Hernández Flórez, presidente.
✔Federación Nacional de Prestadores de Servicios
de Salud -FENALSALUD. Joaquín
Enrique Villamizar Zúñiga, presidente.
✔Asociación de Médicos Egresados de la U. del
Valle -AMEUV. Álvaro Bustos
Mejía, presidente.
✔Unión Gremial de Dermatólogos de Colombia. UNIDERMA.
Arturo César Argote, presidente.
✔Academia de Medicina del Valle del Cauca.
Néstor Harry Amorocho Pedraza, presidente.
| El punto "Proyección
de acciones coyunturales de Litigio y
organizacionales desde gremios de la salud",
aborda la necesidad de implementar correctivos
urgentes ante las "inducciones perversas" que
generan graves deficiencias e inconsistencias en
el funcionamiento del sistema de salud
colombiano. Estas acciones no requieren cambios
normativos profundos y pueden llevarse a cabo al
margen de una reforma estructural, centrándose
en mejoras inmediatas del sistema de
información.
Las acciones
de litigio estratégico propuestas
incluyen la presentación de Derechos de Petición
dirigidos a varias entidades clave para exigir
la corrección y transparencia de la información:
-
ADRES: Para obtener microdatos
sobre los valores pagados por régimen, CUM,
región, EPS, IPS y operador farmacéutico.
-
Ministerio de Salud - OTIC: Para
abordar las inconsistencias en los datos
reportados a SISMED y la falta de
validaciones y análisis.
-
Ministerio de Salud - MiPres: Sobre
las inconsistencias en los datos de
prescripciones y los efectos de la política
de "Presupuestos Máximos".
-
Ministerio de Salud - Cuenta de Alto Costo:
Respecto a las inconsistencias en los
informes publicados.
-
Ministerio de Salud - Med-Col-STAT:
Sobre las inconsistencias en la plataforma.
-
Instituto Nacional de Salud: Para
revisar los informes publicados.
-
INVIMA: En relación con las
inconsistencias en su base de datos y la
farmacovigilancia.
En este contexto,
se hace referencia al Acuerdo
Fundamental N°13 sobre Política Farmacéutica,
firmado por 21 organizaciones médicas, que busca
avanzar en el desarrollo de una Política
Farmacéutica Nacional (PFN) programática e
integral. Esta PFN debería ser:
-
Programática, con metodología
científica y objetivos a corto, mediano y
largo plazo.
-
Integral, con elementos de
integración horizontal y vertical de las
tecnologías en salud.
-
Estratégica, con vocación de
soberanía tecnológica y mecanismos de
transferencia.
-
Priorizada, hacia la defensa de la
salud pública y el derecho fundamental a la
salud.
-
Optimizada, en todos sus procesos
de adquisición y uso pertinente.
-
Sostenible, mediante la eliminación
de falsas innovaciones, el freno a abusos de
posición dominante y la erradicación de la
corrupción.
- Basada en un
Sistema Único e Integrado de
Información en Salud, que garantice
transparencia y acceso público a la
información epidemiológica y económica.
El documento
resalta que, a pesar de los años, el
INVIMA aún presenta graves inconsistencias en su
base de datos (códigos únicos,
indicaciones, titularidad de registros, fechas
de vigencia). Estas deficiencias se extienden a
otros sistemas como SISMED y MiPres. Para
corregir esto, se propone que el Sistema de
salud impulse políticas de mejor información,
educación sanitaria, mayor transferencia de
tecnología y contribuya a la soberanía
farmacéutica nacional. También se busca un
control de precios de medicamentos basado en
comparaciones internacionales, extendiéndose a
todos los medicamentos de alto costo,
innovadores, biológicos y biosimilares, y la
promoción de la producción nacional de insumos y
productos básicos en salud. |
|
6.
6.
Cambios estructurales en el sistema de salud: Ley 2386 de 2024
Luego, tomando en cuenta que una normatividad diseñada para la
defensa de los intereses de la salud pública fue desnaturalizada
por un cambio de gobierno y una política pública de "Todo el
poder a las EPS" (dejó de desarrollarse el Banco de la Salud
ADRES, no se amplió el "Giro Directo a Prestadores", se llenó de
inconsistencias al modelo de transparencia de precios y ventas
del mercado farmacéutico de SISMED y se dañó el acceso al
microdato de ventas y prescripción de los CUBOS de SISMED y
MiPres, se frenó el Decreto de Apertura de competencia de
medicamentos Biotecnológicos, al igual que la Resolución de
transparencia en transferencias de valor, etc. y solo para
mencionar los daños más importantes). Es necesario prevenir
estos retrocesos, con NORMATIVIDADES VIRTUOSAS con fuerza de
Ley, como las siguientes:
Ley de SOBERANÍA
FARMACÉUTICA logro de la Sociedad Civil
Ley 2386 de 25jul24 de
SOBERANÍA FARMACÉUTICA lograda por la Sociedad Civil
✔ Resumen
en Video:
Soberanía_Farmacéutica_Colombia_Ley_2386de2024_Video.mp4
✔ Resumen
en Audio:
Soberanía_Farmacéutica_Colombia_Ley_2386de2024_Video.mp4

Ver
Ley de Política Nacional de Investigación Científica, Desarrollo
Tecnológico, Innovación y Producción de la Industria
Farmacéutica para la Autonomía Sanitaria de Colombia.
Al margen de la tendencia al Maximalismo Verbal Radicalizado
con Insuficiencia Técnica y Ejecutiva, que llevó al fracaso
el Proyecto de Reforma Estructural a la Salud, organizaciones de
la Sociedad Civil, en una mesa intersectorial coordinada por el
Colegio Nacional de Químicos Farmacéuticos de Colombia,
donde participaron:
✔Asociación
de Industrias Farmacéuticas en Colombia (Asinfar),
✔Asociación
de Laboratorios Farmacéuticos de Investigación y Desarrollo (Afidro),
✔Asociación
Colombiana de la Industria Farmacéutica (Ascif),
✔Cámara
de la Industria Farmacéutica de la Asociación Nacional de
Empresarios (Andi), y
✔Asociación
Colombiana de Programas [de pregrado] de Farmacia, Ascolprofar.
Con el respaldo del Clúster Farmacéutico de la Cámara de
Comercio de Bogotá.
Y la gestión del Senador Pedro Flórez y la Representante
Jennifer Pedraza
Y los Ponentes en Senado Pedro Flórez (Comisión VI y Plenaria) y
en Cámara: Dolcey Torres (Comisión VI y Plenaria)
Demostraron que SÍ era posible aprobar una Ley de Política
Nacional de Investigación Científica, Desarrollo Tecnológico,
Innovación y Producción, de la Industria Farmacéutica para la
AUTONOMÍA sanitaria de Colombia.
El punto 6 de "Proyección
de cambios estructurales en el sistema de salud Ley
2386/24 de Soberanía Farmacéutica", destaca la
aprobación de la Ley de Soberanía Farmacéutica
como un logro significativo en contraste con los
intentos fallidos de reformas estructurales previas.
- Crítica a
Enfoques Anteriores: Señala una tendencia
basada en "Maximalismo Verbal radicalizado con
Insuficiencia Técnica y Ejecutiva" que llevó al
fracaso de proyecto de reforma estructural a la
salud. Esta tendencia desvirtuó normativas diseñadas
para la defensa de la salud pública, afectando,
entre otros, al Banco de la Salud ADRES, el giro
directo a prestadores, la transparencia de precios y
ventas en SISMED, el acceso a microdatos de SISMED y
MiPres, el Decreto de Apertura de competencia de
medicamentos Biotecnológicos, y la Resolución de
transparencia en transferencias de valor.
- Logro de la
Ley 2386 de 2024: A pesar de los fracasos
previos, organizaciones de la sociedad civil
lograron aprobar la Ley 2386 de 2024 de
Soberanía Farmacéutica. Esta ley representa
una "normatividad virtuosa con fuerza de Ley".
- Actores
Involucrados: La aprobación de esta ley fue
resultado de una mesa intersectorial coordinada por
el Colegio Nacional de Químicos Farmacéuticos de
Colombia. Contó con la participación de varias
asociaciones de la industria farmacéutica
(Asociación de Industrias Farmacéuticas en Colombia
- Asinfar, Asociación de Laboratorios Farmacéuticos
de Investigación y Desarrollo - Afidro, Asociación
Colombiana de la Industria Farmacéutica - Ascif,
Cámara de la Industria Farmacéutica de la Asociación
Nacional de Empresarios - Andi, y Asociación
Colombiana de Programas de Farmacia - Ascolprofar),
con el respaldo del Clúster Farmacéutico de la
Cámara de Comercio de Bogotá. La gestión fue
liderada por el Senador Pedro Flórez y la
Representante Jennifer Pedraza.
- Propósito de
la Ley: Este logro demostró que sí era
posible aprobar una Ley de Política Nacional de
Investigación Científica, Desarrollo Tecnológico,
Innovación y Producción de la Industria
Farmacéutica, orientada a la autonomía
sanitaria de Colombia. Lamentablemente a
más de un año de su aprobación aún no se ha
reglamentado ni implementado ninguno de sus
artículos.
|
Resumen
de Ley 2386 de 25 de julio de 2024 "Soberanía
Farmacéutica"
Título: "POR MEDIO DE LA CUAL SE ESTABLECEN LAS PAUTAS
DE LA POLÍTICA NACIONAL DE INVESTIGACIÓN CIENTÍFICA,
DESARROLLO TECNOLÓGICO, INNOVACIÓN Y PRODUCCIÓN DE LA
INDUSTRIA FARMACÉUTICA PARA LA AUTONOMÍA SANITARIA DE
COLOMBIA Y SE DICTAN OTRAS DISPOSICIONES"
I. Resumen Ejecutivo
La Ley 2386 establece las directrices para la Política
Nacional de Investigación Científica, Desarrollo
Tecnológico, Innovación y Producción en la Industria
Farmacéutica de Colombia, con el objetivo primordial de
garantizar la autonomía sanitaria del país. La ley
reconoce al sector farmacéutico como estratégico para la
salud humana y veterinaria, buscando asegurar la
disponibilidad oportuna de medicamentos seguros,
eficaces y de calidad, así como la tecnología sanitaria
indispensable para la vida, la salud y el bienestar de
la población. Se enfoca en la promoción de la
investigación, el desarrollo, la innovación y la
producción local, la cooperación internacional, el
fortalecimiento institucional, la vigilancia de la
calidad de los productos y la formación de talento
humano.
II. Temas Principales y
Objetivos Clave
1. Objeto y Ámbito de Aplicación (Título I, Artículos 1
y 2):
Objeto principal: Establecer las pautas y
principios para la Política Nacional de Investigación
Científica, Desarrollo Tecnológico, Innovación y
Producción de la Industria Farmacéutica para la
Autonomía Sanitaria de Colombia. Reconoce al sector
farmacéutico como estratégico para la salud humana y
veterinaria, buscando "proporcionar la disponibilidad
oportuna de medicamentos seguros, eficaces y de calidad,
y para la tecnología sanitaria, la cual será considerada
imprescindible para garantizar la vida, la salud y el
bienestar de la población." (Artículo 1).
Ámbito de aplicación: Se aplica a todas las
instancias que intervienen directa o indirectamente en
el desarrollo y producción de medicamentos, principios
activos, productos biológicos, fitoterapéuticos,
radiofármacos, dispositivos médicos, materias primas y
otros bienes productivos destinados a la salud humana y
veterinaria fabricados y comercializados en Colombia,
que cumplan con los estándares de calidad, seguridad y
eficacia.
2. Pautas de la Política
Nacional (Título II, Artículos 3-7):
Articulación intersectorial: La política será
diseñada por el Ministerio de Ciencia, Tecnología e
Innovación, el Ministerio de Salud y Protección Social,
el Ministerio de Comercio, Industria y Turismo, y el
INVIMA, con la asistencia de la OPS, la OMS, el
Ministerio de Educación Nacional, la academia, la
industria farmacéutica, institutos nacionales, colegios
profesionales del sector salud, aceleradoras de
innovación y la sociedad civil. (Parágrafos 1 y 2 del
Artículo 3).
Garantía de calidad: El gobierno nacional deberá
"garantizar la calidad e idoneidad de la investigación
científica, desarrollo tecnológico e innovación y
producción de la industria farmacéutica, priorizando las
necesidades de los usuarios y cumpliendo con los
estándares médicos y técnicos adecuados, en concordancia
con las normas vigentes." (Parágrafo 3 del Artículo 3).
Objetivo General (Artículo 4): "Promover y
fortalecer, en el país, la investigación científica en
el campo farmacéutico en cualquier fase, el desarrollo
tecnológico, la innovación y la manufactura de
medicamentos, que permita asegurar la disponibilidad de
medicamentos, principios activos, productos biológicos,
fitoterapéuticos, radiofármacos, dispositivos médicos,
materias primas, y otros bienes productivos... de manera
continua para atender las necesidades nacionales en
salud, favoreciendo así la autonomía sanitaria, de modo
que se evite el desabastecimiento y las concentraciones
del mercado en productos farmacéuticos y productos
farmacéuticos esenciales para la salud pública, así como
inequidades en el acceso a estos productos."
Objetivos Específicos (Artículo 5):
•
Promover la cooperación internacional, transferencia de
tecnología e intercambio de conocimientos.
•
Asegurar el acceso, disponibilidad y abastecimiento de
productos farmacéuticos y otros insumos para incentivar
la producción local y garantizar la salud pública.
•
Promover, fortalecer, estimular y propiciar las
capacidades de la industria farmacéutica nacional en
producción, desarrollo tecnológico e innovación.
•
Estimular la producción farmacéutica en Colombia con
incentivos arancelarios, créditos y aduaneros.
•
Fomentar el uso adecuado de medicamentos y
farmacovigilancia.
•
Facilitar la articulación intersectorial y alianzas para
fortalecer buenas prácticas y sostenibilidad en la
producción farmacéutica.
•
Promover la cooperación e inclusión de especialistas
connacionales residentes en el exterior.
•
Promover herramientas de vigilancia y control de
calidad, y erradicación de medicamentos falsificados.
•
Garantizar un flujo continuo de financiación a proyectos
de investigación científica.
•
Garantizar, promover y fortalecer el abastecimiento
nacional y la cadena de valor local de productos
farmacéuticos e insumos.
Lineamientos de la Política (Artículo 6):
Incluyen la producción de materias primas y
medicamentos, preparación ante emergencias, estímulo a
la Ciencia, Tecnología e Innovación (CTel),
fortalecimiento del talento humano, incentivos a la
producción de medicamentos biológicos, fitoterapéuticos,
radiofármacos y de alta tecnología para enfermedades
desatendidas, y farmacovigilancia y producción
sostenible.
Agenda Nacional de Autonomía Sanitaria (Artículo 7):
El Gobierno nacional establecerá iniciativas,
prioridades y estrategias a corto, mediano y largo plazo
para aumentar la productividad y disponibilidad de
medicamentos, materias primas farmacéuticas y
tecnologías sanitarias.
3. Cooperación Internacional,
Transferencia de Tecnología e Intercambio de
Conocimientos (Título III, Artículos 8-10):
Fortalecimiento de la capacidad de investigación:
El Gobierno nacional liderará acuerdos de cooperación
con entidades públicas, privadas, académicas e
industrias farmacéuticas de países que compartan los
objetivos de esta ley. Se realizarán encuentros
gubernamentales anuales para establecer agendas
bilaterales o multilaterales. (Artículo 8).
Fortalecimiento de la capacidad industrial: Se
establecerán vínculos de cooperación con otros países y
organismos multilaterales para investigación
farmacéutica en todas sus fases, promoviendo la
transferencia tecnológica, el intercambio de
conocimientos y la fabricación de medicamentos
esenciales. (Artículo 9).
Integración a herramientas de transferencia de
tecnología frente a emergencias sanitarias: El Gobierno
nacional acelerará esfuerzos para la colaboración
mundial liderada por la OMS, para el desarrollo,
producción y acceso equitativo a medicamentos bajo
criterios de protección y defensa de la salud. (Artículo
10).
4. Acceso, Disponibilidad y
Abastecimiento (Título IV, Artículos 11-13):
Inserción global en cadenas de abastecimiento: Se
fomentará la participación de Colombia en cadenas de
abastecimiento del sector farmacéutico, promoviendo
ventajas competitivas. (Artículo 11).
Suministro de medicamentos de alto costo: Se
incentivará a las empresas farmacéuticas a diseñar
estrategias para suministrar medicamentos de alto costo
no incluidos en el Plan de Beneficios en Salud (PBS).
(Artículo 12).
Atención de necesidades de enfermedades desatendidas:
Se incentivará el desarrollo y manufactura de productos
farmacéuticos para enfermedades desatendidas de interés
en salud pública, especialmente infecciosas o
transmitidas por vectores. (Artículo 13).
5. Fortalecimiento de la
Investigación, la Innovación, la Institucionalidad
Sanitaria Nacional, las Capacidades Locales y el Talento
Humano (Título V, Artículos 14-17):
Plan de Fortalecimiento Institucional (Artículo 14):
Se diseñará e implementará un plan para fortalecer
entidades como INVIMA, INS, Instituto Nacional de
Cancerología, FNE, ICA, IETS, entre otros.
Plan de Calidad en procesos técnicos de producción
(Artículo 15): Los procesos de producción de
medicamentos deberán ser dirigidos por un profesional
químico farmacéutico con la formación y competencias
requeridas. Se exceptúa la medicina tradicional y
ancestral.
Fortalecimiento del talento humano (Artículo 16):
Se promoverán mecanismos para fortalecer las capacidades
locales en talento humano para la innovación y la
producción farmacéutica, incluyendo la formación y
actualización de funcionarios.
Calidad de los medicamentos (Artículo 17): La
Política Nacional "deberá garantizar que los
medicamentos que se produzcan en el país y los que se
importen cumplan con los estándares de calidad y buenas
prácticas de manufactura establecidas en las
regulaciones del Ministerio de Salud y del INVIMA."
6. Financiación e Incentivos
(Título VI, Artículos 18-22):
Mecanismos arancelarios, aduaneros y de fomento
(Artículo 18): El Gobierno nacional podrá establecer
estos mecanismos para promover y fortalecer la
investigación científica, el desarrollo tecnológico, la
innovación y la producción local, reconociendo al sector
farmacéutico como estratégico.
Eficiencia en el uso de recursos (Artículo 19):
Se definirán estrategias para mejorar la eficiencia en
el uso de recursos financieros destinados a la industria
farmacéutica.
Financiación (Artículo 20): La ley se cumplirá
dentro del marco de las políticas públicas y la
situación fiscal del país, prioridades del gobierno y la
programación del gasto.
Recursos de la Asignación para CTel (Artículo 21):
Los recursos de la Asignación para la Ciencia,
Tecnología e Innovación del Sistema General de Regalías
podrán destinarse a la financiación de proyectos de
inversión para Instituciones de Educación Superior en
formación profesional en campos esenciales para la
innovación y producción farmacéutica local.
Promoción de la investigación desde IES (Artículo
22): Se establecerán mecanismos de financiación e
incentivos para la creación y funcionamiento de
Ecosistemas de Investigación que promuevan la generación
y transferencia de conocimientos y el desarrollo de
productos farmacéuticos. Estos ecosistemas podrán
incluir empresas spin-off.
7. Pedagogía y
Farmacovigilancia (Título VII, Artículos
23-24):
Uso adecuado de medicamentos y seguridad del paciente
(Artículo 23): El Ministerio de Salud y Protección
Social junto con el INVIMA promoverán actividades para
orientar el uso adecuado de medicamentos y garantizar la
seguridad de los pacientes en todas las fases de la
cadena terapéutica.
Seguridad en el Uso de Tecnologías Sanitarias
(Artículo 24): Se establecerá un marco integral de
vigilancia que comprenda farmacovigilancia,
tecnovigilancia y ecofarmacovigilancia para detectar,
evaluar, entender y prevenir efectos adversos o
contingencias relacionadas con medicamentos,
dispositivos médicos y su impacto ambiental.
8. Articulación Intersectorial
y Generación de Alianzas (Título VIII,
Artículo 25):
Se establecerán acciones para que el sector académico
(especialmente IES) cree, sostenga y mejore programas de
formación profesional en campos esenciales para la
innovación y la producción farmacéutica local,
garantizando la existencia de talento humano y la
respuesta a las necesidades del sector.
9. Disposiciones Finales
(Título IX, Artículos 26-27):
Rendición de cuentas (Artículo 26): Los
Ministerios de Ciencia, Tecnología e Innovación, Salud y
Protección Social, y Comercio, Industria y Turismo,
incluirán en su informe anual al Congreso de la
República un apartado sobre el avance de las políticas
derivadas de la aplicación de la ley durante los
primeros cinco años.
Vigencia y derogatorias (Artículo 27): La Ley
rige a partir de su publicación y deroga las
disposiciones que le sean contrarias.
III. Ideas y Hechos Más
Importantes
Autonomía Sanitaria como Pilar Central: La ley
busca una "autonomía sanitaria de Colombia" a través del
fortalecimiento de la industria farmacéutica nacional,
reconociéndola como un "carácter estratégico" para
garantizar la salud y el bienestar de la población.
Enfoque Integral: La ley abarca investigación
científica, desarrollo tecnológico, innovación,
producción, cooperación internacional, financiación,
talento humano y control de calidad, demostrando un
enfoque holístico para el sector farmacéutico.
Participación Multiactoral: La formulación e
implementación de la política requiere la articulación
de múltiples ministerios (Ciencia, Salud, Comercio,
Educación, Relaciones Exteriores), entidades públicas (INVIMA,
INS, IETS), academia, industria farmacéutica, organismos
internacionales (OPS, OMS) y la sociedad civil.
Priorización de Necesidades Nacionales: La ley
enfatiza la "atención de las necesidades nacionales en
salud", buscando evitar el desabastecimiento, las
concentraciones de mercado y las inequidades en el
acceso a productos farmacéuticos, incluyendo el fomento
de la producción para "enfermedades desatendidas".
Incentivos a la Producción Local: Se prevén
incentivos arancelarios, créditos de fomento y aduaneros
para estimular la producción farmacéutica en Colombia.
Fortalecimiento de Capacidades y Talento Humano:
Un énfasis significativo en la formación especializada
de talento humano, la creación de ecosistemas de
investigación y el fortalecimiento de las instituciones
sanitarias nacionales.
Vigilancia y Calidad: La ley subraya la
importancia de garantizar "estándares de calidad,
seguridad y eficacia" en todos los productos, con un
marco integral de farmacovigilancia, tecnovigilancia y
ecofarmacovigilancia.
Cooperación Internacional Estratégica: Se busca
establecer acuerdos de cooperación para la transferencia
de tecnología y el intercambio de conocimientos,
posicionando a Colombia en la colaboración mundial,
especialmente en respuesta a emergencias sanitarias.
Sostenibilidad y Financiamiento: La ley reconoce
la importancia de un flujo continuo de financiación para
proyectos de investigación y una gestión eficiente de
los recursos financieros, contemplando el uso de
recursos de la Asignación para Ciencia, Tecnología e
Innovación del Sistema General de Regalías.
IV. Citas Relevantes
"Establecer las pautas y principios que orientan los
principales instrumentos científicos, regulatorios y de
fomento de la Política Nacional de Investigación
Científica, Desarrollo Tecnológico, Innovación y
Producción de la Industria Farmacéutica para la
Autonomía Sanitaria de Colombia; reconociendo al sector
industrial farmacéutico para la salud humana y
veterinaria como de carácter estratégico para, así
mismo, proporcionar la disponibilidad oportuna de
medicamentos seguros, eficaces y de calidad, y para la
tecnología sanitaria, la cual será considerada
imprescindible para garantizar la vida, la salud y el
bienestar de la población." (Artículo 1. Objeto)
"Promover y fortalecer, en el país, la investigación
científica en el campo farmacéutico en cualquier fase,
el desarrollo tecnológico, la innovación y la
manufactura de medicamentos, que permita asegurar la
disponibilidad de medicamentos, principios activos,
productos biológicos, fitoterapéuticos, radiofármacos.
dispositivos médicos, materias primas, y otros bienes
productivos, que cumplan con los estándares de calidad,
seguridad y eficacia establecidos por la normatividad
vigente en Colombia, de manera continua para atender las
necesidades nacionales en salud, favoreciendo así la
autonomía sanitaria, de modo que se evite el
desabastecimiento y las concentraciones del mercado en
productos farmacéuticos y productos farmacéuticos
esenciales para la salud pública, así como inequidades
en el acceso a estos productos." (Artículo 4.
Objetivo general)
"El Gobierno nacional deberá garantizar la calidad e
idoneidad de la investigación científica, desarrollo
tecnológico e innovación y producción de la industria
farmacéutica, priorizando las necesidades de los
usuarios y cumpliendo con los estándares médicos y
técnicos adecuados, en concordancia con las normas
vigentes." (Parágrafo 3 del Artículo 3)
"El Gobierno nacional adelantará de manera
prioritaria esfuerzos para situar al país dentro de la
colaboración mundial liderada por la OMS, para acelerar
el desarrollo, la producción y, el acceso equitativo a
medicamentos bajo criterios de protección y defensa de
la salud y la vida de la población." (Artículo 10.
Integración del país a las herramientas de transferencia
de tecnología frente a emergencias sanitarias o
ambientales declaradas por la Organización Mundial de la
Salud (OMS) o el Gobierno nacional de Colombia.) |
7.
7.
Sistema Integrado Transaccional y Distribuido de Información en
Salud SITDIS
El Sistema Integrado
Transaccional y Distribuido de Información en Salud (SITDIS)
es una iniciativa de la Fundación OBSERVAMED STAR y el Colegio
Médico de Cundinamarca y Bogotá, entre otros actores, para
defender la salud pública, el ejercicio ético de la
profesión médica y el derecho fundamental a la salud.
Propuesto como una evolución del
Sistema Único e Integrado de Información en Salud (SUIIS), el
SITDIS busca gestionar datos transaccionales directos,
integrar los diversos subsistemas existentes y ser interoperable.
Su objetivo es corregir las inconsistencias y
fragmentación de los actuales subsistemas de
información en Colombia, priorizando su carácter público, la
transparencia y la búsqueda de resultados en salud.
Para lograrlo, el SITDIS buscará
estimular la implementación de la Tecnología de Libro
Mayor Distribuido (DLT) o Blockchain, en el Sistema de
Salud, lo que garantizará la inmutabilidad de los datos
(imposibilidad de adulterar la información una vez ingresada) y
la disponibilidad de la información de forma
distribuida. Además, permitirá la identificación de todos los
participantes, el registro permanente e indeleble de sus
interacciones y la protección de la información privada mediante
criptografía avanzada. Esta implementación se proyecta a partir
de año 2025. Ver
https://www.observamed.org/PLUS/SITDIS_Inicio.htm
Algunos enlaces
del respaldo documental
de esta investigación
|
EN CONSTRUCCIÓN -
EN CONSTRUCCIÓN - EN CONSTRUCCIÓN - EN CONSTRUCCIÓN - EN CONSTRUCCIÓN |
|