|
2.
Decretos, Resoluciones y Ley del PND (Ley 1753 de 2015) en
nombre de la LES
 |
Decretos,
Resoluciones y la Ley del
PND (Ley 1753 de 2015) según
Reforma Sistema de Salud (Teletón
30jul17) 1. Se crea el
Modelo Integral de Atención en Salud -MIAS- en donde se
han identificado las patologías más frecuentes entre los
colombianos y con base en ellas se identificaron 17
grupos de riesgos para los cuales se crearon rutas de
atención integral que incluyen acciones de promoción, la
prevención, el diagnóstico, el tratamiento, la
recuperación, la rehabilitación y la paliación de una
enfermedad. Los servicios asociados a dichas rutas serán
prestados por las redes integrales de prestación de
servicios de salud RIPSS
2. Se elimina el rol de las EPS respecto a la
administración de los recursos del sistema y se
centraliza está función en una institución denominada:
Administradora de los Recursos del Sistema General de
Seguridad Social en Salud –ADRES-, que se espera empiece
a funcionar el 01 de agosto de este año.
3. Las EPS, ahora Gestoras de Salud, serán las
responsables de conformar y administrar las redes
integrales de prestación de servicios de salud -RIPSS- ,
con esta decisión se da libertad a la integración
vertical de los actores del sistema.
4. La afiliación de los
colombianos será al sistema de salud y no a una EPS, de
esta forma la afiliación estará a cargo del Estado y la
movilidad entre regímenes contributivo y subsidiado es
posible de acuerdo a las condiciones económicas de las
personas.
5. Se eliminan las barreras de acceso, se prohíbe negar
la atención a una persona e imponer demoras o trámites
innecesarios, incluso manifestar razones económicas para
no prestar el servicio que necesita. De esta forma, los
derechos de petición y tutelas deberían desaparecer.
6. Se elimina el Plan Obligatorio de Salud POS y se
ofrecen servicios integrales en igualdad de condiciones
para toda la población. Esto significa que será
suministrado todo aquello que una persona necesite para
recuperarse, sin necesidad de recurrir a trámites de
autorización. La integralidad de los servicios señala
que los servicios no pueden ser fragmentados o
suspendidos los beneficios. Habrá sanciones ante la
negación de cualquier tipo de servicio.
7. Existirá una lista de exclusiones asociadas a
procedimientos experimentales, procedimientos o
tratamientos que no tengan evidencia científica,
aquellos de carácter cosmético y los que se ofrezcan en
el exterior cuando se presten en Colombia.
8. Se respeta el criterio y la autonomía de los médicos,
ellos deben actuar con ética y autorregulación para no
poner en riesgo los recursos del sistema. En caso de
comprobarse que los médicos reciben dádivas o prebendas
de cualquier origen serán sancionados.
9. Se eliminan los Comités Técnico Científicos de las
EPS, en caso de discrepancia de tipo terapéutico, las
juntas médicas de las redes de prestadores, serán las
únicas autorizadas para dirimirlos.
10. Se dará prioridad a
la atención primaria de salud, esto significa que los
agentes del sistema deben enfocarse en la promoción y
mantenimiento de la salud de las personas y las
comunidades, orientando sus esfuerzos a evitar que se
manifieste la enfermedad.
11. Se propone atención especial para las zonas
dispersas del país (distantes y desprotegidas), de esta
forma se debe garantizar a sus habitantes no solo la
afiliación, sino la disponibilidad de una red de
servicios y las condiciones óptimas para acceder a
ellos. La ley obliga al Estado a generar planes y
políticas específicas de salud para estas zonas del
país; y los hospitales públicos que allí se encuentren
no serán evaluados a partir de su rendimiento económico,
sino que se tendrán en cuenta indicadores de beneficio
social.
12. Se enfoca en mejores resultados de salud para la
población afiliada, por lo cual los actores del sistema
tendrán el reto de sacar a los pacientes de los grupos
de riesgo y mejorar sus condiciones de vida. De esta
forma, se reducirá la carga de la enfermedad y por tanto
los gastos dentro del sistema; esto hará que los actores
reciban un pago basado en resultados. 13. Los
ciudadanos deben asumir sus deberes en salud. Se
atribuye responsabilidad a los ciudadanos consigo mismos
en el cuidado de su salud adoptando hábitos de vida
saludables, previniendo enfermedades y no abusando del
sistema y de sus recursos disponibles. Sin embargo, el
incumplimiento de los deberes no debe ser una barrera de
acceso oportuno a los servicios. |
|
14. Se fortalece la regulación de precios de
medicamentos, dispositivos y servicios a través de toda
la cadena de comercialización.
15. Se prohíbe el embargo de recursos de la salud y su
uso en actividades distintas a la garantía de este
derecho. Aunque aún no es claro si existirán los
recursos para lograr que estos buenos propósitos del
sistema de ser equitativo e integral se cumplan, los
cambios significan que el usuario será el centro del
nuevo modelo de atención en salud. |
3. Documentos sobre Ley Estatutaria
de Salud publicados por el Ministerio de Salud
La página
Ley Estatutaria de Salud de MinSalud
muestra los documentos que resumen la visión del
gobierno sobre esta Ley. El punto de
Avances muestra enlaces a:
-
Decreto de Afiliación (video
de beneficios),
Decreto 2353 de 2015,
Decreto 780 de 2016,
Formule su PQRS y
Abecé de la afiliación en salud
-
Modelo Integral de Atención en Salud (MÍAS),
Normativa y documentos,
Presentaciones,
Rutas - RIAS,
Noticias,
Boletín,
Infografías,
Video Política integral de Atención
-
Eliminación del Comité Técnico Científico (CTC) -
Todo sobre MIPRES.
-
Participación ciudadana |
Retos de la LES |
Mecanismos de exclusión
ENLACES: Normativa:
Decreto 2353 de 2015,
Resolución 0330 de 2017,
Circular 060 de 2015 | Fases del procedimiento técnico
científico (1er. primer momento):
Adopción y publicación de las decisiones,
Nominación y objeciones,
Concepto técnico-científico,
Consulta a pacientes potencialmente afectados | |
Noticias:
Con sanción de Ley Estatutaria, la salud se consolida como
derecho fundamental en Colombia, ¿Cómo
vamos en el proceso de exclusiones? | Documentos:
Abecé,
Cronograma,
Sabías que el proceso de nominaciones y objeciones...
Metodologías | Fases
del procedimiento técnico científico (2do. momento):
Fase de nominación y objeciones,
Estudios técnicos del IETS ||
Otros recursos no MinSalud:
¿Qué es la
Ley Estatutaria en Salud? Video respuesta de la SDS Bogotá
en 3 minutos |
4. Documentos relacionados con últimos
proyectos de reforma al sistema de salud
De los documentos relacionados con
proyectos de Ley ordinaria que se publicaron recientemente. No
incluimos las de la trilogía anti-regulatoria AFIDRO-ASINFAR-CFANDI.
4.1. El
Proyecto del Partido Liberal en trámite. En
este documento de 30 páginas la palabra "medicamentos" aparece
solo en 4 partes: 1) En la pág.3 como parte del análisis del
presupuesto de ADRES, 2) En la pág.26 como parte del parágrafo
del Art.14 que elimina la integración vertical de las GIS
(Gestoras Integrales de Salud que propone reemplacen las EPS)
con IPS y proveedores de medicamentos y dispositivos médicos, 3)
En la pág.27 como inciso i) de las funciones de las GIS para
auditar las facturas de servicios prestados y 4) En la pág.29
como inciso g) del sistema de pago por resultados. El documento
de
Observaciones del CMCB-FMC a este proyecto solo menciona la
palabra "medicamentos" en 2 partes: En relación con la
integración vertical y el sistema de pago por resultado.
4.2. La
Revolución del sistema de salud propuesta por la Asociación
Colombiana de Hospitales y Clínicas (ACHC) no
menciona la palabra "medicamentos" ni una sola vez.
4.3. La
Propuesta de Política Publica en Salud de la Gran Junta
Médica a todos los candidatos de la primera vuelta electoral de
2018 (B1,
B2,
B3) redefine la estructura y funciones del IETS como INETIS,
propone ajustes al INVIMA e incluye los medicamentos en el
Control de Problemas y Enfermedades de Interés en Salud Pública
(CEISP) A18, pertinencia médica (A30), prescripción por DCI
(A32), sistemas de adquisición y distribución (A33) y Atención
Primaria Integral Resolutiva APIR (A37-38-51).
4.4. La
Agenda en Salud 2018 "para definir el rumbo del sector salud a
25 años de la Ley 100"
ARMI incluye el punto "Propuestas de política pública
orientadas a la equidad en el acceso y el uso óptimo de
medicamentos y productos biomédicos" (pág.43) -elaborado por el
núcleo asesor de la administración Santos- que muestra la
necesidad de ajustes urgentes a la regulación vigente.
|
Propuestas de
política pública orientadas a
la equidad en el acceso y el uso óptimo de
medicamentos y productos biomédicos
Por
Claudia Vaca, Óscar Lizarazo, Tatiana Andia,
Rodrigo Moreira, Tatiana Orjuela, Sandra Moreno
Centro de Pensamiento “Medicamentos, Información y
Poder”.
Universidad Nacional de Colombia
"En los
últimos ocho años Colombia desarrolló un modelo de
política de medicamentos
que atiende recomendaciones y tendencias internacionales
y a la vez es observado con
interés por la comunidad internacional"... "Tomando en
cuenta estos avances, pero también la necesidad de
atender las necesidades aún insatisfechas en esta
materia, en este capítulo se presentan una serie de
propuestas que intentan responder la pregunta: ¿Cuáles
son los problemas más relevantes que la ciudadanía
enfrenta actualmente sobre el acceso a sus medicamentos
y a la atención en salud?"...
p49
p52 |
p59
p63 |
|
Como puede
verse, estas "Propuestas de política pública orientadas
a la equidad en el acceso y el uso óptimo de
medicamentos y productos biomédicos" son las que más
incluyen temas consistentes relacionados con
medicamentos. El proyecto presentado por el Partido
Liberal tiene otras prioridades y -como ya se dijo- la
"Revolución del sistema de salud" propuesta por la ACHC
no menciona ni una sola vez la palabra "medicamentos".
Por esta razón, los contenidos del punto 5, buscan
incluir las medidas propuestas por el CP-MIP en el
articulado del proyecto de Ley Ordinaria de las
organizaciones médicas. |
5.
Propuesta Observamed-FMC:
Sugerencia inclusiones en proyecto de reforma
5.1. Apertura
de la competencia con
Biotecnológicos y política antimonopólica de control a abusos de posición dominante
Los gráficos de
Rituximab (Mabthera®)
y Trastuzumab (Herceptin®)
de Roche que aparecen en nuestra
PIDE sobre Regulación de precios de medicamentos,
sugieren
que dicha regulación de precios, seguramente fue la
política pública más exitosa de la administración Santos que
-luego de varios intentos- logró resultados notables con
productos institucionales e incluso algunos medicamentos que
afectan el gasto de bolsillo de los pacientes:
Pero, según el último informe de ADRES
de 2017 los recobros de prestaciones NoPOS (hoy NoPBS) llegaron
a 3,4 billones. Se estima que el 2018 llegarán a 4,4 billones y
no falta quien predice que en 2019 pasarán los 5,4 billones. Por
lo tanto, resulta contradictorio que con una regulación de
precios parcialmente exitosa, los recobros vuelvan a crecer con
un dinamismo que sigue poniendo en riesgo la viabilidad financiera del
sistema.
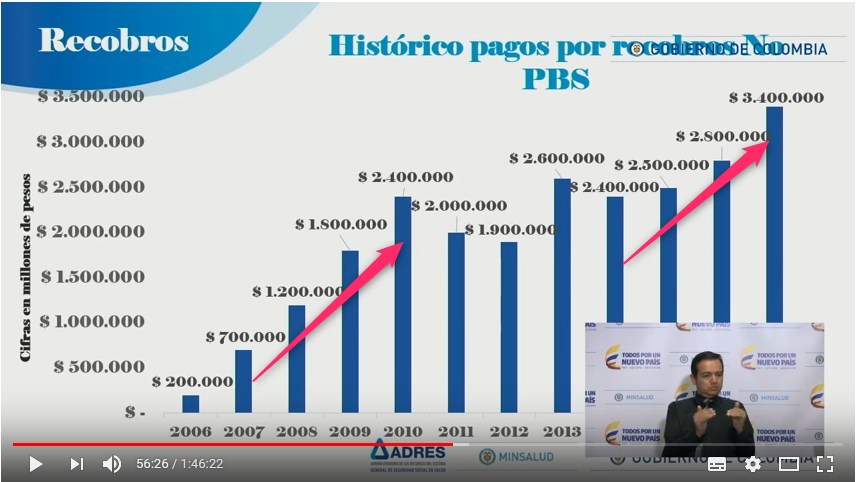
El crecimiento exponencial de recobros,
que había sido detenido en los años 2012 a 2014, volvió
a dinamizarse y pasó de 2,4 billones en 2014 a 3,4
billones en 2017 con la posibilidad de alcanzar los 4,4
billones en 2018. Esto se explica porque las multinacionales impulsan
nuevos Biotecnológicos monopólicos que reemplazan a los
regulados y otros se siguen recobrando en indicaciones
no incluidas en POS-PBS. Parcialmente derrotada ante la
Corte Constitucional y el Consejo de Estado, la
organización gremial hoy tricéfala (Afidro, Asinfar, CFAndi)
recibió a la nueva administración con una
petición de medidas inmediatas (en tono de
exigencia, firmada por el presidente de Afidro) que
incluye tres puntos "para para restaurar la confianza
entre las autoridades sanitarias y el sector privado
farmacéutico": a) Anular la apertura de la competencia
del
Decreto de Biotecnológicos, b) Bloquear la
declaratoria de interés público con fines de licencia
obligatoria solicitada por organizaciones de la sociedad
civil (para antivirales anti-Hepatitis C y otras
futruras) y c) Bloquear la fijación de precios a la
entrada de medicamentos de acuerdo con su valor
terapéutico (Circular 08 de 2018.
de derogatoria del Decreto de Biotecnológicos y adelanta
una agresiva campaña "anti-biolimbos" para desprestigiar
la "ruta abreviada".
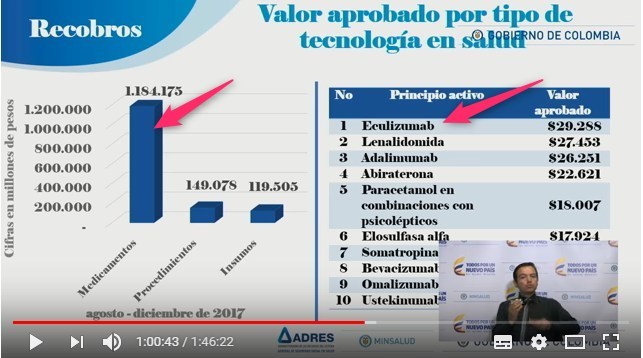 |
Según
el mismo Informe ADRES, se observa que
el peso del componente
"Medicamentos" en los recobros, sigue siendo el más
importante y que en el listado de los principios activos
más recobrados, aparecen nuevos biotecnológicos no
regulados que reemplazaron a los exitosamente regulados.
Los recobros de
biotecnológicos como Rituximab, Trastuzumab, etc, fueron
reemplazados por Eculizumab, Omalizumab, Ustekinumab,
etc., al tiempo que regulados como Adalimumab y
Bevacizumab -después de ser regulados por VMR o PRI y
ser incorporados al POS (hoy PBS) siguen entre los
medicamentos más recobrados en "indicaciones no
incluidas" (esto le da la razón a la FMC que se opuso a
las incorporaciones parciales o por indicaciones)
Por
lo tanto la primera inclusión indispensable en el
proyecto de reforma, tiene que ver con una mejor
implementación del Decreto de Biotecnológicos para abrir
efectivamente la competencia, regular mejor los
medicamentos no regulados, eliminar el fallido sistema
de inclusión parcial al POS-PBS "por indicaciones" y
fijar mecanismos de control real a los abusos de
posición dominante. |
|
Para este propósito y otros
que se mencionan a continuación, el INETIS del proyecto
de LO, debe especificar claramente a) Su carácter público,
b) Independencia financiera, c) Función específica de
evaluación de las tecnologías y SU COSTO, d) Carácter
vinculante de selección de las tecnologías más
costo-eficientes y d) Carácter vinculante de sus
propuestas de precios a la entrada para la CNPMyDM.
Aspectos que el actual IETS no toca o no cumple
suficientemente. El INETIS -antes que generador de
investigaciones "asepticas"- debe ser un
valuarte de probidad científica y capacidades técnicas para
defender al sistema de las acciones ilegales (algunas con visos
de legalidad) y las prácticas perversas
de todo tipo que emplean los actores con poder,
para llevarse una parte sustancial de los recursos
públicos. |
5.2. Regulación de precios
con PRI basado en referencia nacional e internacional "completa"
y precios a la entrada
Al analizar los precios reportados a SISMED y aplicar el concepto de
"Precio Promedio de Presentación en Sismed PPPS"
puede verse que el PPPS o
precio promedio real reportado por los laboratorios (que resulta de dividir el total
de ventas en valores reportado por el laboratorio, por canal
comercial e institucional, entre el total de las ventas en
unidades en ambos canales) muestra relaciones diferentes con el
precio regulado, cuando se trata de "marcas pioneras",
"competidores con marca" o "genéricos genuinos" según la
nomenclatura mercadotécnica propuesta por OBSERVAMED-FMC y
el Colegio Nacional de Químicos Farmacéuticos de Colombia CNQFC.
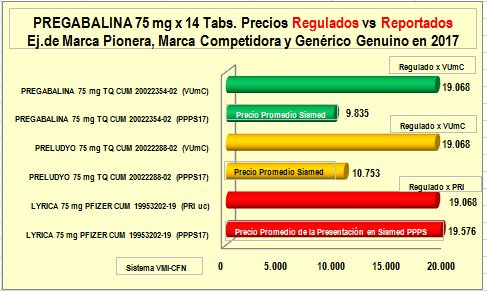 |
Por
ejemplo, al tomar
Pregabalina -el
principio activo más prescrito (y recobrado) con el aplicativo
MiPres- y comparar el precio Regulado por PRI con el PPPS de
la “marca pionera” y el precio regulado por Valor de
unidad mínima de concentración (VUmC) y el PPPS de una
“marca competidora” y un “genérico genuino” puede verse que:
a)
La “marca pionera” muestra un PPPS
igual al precio regulado por PRI
b)
La
“marca competidora” muestra
un PPPS equivalente a la mitad del precio regulado por VUmC
(que es igual al precio regulado por PRI) y
c)
El “genérico genuino” muestra
un PPPS inferior al 50% del precio regulado por VUmC
o PRI.
Esto permite plantear la hipótesis del
llamado
"efecto murciélago selectivo" en los recobros con
"marcas
competidoras" y "genéricos genuinos" que el sistema
puede pagar al
precio regulado de la marca pionera. Así, ciertos actores
(EPS y prestadores recobrantes) podrían estar apropiándose
del ahorro que debería beneficiar al sistema. Se estaría generando una “propensión
a recobrar con el precio regulado mayor” que puede no beneficiar
directamente a las farmacéuticas, pero puede ser usado como
argumento de venta y fuente de ingresos adicionales con las
"marcas competidoras" y
los "genéricos genuinos". |
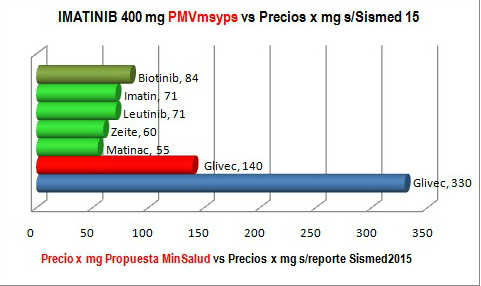 |
Para
evitar este fenómeno y mejorar la regulación en general, es
indispensable incluir en los proyectos de reforma, la fórmula del
"PRI-mejorado" (como el generado
en el proceso de Imatinib) que consiste en regular precios incluyendo en
el cálculo de
comparaciones toda la oferta disponible a nivel internacional y no
solamente la marca
pionera.
<= El gráfico muestra
el valor por mg (barra roja $140 que finalmente quedó en
206,42) que la propuesta de MinSalud, al incluir
competidores en la comparación de precios.
Todo cálculo con el "PRI-completo"
resulta más favorable para la viabilidad financiera del
sistema de salud y su aplicación con fuerza de Ley llevaría
la regulación de precios al nivel más justo, si además
incluye la fijación de precios a la entrada.
Circular08
AR.
Adicionalmente, al ajustar el cálculo de PRI con toda la
oferta disponible, puede ajustarse mejor
la “regulación por unidad mínima de
concentración VUmC”
de las presentaciones hospitalarias (multi-unitarias)
que con el sistema actual presentan precios absurdamente
elevados. |
| La
propuesta de INETIS debe incluir una
ampliación de sus funciones hacia un énfasis en la
evaluación de costo eficiencia de todas las tecnologías y la definición de
precios a la entrada (con ajustes periódicos
esencialmente técnicos). Debe definirse claramente la
inclusión del tema de medicamentos y otras tecnologías
en las políticas públicas de Control de Problemas y
Enfermedades de Interés en Salud Pública (CEISP) A18,
Pertinencia Médica (A30), Prescripción por DCI (A32),
Sistemas de adquisición y distribución (A33) y Atención
Primaria Integral Resolutiva APIR (A37-38-51). |
5.3. Regulación con
políticas públicas ajustadas a resultados en salud
La
experiencia del proceso de regulación de Imatinib (Glivec de
Novartis) también nos
enseñó que regular un solo medicamento dejando sin regulación
otras opciones de su grupo, termina por desplazar hacia los
no-regulados todos los ahorros que puedan lograse con la
regulación. Ver la explicación en el siguiente gráfico:
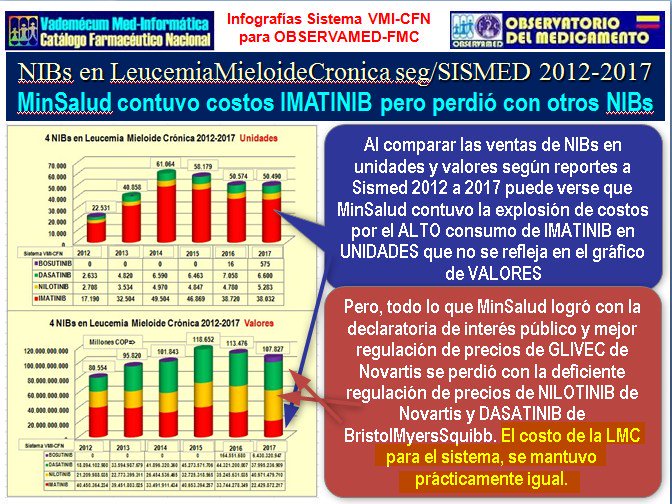
Y desde el lado positivo, la experiencia de lo logrado
con el proceso de compras centralizadas y ajustes
administrativos para Hepatitis C, nos indican que la
regulación integral por grupo terapéutico constituye la mejor
opción y debe ser incluida en el proyecto de reforma al
sistema.
Los resultados
del primer año de implementación de la
Resolución 1692 de 2017
aparecen resumidos en el
Boletín N°11 de 2018 de la Cuenta de Alto Costo publicado en
ocasión del Día Mundial contra la Hepatitis (28 de julio de
2018) que en la pág,4 dice: “La compra centralizada no solo
ha permitido la reducción de los costos del sistema de salud (92
mil millones de pesos en la primera compra), sino que también ha
minimizado las barreras en el acceso al tratamiento, ha limitado
la transmisión de la enfermedad, ha logrado la cura del 94,1% de
los pacientes que hacen arte de la cohorte de seguimiento y ha
reducido la aparición de otras hepatopatías” (ver
Instructivo, pág.4, 5 y 6 del
Boletín y gráfico N°30).
Gráfico N°30: Casos reportados a la Cuenta de Alto Costo y
Medicamentos prescritos 2017-2018
|
En resumen la implementación de la
Resolución 1692 de 2017
está resolviendo el problema de subregistro en la
notificación de casos con Hepatitis C Crónica y está
regulando la
prescripción, distribución y suministro de los
medicamentos y mejorando el sistema de información y la
identificación de pacientes, diagnósticos y
tratamientos.
Estos aprendizajes deben incluirse en
las políticas
públicas de Control de Problemas y
Enfermedades de Interés en Salud Pública (CEISP) A18,
Pertinencia Médica (A30), Prescripción por DCI (A32),
Sistemas de adquisición y distribución (A33) y Atención
Primaria Integral Resolutiva APIR (A37-38-51).
|
5.4.
Transparencia total de la información de recobros
Los
informes publicados por ADRES (6
informes del 17 de noviembre de 2017 al 22 de agosto de 2018
y
dos boletines de reclamaciones y recobros, por ejemplo) son
una muestra de las potencialidades del análisis y publicación de
la información de recobros. Los informes sobre
Síndrome de Morquio y
Enfermedad de Gaucher son ejemplos de formas en que se
pueden analizar los datos y recomendar cambios en políticas
públicas, pero, al mismo tiempo, muestran la necesidad de
múltiples informes de este tipo, por lo menos para los temas de
mayor costo y con mayor impacto en las finanzas del sistema de
salud. Urge por ejemplo un informe de las mismas características
sobre Eculizumab como el medicamento más recobrado en la
actualidad.

Y en relación con Eculizumab (Soliris
de Alexion) están los ejemplos de Asfotasa y Sebelipasa (Strensiq
y Kanuma del mismo Alexion) que hablan de la urgencia de los
cambios del IETS para el manejo de precios a la entrada.
5.5.
Estímulo a la
competencia, investigación, producción nacional y soberanía farmacéutica
xxxxxxxxxxxxxxxxxxxxx En
construcción

EN CONSTRUCCION -
EN CONSTRUCCION - EN CONSTRUCCION - EN CONSTRUCCION -
RESERVA DE ENLAcES DE INTERES - RESERVA DE
ENLACES DE INTERES - RESERVA DE ENLACES
- Sistema de salud en Colombia
https://es.wikipedia.org/wiki/Sistema_de_salud_en_Colombia
-
Los puntos clave del proyecto de reforma a la salud en
Colombia Video 27oct20 Noticias.canalrcn.com
El ministro de Salud dijo que busca centrar el sistema
en el paciente, rehumanizar la práctica profesional y
que haya transparencia contra la corrupción.
-
Proyecto de Ley 010, en contravía del derecho a la salud
23oct20 Por: Luz Marina Restrepo Uribe –
Periodista El Debate académico nacional convocado por
las universidades de Antioquia, Nacional y del Valle
realizado el 16 de octubre de 2020, planteó la
inconveniencia del proyecto de Ley 010 que cursa en el
Congreso de la República, por considerar que éste
vulnera el derecho fundamental a la salud y a la vida de
todos los colombianos, consagrado en la Constitución
Política de 1991.
-
Proyecto de reforma al sistema de salud, cerrado e
inconveniente 13oct20 UN Periódico Digital/
El profesor Mario Hernández, de la Universidad Nacional
de Colombia (UNAL), explicó en el programa UN Análisis,
de UN Radio (98.5 FM), por qué el proyecto se constituye
en una profundización de la salud como un negocio.
-
Proyecto de ley 010: una reforma para empeorar la salud
en Colombia 10oct20
El Representante Jorge Gómez y el Senador
Juan Luis Castro junto a la médica Juliana Cuellar y el
Abogado Juan Ahumada explican de que se trata esta nueva
reforma al sistema de salud.
-
Gobierno quiere aprobar a pupitrazo limpio PL 010 Senado
que reforma el Sistema de Salud
Video 25sep20 Asmedas Antioquia:
Así lo expresa en el mensaje de urgencia que envió
MinSalud a presidentes de Cámara y Senado y a
presidentes de sus respectivas comisiones Séptimas
-
REFLEXIONES SOBRE EL SISTEMA DE SALUD COLOMBIANO
Video 22mar20 Reflexiones del ex Ministro de Salud
Alejandro Gaviria escrito para el libro Al filo de la
vida: una historia del Hospital Universitario del Valle
editada por Julio Cesar Londoño
-
REFORMA AL SISTEMA DE SALUD – PROYECTO DE LEY Partido
Liberal Artículo ConsultorSalud Publicado el
19 noviembre, 2018
-
Presentada propuesta de política pública para reformar
el sistema de salud colombiano GJM - SCARE 01feb18
-
La nueva reforma a la salud en Colombia: el derecho, el
aseguramiento y el sistema de salud Oscar Bernal,
MD, D en SP,(1) Samuel Barbosa, MD.(2) (1) Maestría en
Salud Pública, Escuela de Gobierno, Universidad de los
Andes. (2) Escuela de Gobierno, UniAndes. Salud pública
Méx vol.57 no.5 Cuernavaca sep./oct. 2015
-
Reforma del Sistema de Salud. ¡Qué dolor de cabeza!
Claves para el Debate UN Oct2013 Excelente resumen
-
Reforma del Sistema de Salud, Bases para el Articulado
del Proyecto de Ley EnColombia Buen resumen sin
especificación de autor ¿Academia M. 088?
-
El sector salud en Colombia: Impacto del SGSSS después
de más de una década de reforma Mauricio Santa María
et al
-
La nueva reforma a la salud en Colombia: el derecho, el
aseguramiento y el sistema de salud Ensayo OBernal
SBarbosa
-
Análisis de la reforma al sistema general de salud en
Colombia y su impacto al fondo de solidaridad y
garantías – FOSYGA
AR
-
4MarcoRegulatorioFavorableCompetenciaFarmaceuticosAgo2009_OCDE_MEX_45048775
-
Colombia: ¿qué ha pasado con su reforma de salud?
Rubén Darío Gómez-Arias1,a, Emmanuel Nieto2,b 1 Facultad
Nacional de Salud Pública, Universidad de Antioquia.
Medellín, Colombia. 2 Facultad Nacional de Salud
Pública, Universidad de Antioquia. Medellín, Colombia. a
Médico, MSP, phD; b economista. Magíster en
Epidemiología Rev. perú. med. exp. salud publica vol.31
no.4 Lima oct./dic. 2014
-
Reforma a la salud: una propuesta de atención
diferencial 18mar13 Boletín electrónico para
los actores del sistema de salud en Colombia No. 22 –
marzo 118de 2013
-
Expectativas del nuevo proyecto para la reforma al sistema de
salud 2013 MAVR Trabajo Grado URosario mayo2913
AR
-
FORO SOBRE PROYECTO DE REFORMA A LA LEY 100/93: REFORMA A LA
SALUD 18nov13 Erwin Hernando Hernández Rincón, MD
Centro de Estudios en Salud Comunitaria - CESCUS Facultad de
Medicina Universidad de La Sabana. Ver diapositiva 11 de 33
-
La última reforma del sistema general de seguridad social en
salud Colombiano Álvaro Franco-Giraldo Facultad Nacional de
Salud Pública, Universidad de Antioquia. Medellín, Colombia.
alvarofrancogiraldo@hotmail.com Recibido 28 Enero 2012/Enviado
para Modificación 27 Junio 2012/Aceptado 30 Julio 2012
-
Sistema de
salud en Colombia: 20 años de logros y problemas Carlos
Alberto Agudelo Calderón 1 Jaime Cardona Botero 1 Jesús Ortega
Bolaños 1 Rocio Robledo Martínez 1 Ciência & Saúde Coletiva,
16(6):2817-2828, 2011
-
Luces y sombras de la reforma de la salud en Colombia Ley 100 de
1993 Francisco J. Yepes, Manuel Ramírez, Luz Helena Sánchez,
Marta Lucía Ramírez, Iván Jaramillo Primera edición: marzo de
2010 Assalud en coedición con la Universidad del Rosario,
Facultad de Economía y Mayol Ediciones S.A.
-
La reforma del sector de la salud en Colombia: ¿un modelo de
competencia regulada? Sin fecha Revista Panamericana
de Salud Pública Francisco José Yepes Luján1 y Luz Helena
Sánchez Gómez
-
PERFIL DE LOS SISTEMAS DE SALUD COLOMBIA MONITOREO Y ANÁLISIS DE
LOS PROCESOS DE CAMBIO Y REFORMA Septiembre, 2009
Área de Sistemas y Servicios de Salud- HSS-SP Organización
Panamericana de la Salud/ Organización Mundial de la Salud
-
Reforma sanitaria, equidad y derecho a la salud en Colombia
Mario Hernández 1 1 Departamento de Salud Pública y Tropical,
Facultad de Medicina, Universidad Nacional de Colombia. Ciudad
Universitaria, Carrera 30 Calle 45, Bogotá D.C., Colombia.
mha062@cable.net.co Cad.
Saúde Pública v.18 n.4 Rio de Janeiro jul./ago. 2002 http://dx.doi.org/10.1590/S0102-311X2002000400007
-
La
Reforma El Sistema de Seguridad Social en Salud de Colombia
http://www.saludcolombia.com/ Ley 100 Avances Cronología
hasta 2000 Sin fecha
LLAMA LA ATENCIÓN!!! (de
medicosgeneralescolombianos.com)
1. Llama la atención que el
gobierno y el Congreso de la República hayan acogido en su
totalidad la propuesta de Ley Estatutaria presentada por la Gran
Junta Medica Nacional. (los tres documentos a continuación son
identicos).
Para ver
el Proyecto de Ley 209 Ley Estatutaria del Gobierno haga
clic aquí
Para ver
el Proyecto Ley Estatutaria publicada en EL TIEMPO haga
clic aquí
Para ver
el original del Proyecto Ley Estatutaria presentado por la
Gran Junta Médica Haga
clic aquí.
2. Llama
la atención que la Gran Junta Médica, a pesar de de
estar de acuerdo con el gobierno en cuanto a la Ley
Estatutaria, no lo esten del todo en cuanto a la Ley
Ordinaria.
Para ver
resumen de la Ley Ordinaria publicado por EL TIEMPO haga
clic aquí.
Para ver
el texto completo del Proyecto Ley Ordinaria 210 Reforma
Salud Haga
clic aquí
3. Llama
la atención que otro de los proyectos de ley
radicados en el Congreso haya sido presentado por La
Comisión de Seguimiento a la Sentencia T-760 de 2008 y de
Reforma Estructural al Sistema de Salud y Seguridad Social –
CSR y la Alianza Nacional por un Nuevo Modelo de Salud –
ANSA –. Se trata del Proyecto de ley Ordinaria # 233, el
cual cuenta con el respaldo de la bancada del Polo
Democrático, el Partido MIRA y la Federación Médica
Colombiana con su presidente el Dr. Sergio Isaza a la
cabeza.
Para ver
el texto completo del Proyecto de Ley 233 Reforma Salud haga
clic aquí
4. Llama
la atención que otro de los proyectos de ley
radicados en el Congreso haya sido presentado por el
Representante a la Cámara Holger Diaz (Médico), quien ha
sido recientemente cuestionado por Daniel Coronel en su
columna de la Revista SEMANA por sus vinculos con Saludcoop
y su expresidente Carlos Palacino.
Para ver
el artículo original de revista SEMANA haga
clic aquí.
1.1. Tendencias globales: Consenso de
Washington y su aplicación en Colombia
El Artículo 48 de la Constitución
Política de 1991 abrió la puerta al manejo de la
Seguridad Social Pública por el sector privado. El
Congreso de esa época –por iniciativa del gobierno de
César Gaviria y su Ministro de Salud Juan Luis Londoño
De La Cuesta- aprobó la Ley 100 de 1993 que creó las
Empresas Promotoras de Salud (EPS) y Fondos Privados de
Pensiones y Cesantías.
Durante los años
2003-2010, se aplicaron en Colombia políticas públicas
de liberalización a ultranza con desregulación total y
privatización de la Seguridad Social Pública.
Entre otros
efectos, esta política generó el crecimiento exponencial
de recobros al FOSYGA y una apropiación obscena de
recursos de la salud por parte de empresas farmacéuticas
con productos monopólicos de alto costo, junto a algunas EPSs
que montaron una verdadera “industria de recobros”.
En este
período –que la FMC llama octenio de la desregulación-
los recobros al Fosyga por tecnologías “No-POS” pasaron
de 4.244 millones a 2.236.120 millones (2,2 billones),
con un alto componente de “medicamentos” que se recobraron
“a cualquier precio”.
1.2. Apuntes sobre la liquidación del ISS
El Instituto de Seguros Sociales (ISS),
Instituto Colombiano de Seguros Sociales, o Seguro
Social, fue una entidad pública creada el 26
de diciembre de 1946 encargada
de la seguridad
social, principalmente de los empleados del sector
privado con empleo formal.
Funcionó bajo cuatro negocios de la Salud: Entidad
Promotora de Salud (EPS) junto a una red de Clínicas
y Centros de Atención Ambulatoria (CAA), es decir, Instituciones
Prestadoras de servicios de Salud (IPS); asimismo
con Pensiones y
la Administradora
de Riesgos Profesionales (ARP).
El proceso de desaparición y liquidación
de la entidad se inició en 1990,
previo a la nueva constitucionalidad colombiana (ver Constitución
de Colombia de 1991). Este proceso fue abanderado
por una serie de políticos, entre ellos, el presidente
de turno
Cesar
Gaviria Trujillo (1990-1994) y el que sería próximo
presidente, Alvaro
Uribe Velez(2002-2010) quien haría realidad todas
estas políticas de privatización a
través de la ley 50 de 1990 y la ley
100 de 1993. Así, se aplicó el "recetario
económico" del Fondo
Monetario Internacional (FMI) en relación con la privatización de la Seguridad
Social Pública según lo planteado por el Consenso
de Washington
En 2007 fueron
privatizadas todas las IPS de la entidad en todo el
país. En 2008 se
privatizó la EPS y la ARP, quedando sólo con el negocio
de las pensiones.
En 2012 el
Instituto de Seguro Social dejó de existir, siendo
sustituido por Colpensiones en
la administración de las pensiones de los afiliados en
el régimen de prima media.
Cinco de las 10 recomendaciones del
"Consenso de Washington" afectaron el precio de los
medicamentos:
-
Liberalización del comercio: liberación de las
importaciones, con un particular énfasis en la
eliminación de las restricciones cuantitativas
(licencias, etc.); cualquier protección comercial
deberá tener aranceles bajos
y relativamente uniformes;
-
Liberalización de las
barreras a la inversión
extranjera directa;
-
Privatización de las empresas
estatales;
-
Desregulación: abolición de regulaciones que
impidan acceso al mercado o restrinjan la
competencia, excepto las que estén justificadas por
razones de seguridad, protección del medio ambiente
y al consumidor y una supervisión prudencial de entidades
financieras;3
-
Seguridad jurídica para
los derechos
de propiedad.3
Desde 1990, Uribe Vélez fue el promotor
(antes de la expedición de la Constitución Política
de 1991) de los procesos
de privatización de la Seguridad Social Pública,
entendida ésta como los riesgos
en salud, profesionales, cesantías y pensiones.
El último capítulo del
Proyecto de Ley, hoy Ley 50 de 1990, contenía un
articulado final que liquidaba
la seguridad social pública y daba paso al manejo
financiero de ésta por el sector
privado pero, en buena hora, el Congreso de la
República de la época no lo
aprobó y tuvo que esperar hasta la Constituyente
del 91.
La Constitución Política de 1991, en su Artículo
48, permite el manejo de la
Seguridad Social Pública por el sector privado y,
en desarrollo de ésta, se expide
por parte del Congreso y a iniciativa del
Gobierno de la época, el Liberal César
Gaviria, y su Ministro de Salud, Juan Luis
Londoño De La Cuesta, la hoy vigente
Ley 100 de 1993 que crea los Fondos Privados de
Pensiones y Cesantías y las
denominadas Empresas Promotoras de Salud (EPS).
El ministro Juan Luis Londoño de la Cuesta, al
momento de ser aprobada la Ley
100, fue claro en sus declaraciones y exclamó “bienvenidos
al negocio de la
Salud”, parafraseando al entonces Presidente
Gaviria con su frase
“bienvenidos al futuro”.
La Ley 100 de 1993, tuvo tres
propósitos claros: privatizar
la Seguridad Social Pública,
entregando los recursos al sector financiero
especulativo nacional e
internacional, liquidar la Red Pública
Hospitalaria que se venía construyendo en
el esquema del Sistema Nacional de Salud y
entregar el sistema pensional a los Fondos Privados de
Pensiones y Cesantías.
Sangre y componentes anatómicos
CRONOLOGIA
|