|
Tema:
Urgencia de nueva circular regulatoria 2018
22ene18
OBSERVAMED-FMC e IFARMA en Noticias RCN:
Urge mayor regulación
~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~
25ene17
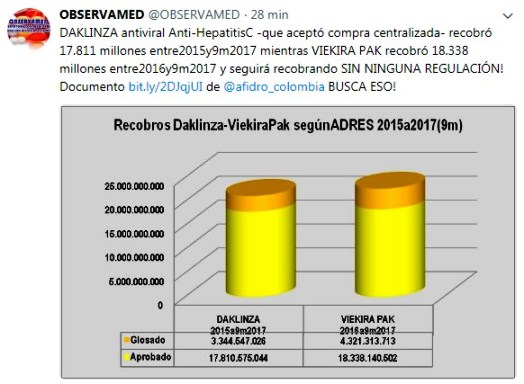
Regulación incompleta estimula prácticas perversas. Aquí
beneficia a Viekira Pak
~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~~
24ene18
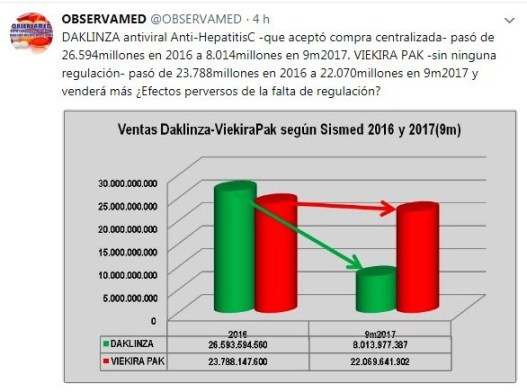
Regulación incompleta estimula prácticas perversas. Aquí
favorece a Viekira Pak
 |
Tema:
Tweets de OBSERVAMED-PLUS
~~~~~
Tema:
Opciones para acceso a
Antivirales Anti-Hepatitis C
23ene17
Recomendación de OMS sugiere tres vías y
radicalismo de Afidro: NADA
OMS propone soluciones basadas en
licencias voluntarias, escalas de precios y LICENCIAS
OBLIGATORIAS para el problema de altos costos de Antivirales
para Hepatitis C. Sofosbuvir y Daclatasvir aceptaron compra
centralizada. Radicales de @afidro_colombia no ofrecen ninguna
solución
~~~~~
Tema:
Urgencia de nueva circular regulatoria
2018
19ene18
Regulación incompleta estimula prácticas perversas. Aquí ¿Pierde
BMS?
DAKLINZA de BristolMyersSquibb el
antiviral más importante para Hepatitis C (en unidades) no tiene
NINGUNA regulación de precios, pero Sismed3Tde2017 ya muestra el
efecto de las compras centralizadas. Argumentos del documento
http://bit.ly/2DJqjUI de @afidro_colombia
son FALSOS
~~~~~
18ene18
Regulación incompleta estimula prácticas perversas.
Gana Abbvie-Abbott
VIEKIRA PAK de ABBVIE-ABBOTT el
antiviral más importante para Hepatitis C no tiene NINGUNA
regulación de precios y según Sismed3Tde2017 NO se afectó con
medidas @MinSaludCol (verPantallaProducto). Los argumentos del
documento http://bit.ly/2DJqjUI
de @afidro_colombia son FALSOS
~~~~~
Tema:
Casos y cosas del Informe Sismed de trimestre3/2017
17ene18
25 CUM con precios más exorbitantes. Muchos aún no regulados
Top 25 CUM(presentaciones) con PRECIOS MAS ELEVADOS según
reportes a Sismed3Tde2017. Vendieron COP 60.000millones con solo
2.961 unidades. Las 25 presentaciones NO están incluidas
enPOS(PlanBenef) y las paga ADRES (antes FOSYGA). Para 16CUM no
existe NINGUNA regulación de precios
~~~~~
16ene18
25 CUM con mayores ventas en valores. Muchos aún no regulados
Top 25 CUM (presentaciones) con mayor volumen de ventas
reportadas a SISMED del trimestre 3° de 2017. Vendieron COP
338.752.860.280.- De las 25 presentaciones 9 son POS (pagan EPSs
con UPC) y 16 No-POS (paga ADRES)
~~~~~
14ene18
Datos generales del Informe Sismed trimestre 3°de2017.
Misma dinámica
Informe SISMED de trim.3° de 2017 publicado el 11/dic/2017
muestra reportes de 49.510 CUM (presentaciones) de las cuales
solo 12.227 CUM muestran precios y ventas de Laboratorios por
COP 3,47 Billones (260.095.968 unidades) El acumulado de 9
meses/2017 llegó a COP 9,56 Billlones
~~~~~
Tema:
Casos y cosas de la Circular 03 de 2017
(11dic17)
13ene18
Los 20 CUM con mayor reducción de precios por Art.3°. No es gran
cosa
20 CUM con mayor reducción de PMV por Art.3° de Circular03
de2017 frente a PPP reportado a Sismed2017 vendieron COP 198.653
millones en 2016 y COP 143.366 millones en 9 meses de 2017.
Productos de Actelion/Biotoscana, Roche, Ipsen/Biopas, Janssen,
Tolmar/Tecnofarma, Abbott/Abbvie |